高一化学试题
 He可以作为核聚变材料。下列关于
He可以作为核聚变材料。下列关于  He的叙述正确的是( )
He的叙述正确的是( )
A .  He和
He和  H互为同位素
B .
H互为同位素
B .  He原子核内中子数为2
C .
He原子核内中子数为2
C .  He原子核外电子数为2
D .
He原子核外电子数为2
D .  He代表原子核内有2个质子和3个中子的氦原子
He代表原子核内有2个质子和3个中子的氦原子
 He和
He和  H互为同位素
B .
H互为同位素
B .  He原子核内中子数为2
C .
He原子核内中子数为2
C .  He原子核外电子数为2
D .
He原子核外电子数为2
D .  He代表原子核内有2个质子和3个中子的氦原子
He代表原子核内有2个质子和3个中子的氦原子
若取等质量的铝粉分别与足量的稀盐酸和NaOH溶液反应,所得氢气的体积在同样条件下相比( )
A . 与酸反应产生氢气多
B . 与碱反应产生氢气多
C . 一样多
D . 不知道铝粉的质量,无法比较
中国科学技术大学的钱逸泰教授等以CCl4和金属钠为原料,在700oC时反应制造出纳米级金刚石粉末和另一种化合物。该成果发表在世界权威的《科学》杂志上,立即被科学家们高度评价为“稻草变黄金”。同学们对此有下列一些“理解”,你认为其中错误的是( )
A . 这个反应是氧化还原反应
B . 制造过程中元素种类没有改变
C . 另一种化合物为NaCl
D . 金刚石属于碳的一种同位素
相同物质的量的下列各烃,完全燃烧后消耗氧气最多的是( )
A . 甲烷
B . 乙烷
C . 乙烯
D . 乙炔
某微粒的结构示意图为  ,它表示( )
,它表示( )
A . 氧原子
B . 氧离子
C . 氖原子
D . 钠离子
下列各组中互为同位素的是( )
A . 甲烷和乙烷
B . O2和O3
C . 正丁烷和异丁烷
D .  和
和 
 和
和 
将等物质的量的乙烷和溴蒸气混合后,在光照条件下充分反应,所得产物中物质的量最大的是( )
A . CH3CH2Br
B . CHBr2CHBr2
C . CBr3CBr3
D . HBr
工业上由氨合成硝酸并进一步制取化肥硝酸铵。工业上制备硝酸的流程如图所示。由图可知,根据绿色化学要求,生产中采用循环操作,理论上使氨气完全转化为硝酸。已知实际生产中:氨合成硝酸时,由NH3制NO的产率为94%,NO制HNO3的转化率为90%。氨与硝酸反应生成硝酸铵的转化率为94%。计算:

-
(1) 制HNO3所用的NH3占总消耗NH3(不考虑其它损耗)的质量分数为%(保留三位有效数字)。
-
(2) 写出计算过程
有NaCl、CaCl2、AlCl3三种溶液,分别与足量的AgNO3溶液反应:①若所含溶质的物质的量相等,则生成沉淀的物质的量之比是;②若生成沉淀的质量相等,则三种溶液中所含溶质的物质的量之比是.
氯元素的天然同位素有35Cl 和37Cl 。氯元素的相对原子质量为35.45,则天然氯元素中35Cl 和37Cl的原子数目之比约为( )
A . 3:1
B . 1:3
C . 3:2
D . 4:1
著名的“侯氏制碱法”的第一步反应是向饱和食盐水中通入CO2而析出NaHCO3 , 该反应可表示为:NH3+NaCl+CO2+H2O═NaHCO3↓+NH4Cl
已知NaCl、NaHCO3、NH4Cl如下温度的溶解度:
物质 | NaCl | NaHCO3 | NH4Cl |
40℃时溶解度/g | 37 | 13 | 46 |
10℃时溶解度/g | 33 |
今在40℃时,向434g饱和食盐水中通入44.8L(标准状况)NH3 , 再向溶液中通入过量的CO2 , 求:
(1)可析出NaHCO3多少克?
(2)NH4Cl能否析出?
(3)若降温至10℃,可析出NH4Cl多少克?
(4)降温至10℃时,若要析出更多的NH4Cl晶体应采取什么措施?
下列说法正确的是( )
A . 葡萄糖的分子式:C6H12O6
B . 甲烷的比例模型:  C . 次氯酸的结构式为 H-Cl-O
D . 氘的原子结构示意图:
C . 次氯酸的结构式为 H-Cl-O
D . 氘的原子结构示意图: 
m mo1乙炔跟n mo1氢气在密闭容器中反应,当其达到平衡时,生成p mol乙烯,将平衡混合气体完全燃烧生成CO2和H2O,所需氧气的物质的量是( )
A . (3m+n)mol
B . ( 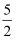 m+
m+  )mol
C . (3m+n+2p)mol
D . (
)mol
C . (3m+n+2p)mol
D . (  +
+  )mol
)mol
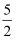 m+
m+  )mol
C . (3m+n+2p)mol
D . (
)mol
C . (3m+n+2p)mol
D . (  +
+  )mol
)mol
等物质的量的下列物质:①NaHSO4②Ca(H2PO4)2③Si ④Al2(SO4)3 ⑤ , 分别与足量的氢氧化钠溶液反应,耗碱量由多到少的顺序正确的是( )
, 分别与足量的氢氧化钠溶液反应,耗碱量由多到少的顺序正确的是( )
A . ②⑤④③①
B . ④②⑤③①
C . ④②③⑤①
D . ④⑤②③①
实验室里常用浓盐酸跟高锰酸钾反应来制取少量氯气,反应的化学方程式为:
2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O.
-
(1) 将上述方程式改写为离子方程式:.
-
(2) 反应中体现了浓盐酸的、.(填性质)
-
(3) 若反应中产生了的Cl2气体的体积 (标准状况下)为4.48L,则该反应中转移电子的物质的量是 mol,作氧化剂的浓盐酸是mol.
由以下粒子结构示意图得出的结论正确的是( )

A . ④表示的是阳离子
B . ①③属于同种元素,②④属于另一种元素
C . ②④形成的化合物是Al2O3
D . ①③的化学性质相似
观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题:

(1)属于阴离子结构示意图的是 (填字母编号).
(2)性质最稳定的原子是 (填字母编号).
(3)元素D的单质在B2中燃烧,该产物的化学式 (用元素符号).
(4)写出化合物EAB在水溶液中的电离方程式 .(用元素符号)
将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L.请回答:
-
(1) NO的物质的量为mol,NO2的物质的量为mol.
-
(2) 待产生的气体全部释放后,向溶液中加入VmL、amol•L﹣1的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为mol•L﹣1 .
-
(3) 欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为NaNO3 , 至少需要30%的双氧水g.
在含有4 mol HCl和1 mol MgSO4的混合溶液中逐滴加入Ba(OH)2溶液,产生的沉淀质量m与加入Ba(OH)2物质的量n之间的关系如右图,下列说法正确的是( )

A . a→b时的沉淀的成分为BaSO4与Mg(OH)2
B . b→c时发生的离子反应为:H++ OH-→ H2O
C . c→d时离子的物质的量:Ba2+可能大于Cl-
D . d→e时离子的物质的量:Ba2+一定大于OH-
下列选项中,表示ⅥA族某元素原子结构示意图的是( )
A .  B .
B .  C .
C .  D .
D . 
 D .
D . 
最近更新
- 如图,将矩形ABCD对折,得折痕PQ,再沿MN翻折,使点C恰好落在折痕PQ上的点C′处,点D落在D′处,其中M是BC的中
- In order to evaluate the effect that the computer has ______
- 关于自由落体运动,下列说法正确的是( )A.物体竖直向下的运动就是自由落体运动B.自由落体运动是初速度为零,加速度
- 已知某温度下CH3COOH和NH3·H2O的电离常数相等,现向10 mL浓度为0.1mol·L-1的CH3COOH溶液中
- 为保证司乘人员的安全,轿车上设有安全带未系提示系统.当乘客坐在座椅上时,座椅下的开关S1闭合,若未系安全带,则开关S2断
- 知之者不如好之者, 。(《论语》)
- 下列有关热化学方程式的评价合理的是 实验事实热化学方程式评价A已知H+(aq)+OH-(aq)=H2O(l)
- 下列有关厨房的物理知识,说法正确的是 【 】
- I should very much like to have gone to that party of theirs
- 人体组织细胞从组织液中吸收甘油的量主要取决于( ) A.组织液中甘油的浓度
- (2011•北京)如图,在梯形ABCD中,AD∥BC,对角线AC,BD相交于点O,若AD=1,BC=3,则的值为()A、
- 找出下列词语中的错别字并订正。(4分) 新陈代谢 分道扬镖 绿阴如盖 纷至踏来 生意盎
- 类推的思维方法在化学学习与研究中常会产生错误的结论。因此,类推出的结论最终要经过实践的检验才能决定其正确与否。以下几种类
- 完形填空 What do the people usually do on weekends? Some people
- 下列各句中,没有语病,句意明确的一句是 A.应俄罗斯总理普京邀请,中国国务院总理温家宝27日抵达莫斯科,对俄罗斯进行正式
- Did you know that if youneed an alarm clock to wake up in th
- 若点A(a,b)在第二象限,则点B(a-b,b-a)一定在( )A.第一象限 B.第二象限 C.
- 在KCl、FeCl3、Fe2(SO4)3三种盐配成的混合溶液中,若K+为0.15 mol,Fe3+为0.25 mol,C
- — I put him down for a well-educated man. —______ ? — I mean
- 下列操作正确的是 A.胶头滴管的使用 B.试管夹套入试管 C.熄灭酒精灯 D.液体药品的取用



