高一化学试题
硝酸铜是重要的化工原料,以下三种方法均可得到硝酸铜.
已知:2NO2+2NaOH→NaNO3+NaNO2+H2O
NO+NO2+2NaOH→2NaNO2+H2O
(以下涉及到的气体体积均为标准状况下数据):
-
(1) 甲组用a克Cu粉,在加热的条件下,与空气充分反应,然后将生成的CuO全部溶于VmL稀硝酸中,制得硝酸铜溶液,则所需稀硝酸的浓度至少为mol/L,需要质量分数为w%,密度为ρg/cm3的浓硝酸mL(均用最简分式表示).
-
(2) 乙组用b克Cu粉,全部溶于过量的稀硝酸中,溶液质量增重克,将生成的气体通入足量NaOH溶液中并同时通入氧气的体积至少L才能使生成的气体吸收完全(均用最简分式表示).
-
(3) 丙组取某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).列式计算原混合酸中硝酸的物质的量是多少?硫酸的物质的量浓度多少?

某物质在一定条件下加热分解,产物都是气体.分解方程式为2A  B↑+2C↑+2D↑.测得生成的混合气体对氢气的相对密度为d,则A的相对分子质量为( )
B↑+2C↑+2D↑.测得生成的混合气体对氢气的相对密度为d,则A的相对分子质量为( )
 B↑+2C↑+2D↑.测得生成的混合气体对氢气的相对密度为d,则A的相对分子质量为( )
B↑+2C↑+2D↑.测得生成的混合气体对氢气的相对密度为d,则A的相对分子质量为( )
A . 7d
B . 5d
C . 2.5d
D . 2d
将3.2g铜与足量浓硫酸混合加热,使其充分反应.
-
(1) 该反应的化学方程式是.
-
(2) 反应后生成的气体在标准状况下的体积为 L.
-
(3) 将反应后溶液加水稀释至50mL,所得溶液中Cu2+的物质的量浓度为 mol/L.
下列表示错误的是( )
A .  分子的空间填充模型:
分子的空间填充模型: B . 硫离子结构示意图
B . 硫离子结构示意图 C .
C .  的结构式为
的结构式为 D . 乙醛的结构简式
D . 乙醛的结构简式
 分子的空间填充模型:
分子的空间填充模型: B . 硫离子结构示意图
B . 硫离子结构示意图 C .
C .  的结构式为
的结构式为 D . 乙醛的结构简式
D . 乙醛的结构简式
加热条件下把16.8g铁粉完全溶解于100mL某浓度的硝酸中,如反应只收集到0.4mol NO2和0.1mol NO,下列说法不正确的是( )
A . 反应后溶液中NO3﹣的物质的量为0.7 mol
B . 硝酸有剩余,铁粉反应完
C . 反应后生成的盐为Fe(NO3)3和Fe(NO3)2 , 其物质的量之比为1:2
D . 该硝酸的浓度为12 mol•L﹣1
NH3加热分解为N2和H2 , 在相同条件下,测得分解后混合气体密度为分解前的 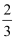 ,则氨的分解率为( )
,则氨的分解率为( )
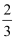 ,则氨的分解率为( )
,则氨的分解率为( )
A . 80%
B . 60%
C . 50%
D . 40%
将钠、镁、铝各0.3mol,分别放入100mL 1mol•L﹣1的硫酸中,同温同压下产生的气体的体积比是( )
A . 1:2:3
B . 6:3:2
C . 3:2:2
D . 3:1:1
CuSO4溶液对过氧化氢的分解有催化作用(2H2O2=2H2O+O2↑)。取溶质质量分数为8.5%的过氧化氢溶液20g倒入小烧杯中,向其中加入溶质质量为0.75g的CuSO4溶液10.8g,使过氧化氢完全分解。试计算:
-
(1) 产生氧气的质量;
-
(2) 反应后所得溶液中CuSO4的质量分数。
我国科学家首次合成了一种过渡金属的新核素  Hf,其单质有延展性、不易被腐蚀等特点,可应用于高科技领域.185Hf可由180Hf转化而成,下列有关180Hf、185Hf说法正确的是( )
Hf,其单质有延展性、不易被腐蚀等特点,可应用于高科技领域.185Hf可由180Hf转化而成,下列有关180Hf、185Hf说法正确的是( )
 Hf,其单质有延展性、不易被腐蚀等特点,可应用于高科技领域.185Hf可由180Hf转化而成,下列有关180Hf、185Hf说法正确的是( )
Hf,其单质有延展性、不易被腐蚀等特点,可应用于高科技领域.185Hf可由180Hf转化而成,下列有关180Hf、185Hf说法正确的是( )
A . 180Hf转化为185Hf是化学变化
B . 二者的核外电子数分别为108、113
C . 1mol180Hf的中子数比1mol185Hf少5NA
D . 在元素周期表中的位置不同
已知:Pb元素在化合物中有+4和+2两种价态:Pb02受热分解可生成Pb304、Pb0和O2:+4价的Pb能氧化浓盐酸生成Cl2 PbO能与浓盐酸反应但不能将其氧化.现将1.4mol Pb02加热一段时间分解得到O2和固体甲,向甲中加入足量的浓盐酸得到Cl2 . 反应生成的O2和Cl2的物质的盘之比为2:3,下列说法正确的是 ( )
A . 甲可能是Pb304和PbO的混合物
B . 整个反应过程中转移电子的总量为2.1mol
C . 若甲与浓盐酸充分反应,则需要消耗HCl的总量为2.8 mol
D . 甲中各物质的物质的量之比可能是n(PbO2):n(Pb304):n(PbO)=3:3:2
将 19.5 g锌粒投入250 mL 2mol/L的硫酸溶液中,试计算:(写出计算过程)
-
(1) 产生的氢气在标准状况下的体积;
-
(2) 忽略溶液体积变化体积,反应后溶液中氢离子浓度是多少?
-
(3) 要配制250 mL 2mol/L的硫酸溶液,需用质量百分数为98%,密度为1.84 g/cm3浓硫酸多少毫升?(保留三位有效数字)
m g某金属M溶于盐酸中,放出的气体在标准状况下的体积为n L,并生成氯化物MCl2 , 则金属M的相对原子质量是( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
在V L Al2(SO4)3溶液中加入过量氨水,过滤得沉淀,然后在高温中灼烧沉淀最后得白色固体m g,则溶液中SO42-的物质的量浓度是( )
A . m/27V mol·L−1
B . 2m/27V mol·L−1
C . m/34V mol·L−1
D . 3m/54V mol·L−1
用1L 0.1mol·L-1NaOH溶液吸收0.07molCO2 , 所得溶液中n(Na2CO3)和n(NaHCO3)之比约为( )
A . 3︰4
B . 3︰1
C . 2︰3
D . 3︰2
氮化铝(AlN)被广泛应用于集成电路生产领域。在氮气(N2)流中由氧化铝与焦炭在高温条件下制得氮化铝:Al2O3+N2+3C  2AlN+3CO。若有14 kg的氮气参加反应,可生成氮化铝的质量为多少?
2AlN+3CO。若有14 kg的氮气参加反应,可生成氮化铝的质量为多少?
 2AlN+3CO。若有14 kg的氮气参加反应,可生成氮化铝的质量为多少?
2AlN+3CO。若有14 kg的氮气参加反应,可生成氮化铝的质量为多少?
现有250mL浓度为2.0mol/L的硫酸和含1mol氢氧化钠的溶液,足量的铝屑.用上述原料生产Al(OH)3的量最多时消耗铝的质量为( )
A . 26g
B . 36g
C . 104g
D . 37.8g
某粒子的结构示意图为  , 关于该粒子的说法正确的是( )
, 关于该粒子的说法正确的是( )
 , 关于该粒子的说法正确的是( )
, 关于该粒子的说法正确的是( )
A . 核外电子数为16
B . 在化学反应中易得电子
C . 属于金属元素
D . 在周期表中位于第3周期 第ⅥA族
32g Cu与一定量的浓硫酸加热后,恰好完全反应,反应方程式如下:Cu+2H2SO4  CuSO4+SO2↑+2H2O问:
CuSO4+SO2↑+2H2O问:
 CuSO4+SO2↑+2H2O问:
CuSO4+SO2↑+2H2O问:
-
(1) 得到SO2气体的体积(标准状况下)是多少?
-
(2) 把所得的CuSO4 配制成250mL CuSO4溶液,所得溶液中溶质的物质的量浓度.
有两份铝粉,分别投入盐酸中(甲)和氢氧化钠溶液中(乙),在相同条件下产生氢气的体积相等,则甲、乙反应中转移电子的物质的量之比是( )
A . 1:1
B . 1:2
C . 1:3
D . 1:4
将6.4g某物质R完全燃烧生成8.8gCO2 , 化学反应方程式是2R+3O2  2CO2+4H2O则由此得出的下列结论,完全正确的一组是( )
2CO2+4H2O则由此得出的下列结论,完全正确的一组是( )
 2CO2+4H2O则由此得出的下列结论,完全正确的一组是( )
2CO2+4H2O则由此得出的下列结论,完全正确的一组是( ) ①R由碳、氢两种元素组成
②R中碳元素的质量分数是37.5%
③6.4gR燃烧还生成了7.2gH2O
④R的相对分子质量等于64.
A . ①②
B . ③④
C . ①④
D . ②③
最近更新
- 有如下算法: S1 使x←3,s←0. S2 使x←x+2. S3 使s←s+x. S4 如果s
- 两汉实行的一系列政治经济制度中,具有监察职能的是() A.刺史制度 B.郡国并行制 C.察举制 D.“三公九卿”
- 如图所示,A、B两物块的质量分别为2m和m,静止叠放在水平地面上.A、B间的动摩擦因数为μ,B与地面间的动摩擦因数为μ.
- 1.When studied in the USA, they traveled a lot. 2.It was in
- 下列叙述中,不正确的是() A.CaCO3、Ca(HCO3)2、Cu2(OH)2CO3都属于碳酸盐 B.HCl、纯碱、醋
- 把多项式分解因式的结果是() A. B. C. D.
- 欧美资产阶级革命、战争或改革完成后,各国先后建立了形式各异的资产阶级民主制度,但核心都是资产阶级掌握了国家的
- 奥运圣火“祥云”2008年5月26日来到古城扬州,从15时到16时30分进行了全长11km的火炬传递。如图5所示,火炬手
- (12分)如图,在四棱锥S—ABCD中,底面ABCD为矩形,SA⊥平面ABCD,SA=AD,M为AB中点,N为SC中点
- 下列化肥属于钾肥的是() A.CO(NH2)2 B.K2SO4 C.Ca3(PO4)
- 有专家指出,业已启幕的收入分配体制改革,若能通过适度的转移支付并强化制度执行力,则不仅能够实现财富积累有序转化为民生福利
- 已知某双链DNA分子中,G与C之和占全部碱基总数的34%,其一条链中的T与C分别占该链碱基总数的32%和18%,则在它的
- 图甲~丁中关于海带提取碘的部分实验操作及目的正确的是( )A.装置甲的作用是使海带中I2升华 B.装置乙
- A MENTORING(导师制)program is givinglife changing opportunities
- 美国是世界上的超级消费大国,与美国的贸易合作为我国的产业发展带来巨大的机遇。但如今,受金融危机影响,美国经济复苏乏力、失
- 我国地势第二、三阶梯分界线是( ) A.昆仑山﹣祁连山﹣横断山脉 B.大兴安岭﹣巴颜
- 如图,静止于水平地面的小车,一端高h 的支架上固定着一个半径为R的1/4圆弧光滑导轨,一质量m=0.2kg的物体从圆弧的
- 下图为某学校平面示意图,读图完成下题。该平面图的比例尺最有可能是A.1:10 000
- Only after you (学得) a good knowledge of law,can you become a
- 农耕文明催生了较为完善的土地制度。“这是按人口分配土地的制度,但仅分配国家掌握的土地,不触动地主的原有土地。”对这段材料



