高一化学上学期上册试题
下列有关硅材料的说法不正确的是
A.晶体硅是良好的半导体材料和制作太阳能电池的材料
B.SiO2可用于制造光导纤维
C.普通玻璃是以纯碱、石灰石和石英为原料经高温烧结而制成的
D.SiO2是酸性氧化物,它可溶于水生成硅酸
在水溶液中,下列电离方程式中正确的是
A.NaHCO3![]() Na++H++CO32- B.Ca(OH)2
Na++H++CO32- B.Ca(OH)2![]() Ca2++(OH-)2
Ca2++(OH-)2
C.Ba(AlO2)2![]() Ba2++2AlO2- D.2Fe3++3SO42-
Ba2++2AlO2- D.2Fe3++3SO42-![]() Fe2(SO4)3
Fe2(SO4)3
下列说法中,不正确的是( )
A. 胶体与溶液的本质区别是丁达尔效应
B. 氯化铁溶液可应急止血,利用的是胶体的聚沉
C. 用一束平行光线入射淀粉溶液里,从侧面可以观察到一条光亮的通路
D. 将稀硫酸逐滴加入氢氧化铁胶体中,开始时产生沉淀,继续滴加时沉淀又溶解
在印刷电路时常用氯化铁溶液作为“腐蚀液”,发生的反应为2FeCl3+Cu=2FeCl2+CuCl2向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后下列结果不可能出现的是( )
A.烧杯中有铜无铁 B.烧杯中有铁无铜
C.烧杯中铁铜都有 D.烧杯中铁铜都无
我国有丰富的海水资源,开发和利用![]() 海水资源是当前科学研究的一项重要任务。
海水资源是当前科学研究的一项重要任务。
(1)被称作海洋元素的是 (写元素符号)。
(2)工业上常以饱和食盐水为原料制备氯气,请写出反应的化学反应方程式 。
(3)从海水中提取食盐和溴的过程如下:
 |
①步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br¯,其目的为富集溴元素,请写出步骤Ⅱ的化学方程式, ![]() 。
。
②步骤Ⅱ中通入空气吹出溴,是利用了溴的 性质,步骤Ⅲ得到工业溴的化学方程式为: 。
氯气是一种化学性质活泼的气体:
(1)氢气在氯气中燃烧的现象为 。用合成的氯化氢溶于水制得一定浓度的盐酸,取用任意体积的该盐酸溶液时,下列物理量中不随所取体积![]() 的多少而变化的是 (填序号)
的多少而变化的是 (填序号)
a.溶液中HCl的物质的量 b.溶液的浓度
c.溶液中Cl-的数目 ![]() d.溶液的密度
d.溶液的密度
(2)在一密闭容器中盛有aLCl2和H2的混合气体,用电火花引燃后,恢复到原来状态,发现气体仍为aL。用足量![]() 的NaOH溶液吸收燃烧后的气体,
的NaOH溶液吸收燃烧后的气体,![]() 结果无气体剩余。由以上条件,推知原混合气体中Cl2和H2物质的量之比一定是 (填序号)
结果无气体剩余。由以上条件,推知原混合气体中Cl2和H2物质的量之比一定是 (填序号)
a.Cl2︰H2=1 b.Cl2︰H2<1 c.Cl2︰H2≥1 d.Cl2︰H2≤1
(3)新制备的氯水呈 色,说明氯水中有 分子存在。向氯水中滴入几滴AgNO3溶液,现象是 ,说明氯水中有 存在。
(4)下列氯化物中,既能由单质直接反应制得,又能由单质与酸反应制得的是 (填序号)
A.CuCl2 B.FeCl3 C.FeCl2 D.AlCl3
用NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
A.标准状况下,11.2 L 酒精含有的分子数为0.5NA
B.在常温常压下,1g H2含有的分子数为0.5NA
C.常温常压下,1mol O2的体积为22.4L
D. 0.5mol/L MgCl2溶液,含有Cl-离子数为NA
下外关于物质用途的叙述中,不正确的是( )
A. 硅可以用来制造变压器的铁芯片材料 B. 二氧化硅可以用来制造光导纤维
C. 石墨可以用来做绝缘材料 D. 石英玻璃可以用来制造耐高温的化学仪器
某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、H3AsO4、H2O和一种未知物质X.
(1)已知KBrO3在反应中得到电子,则该反应的还原剂是 。
(2)已知0.2molKBrO3在反应中得到1mol电子生成X,则X的化学式为: 。
(3)根据上述反应可推知 。
a.氧化性:KBrO3>H3AsO4 b.氧化性:H3AsO4>KBrO3
c.还原性:ASH3>X d.还原性:X>ASH3
(4)根据上述条件写出化学方程式
。
(5) 将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,用
将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,用
单线桥表示电子转移:
.下列实验中,所采取的分离方法与对应原理都正确的是
| 选项 | 目的 | 分离方法 | 原理 |
| A | 分离溶于水中的碘 | 乙醇萃取 | 碘在乙醇中的溶解度较大 |
| B | 除去CO2中的HCl | 通过饱和Na2CO3溶液、浓H2SO4的洗气瓶 | Na2CO3溶液可将CO2中的HCl转化为CO2 |
| C | 除去FeCl3溶液中的FeCl2 | 加入一定量稀硝酸,充分反应 | 硝酸会氧化FeCl2 |
| D | 由稀硫酸铜溶液得到胆矾 | 加热浓缩、冷却结晶,过滤洗涤 干燥。 | CuSO4的溶解度度受温度变化影响较大 |
下列关于Na2CO3和NaHCO3的叙述正确的是( )
A. Na2CO3俗名苏打,NaHCO3俗名纯碱
B. 受热时,NaHCO3比Na2CO3容易分解
C. Na2CO3溶液显碱性,NaHCO3溶液显酸性
D. Na2CO3和NaHCO3各1mol分别与足量的盐酸充分反应,产生CO2质量不相等
. 某MgSO4和H2SO4的混合溶液中,c(Mg2+)=2mol/Lc(SO42-)=3mol/L,若将100mL此混合溶液中的Mg2+沉淀完全,最少需加2mol/L的NaOH溶液体积是( )
A. 100mL B. 200mL C. 300mL D. 400mL
下列操作符合实验要求并能达到实验目的的是


![]()
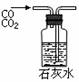
A.吸收HCl防倒吸 B.检验钠元素的存在 C.转移溶液 D.除去杂质气体CO2
下列反应中,离子方程式书写正确的是
A.Fe和盐酸反应:2Fe + 6H+ =2Fe3+ + 3H2↑
B.硫酸与氢氧化钡溶液反应:H++ ![]() + Ba2+ + OH﹣=BaSO4↓ + H2O
+ Ba2+ + OH﹣=BaSO4↓ + H2O
C.醋酸和碳酸钠溶液反应:2H++![]() =H2O+CO2↑
=H2O+CO2↑
D.石灰石和盐酸反应:CaCO3 + 2H+ =Ca2+ + CO2↑ + H2O
某固体混合物中可能含有:K+、Na+、Clˉ、CO32﹣、SO42﹣等离子,将该固体溶解所得到的溶液进行如下实验:下列说法正确的是( )

A.该混合物一定是K2CO3和NaCl
B.该混合物可能是Na2CO3和KCl
C.该混合物可能是Na2SO4和Na2CO3
D.该混合物一定是Na2CO3和NaCl
写出与下列离子方程式相对应的化学方程式。
(1)Cu2++2OH-==Cu(OH)2↓
(2)H++OH-==H2O
(3)2H++CaCO3==Ca2++H2O+CO2
(4)Cu2++Fe==Fe2++Cu
从海水中提取金属镁,正确的方法是 ( )。
A.海水![]() Mg(OH)2
Mg(OH)2![]() Mg
Mg
B.海水![]() Mg(OH)2
Mg(OH)2![]() MgCl2溶液—→MgCl2(熔融)
MgCl2溶液—→MgCl2(熔融)![]() Mg
Mg
C.海水![]() Mg(OH)2
Mg(OH)2![]() MgO
MgO![]() Mg
Mg
D.海水![]() MgCl2溶液—→MgCl2(熔融)
MgCl2溶液—→MgCl2(熔融)![]() Mg
Mg
如将物质按照单质、氧化物、酸、碱、盐分类,下列各组物质中,类别相同的是( )
A. 氧气、氧化镁、四氯化碳、水
B. 硫酸铜、氯化钠、碳酸钙、硫化钾
C. 硫酸、碳酸钠、氯化镁、氧化钠
D. 硝酸银、氢氧化钠、醋酸钠、氯化钾
下列离子方程正确的是
A.饱和石灰水中通入过量二氧化碳:OH- + CO2 = HCO3-
B.向稀硫酸中投入铁粉:2Fe +6H+ = 2Fe3+ +3H2 ↑
C.实验室制取二氧化碳:CO32- + 2H+ = H2O +CO2 ↑
D.氢氧化钡溶液中加入硫酸:H+ + OH- =H2O
在pH=1的溶液中,可以大量共存的离子组是( )
A. Na+,K+,S2﹣,Cl﹣ B. Al3+,Mg2+,SO42﹣,Cl﹣
C. K+,Na+,AlO2﹣,NO3﹣ D. K+,Na+,SO42﹣,S2O32﹣
- 图为空中飞行的足球,请画出足球所受重力的示意图.
- 下面四个图形中,线段BE是⊿ABC的高的图是( )
- 下列叙述中正确的是(设NA为阿佛加德罗常数):( )A.标准状况下,22.4L苯所含的分子数为NA B.0.1mol
- 若氢原子的核外电子绕核作半径为r的匀速圆周运动,则其角速度ω=__________;电子绕核的运动可等效为环形电流,则电
- 下列结构示意图中表示原子的是( ) A. B. C. D.
- 图4中线段长短表示影响程度大小,下列情况与甲、乙、丙、丁四图相符的是A.甘蔗制糖、制鞋、微电子、啤酒 B.甘蔗制糖
- 标出图中通电螺线管的小磁针(静止)的南北极(用“S”和“N”表示)。
- 对于绿色植物来说,可以在晴天、多云、阴天、下雨和黑夜都能进行的生命活动是( ) A.光合作用
- 用一句话概括下面新闻的内容。﹙3分) 贵州大学“211工程”建设项目全面完成,达到预期建设目标,项目管理规范,
- 有些干部为了追求所谓“政绩”,盲目攀比,不顾财力民力,不讲究实际效益,不考虑群众利益,大肆修建各类“形象工程”、“标志工
- 阅读下面这首唐诗,完成文后各题。 登 楼 唐.杜甫 花近高楼伤客心,万方多难此登临。 锦江春色来天地,玉垒①浮云变古今
- “万乘之主,千乘之君,所以制天下而征诸侯者,以其威势也。”下列各项中,与这一政治思想属于同一学派的是( ) A.“不期
- 机动车驾驶员严禁酒后驾车,交警常用装有重铬酸钾(K2Cr2O7)的仪器检测司机 是否酒后驾车,因为酒中的酒精分子可以
- 以下各句中均有成语使用错误,请简要分析。 1、这篇文章不仅结构混乱,而且文不加点,令人费解。 2、发展生产力是当前首
- 在正三棱锥V﹣ABC内,有一半球,其底面与正三棱锥的底面重合,且与正正三棱锥的三个侧面都相切,若半球的半径为2,则正三棱
- 图是测定小灯泡电功率的实验电路,电路连接正确后闭合开关,发现灯不亮,电流表指针稍有偏转,电压表指针几乎不动,产生这一现象
- 有关农业社会阶段地理环境对人类活动影响的叙述,正确的是() A.人类的主要生活来源是采集和狩猎的果实和动物 B.人类的主
- 下列关于英国君主立宪制的表述,正确的是() ①起确立的标志是《权利法案》的的实施②是以责任内阁制为核心的③其政治制度是以
- 晏殊《浣溪沙》中情致缠绵,音调婉转,对仗工整,宛若天成的诗句是:
- 一只标有“220V 100W”的灯泡(灯丝电阻不变)与一电阻串联后,接在220V电源上,电阻消耗的功率为10W,则此时(



