高一化学上学期上册试题
向Na2CO3、NaHCO3 混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示。则下列离子组在对应的溶液中一定能大量共存的是

A. a点对应的溶液中: Na+、Ca2+、SO42-、NO3-
B. b 点对应的溶液中: K+、Na+、OH-、Cl-
C. c点对应的溶液中: Na+、Ca2+、NO3-、Cl-
D. d 点对应的溶液中: Cl-、NO3-、Fe2+、Na+
为提纯或分离下列物质(括号内物质为需除去的物质),所选用的试剂和分离方法不正确的是( )
| 物质[] | 除杂试剂 | 分离方法 | |
| A | 苯(甲苯)(沸点分别为85.6℃、110.6℃) | ── | 蒸馏 |
| B | 铜粉 (铁粉) | 稀盐酸 | 溶解,过滤、洗涤 |
| C | 碘水(水) | 四氧化碳 | 萃取、分液、蒸发 |
| D | 氯化钠(碳酸氢铵) | —— | 加热 |
潮湿氯气、新制氯水以及次氯酸钠溶液都能使有色布条褪色,因为它们都含有微粒
A. HClO B. ClO- C. HCl D. Cl2
实验室用浓盐酸与二氧化锰反应制取氯气,下列有关说法中正确的是(气体体积在.标况下测定)( )
A. 若提供0.4 mol HCl,MnO2过量,则可制得氯气4.48 L
B. 若提供0.4 mol HCl,MnO2过量,则转移电子数一定为0.1mol![]()
C. 若有0.4 mol HCl参加反应,则可制得氯气2.24 L
D. 若有0.4 mol HCl被氧化,则可制得氯气2.24 L
下列A、B、C、D是中学常见的混合物分离或提纯的基本装置。请根据装置图回答下列问题:
![]() ①
①

(1) 将A、B、C、D 填入适当的空格中。
从碘水中提取碘_______;
分离酒精与水的混合物_______;
除去粗盐中的泥沙________;
与海水晒盐原理相符的是 ;
(2) 装置A中仪器①的名称是 ,冷却水是从 口进水(填“下”或“上”)。
有些科学家提出硅是“21世纪的能源”,下列有关硅及其化合物的说法正确的是
A.硅在自然界中以游离态和化合态两种形式存在
B.硅晶体是良好的半导体,可用于制造光导纤维
C.SiO2是酸性氧化物,不与任何酸发生反应
D.木材浸过水玻璃后,不易着火
阿斯匹林(分子式为 C9H8O4)是人们熟知的治感冒药,具有解热镇痛作用。它的摩尔质量是( )
A. 148g B. 148g/mol C. 180g/mol D. 146g
回答下列关于铁元素及其化合物的知识:
(1)向一支装有 FeCl3 溶液的试管中滴加 NaOH 溶液,现象为 ,
其中含铁元素的产物的化学式是 ;
(2)为了检验某未知溶液是否含有 Fe2+离子,两位同学分别设计了以下实验方案加以证明。方案一:向一支装 有该未知溶液的试管中先通入氯气,再滴加 KSCN 溶液,溶液呈现红色,证明该未知溶液含有 Fe2+离子; 方案二:向另一支装有该未知溶液的试管中先滴加 KSCN 溶液,无现象,再通入氯气,溶液变为红色,证明该未 知溶液含有 Fe2+离子;
则请回答:①你认为哪个方案较为合理 ;
②写出 Fe2+与氯气反应的离子方程式 ;
③实验室在保存含有 Fe2+离子的溶液时,为了防止 Fe2+离子变质,经常向其中加入铁粉,
其原因是(用离子方程式表示)
(4)鲜榨苹果汁是人们喜爱的饮料。由于此饮料中含有 Fe2+,鲜榨的苹果汁在空气中会由淡绿色的 Fe2+变为棕
黄色的 Fe3+,则这个变色的过程中 Fe2+被
发生。这说明维生素 C 具有 。
;若在榨汁的时候加入适量的维生素 C,可有效防止这种现象的
A.氧化性 B.还原性 C.酸性 D.碱性
下列离子反应方程式正确的是( )
A.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O = AlO2-+4NH4++2H2O
B.向Ba(OH)2溶液中滴加NaHSO4溶液至恰好为中性:
Ba2+ + OH- + H+ + SO42- = BaSO4↓+ H2O
C.少量氢氧化钙与碳酸氢钠溶液反应:Ca2+ + 2HCO3-+2OH-= CaCO3↓+ 2H2O + CO32-
D.Fe3O4溶于稀硫酸:Fe3O4 + 8H+ = 3Fe3+ + 4H2O
按要求表示下列方程式:(6分)
(1)FeCl3可使湿润的淀粉碘化钾试纸变蓝,化学方程式如下:2FeCl3 + 2KI = 2FeCl2 + I2 +2KCl.标出该反应电子转移的方向和数目(单线桥):
。
(2)在Fe3O4 +4CO![]() 3Fe+4CO2的的中, 是氧化剂;
3Fe+4CO2的的中, 是氧化剂;
(3)写出铜粉与FeCI3溶液反应的方程式: 。
(3)按要求表示下列方程式:(6分)
①FeCl3可使湿润的淀粉碘化钾试纸变蓝,化学方程式如下:2FeCl3 + 2KI = 2FeCl2 + I2 +2KCl,标出该反应电子转移的方向和数目(单线桥):
纳米材料”是当今材料科学研究的前沿,其研究成果广泛应用于催化及军事科学中.所谓“纳米材料”是指研究、开发出的直径从几纳米至几十纳米的材料,如将纳米材料分散到分散剂中,所得混合物一定具有的性质是( )
A. 无色透明 B. 有丁达尔效应
C. 所得液体呈胶状 D. 所得物质一定是悬浊液
下列离子的检验方法中,正确的是
A. 先加入AgNO3溶液,若出现白色沉淀且过滤后加稀硫酸沉淀不溶解,则该溶液中含Cl-
B. 先加BaCl2溶液,再加HCl,产生白色沉淀,则原溶液中存在SO42-离子
C. 加入用HCl酸化的BaCl2溶液,产生白色沉淀,则原溶液中存在SO42-离子
D. 加入过量HCl酸化,无沉淀产生,再加入BaCl2溶液,产生白色沉淀,则说明原溶液中存在SO42-离子
从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:

请回答下列问题:
(1)固体A的主要成分是 (写名称)
(2)铝土矿与过量烧碱反应的离子方程式为 、 .
(3)电解熔融氧化铝可制得两种单质,写出该反应化学方程式 .
(4)指出流程乙的一个缺点是 .
(5)氧化铝与焦炭的混合物在氮气中高温加热反应,制得新型非金属材料AlN与一种中学常见气体X.已知每转移6.02×1023个电子,有0.5mol化合物X生成,此反应的化学方程式 .
.实验室欲用氢氧化钠固体配制1.0mol·L-1的氢氧化钠溶液240mL:
(1)配制溶液时,一般可以分![]() 以下几个步骤:
以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却 ⑨摇动
其正确的操作顺序为___。必须用到的玻璃仪器有烧杯、胶头滴管、___。
(2)某同学欲称量氢氧化钠的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图所示。烧杯的实际质量为___g,要完成本实验该同学应称出__g氢氧化钠。

(3)如图是该同学转移溶液的示意图,图中有两处错误,请写出:

①____;
②____。
(4)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏高的是__(填字母)。
A.所用氢氧化钠已经潮解
B.溶液未冷却至室温就注入容量瓶中定容
C.在配置过程中未洗涤烧杯和玻璃棒
D.定容时,俯视容量瓶刻度线
下列过程只涉及物理变化的是
A.硫酸除锈 B.盐酸挥发 C.铁的钝化 D.氯气消毒
过氧化氢俗称双氧水,可用过氧化钡(BaO2)与稀硫酸反应来制备。过氧化氢与过氧化钡都是过氧化物,过氧化物一般可用作氧化剂、漂白剂、供氧剂等。阅读下文并回答有关问题:
(1)实验室可用过氧化氢溶液制取氧气,其反应的化学方程式是___________________,
过氧化钡还可以通过以下方式制备过氧化氢:BaO2+X+H2O==BaCO3↓+H2O2,其中物质X的化学式是____________。
(2)过氧化钠(Na2O2)也是一种过氧化物,潜水艇常用过氧化钠作供氧剂,同时维持艇内空气成分的稳定,写出这一反应的化学方程式________________________。
往甲、乙、丙、丁四个烧杯内分别放入0.1 mol的钠、氧化钠、过氧化钠和氢氧化钠,然后各加入100 mL水,搅拌,使固体完全溶解,则甲、乙、丙、丁溶液中溶质的质量分数大小顺序是( )
A.甲<乙<丙<丁 B.丁<甲<乙<丙
C.甲=丁<乙=丙 D.丁<甲<乙=丙
将饱和FeCl3溶液滴入沸水并煮沸一段时间,可得到红褐色液体,此液体不具有的性质是
A.光束通过该液体时形成光亮的“通路”
B.插入石墨电极通直流电后,有一极附近液体颜色加深
C.向该液体中加入硝酸银溶液,无沉淀产生
D.向该液体中逐滴滴入过量的稀硫酸,会看到液体先生成红褐色沉淀,后沉淀溶解
28g铜、银合金与足量的一定浓度的硝酸完全反应,放出的气体与2.24L的O2(标准 状况)混合,通入水中,恰好完全吸收,则合金中Cu与Ag的物质的量之比为( )
A.1:1 B.1:2 C.2:1 D.3:1
某有机物的结构简式为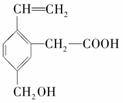 ,这种有机物不可能具有的性质是( )
,这种有机物不可能具有的性质是( )
A.能使酸性KMnO4溶液褪色 B.能发生酯化反应
C.能跟NaOH溶液反应 D.能发生水解反应
- 如图所示为一个透明介质制成的半径为R的球,透明介质的折射率为n,球心为O.透明球内有一点光源S,S距球心O的距离为R/n
- 35.Notice for the moment was ____________of the arguments ab
- (08年南充市适应性考试三理) 直线(m, n是正实数)被圆截得的弦长为4,则 的最小值是 A.2
- ________with this fiercely competitive society, _______ Eng
- 如图所示为接在频率为50Hz的低压交流电电源上的打点计时器,在纸带做匀加速直线运动时打出的一条纸带,图中所示的点是依次所
- (08年厦门双十中学月考)(15分)如图是新兴的冰上体育比赛“冰壶运动”的场地(水平冰面)示意图,实际尺寸如图为已知,要
- 读下图,完成下列问题(1).地球自转的方向是 ,同一天哈尔滨比乌鲁木齐 看到日出。 (2).图中的太阳
- 产生热力环流的根本原因是 A、相邻地区存在气流升降运动 B、地区之间存在热力差异 C、同一等压面存在气压差异 D、相
- 用斜线(/)给下面短文断句。(5分) 凌 云 台 楼 观 精 巧 先 称 平 众 木 轻 重 然 后 造 构 乃
- 下列图像不能正确反映对应变化关系的是 A.加热一定量的高锰酸钾固体 B.向一定量的二氧化锰中加入过氧化氢溶液 C.用
- 英国《自然》杂志报道,科学家在研究地下水时发现,处于地下深处两个矿物层中的水,由于受到高压的作用变成了类似“果冻”状的胶
- 下列关于单倍体的叙述,正确的是( ) A.单倍体的体细胞中只含有一个染色体组 B.一个卵细胞就是一
- 布雷顿森林体系建立后,美国财政部部长福勒得意地说:“各个行星围绕太阳转,各国的货币围绕着美元转。”这句话的实质含义是(
- 根据在蛋白质生物合成中遗传信息传递的规律,在下面的表格空白处填上相应的字母DNA双螺旋 ① T (1)_________
- 水被称为“生命之源”, 双氧水被称为“绿色氧化剂”。下列关于它们的说法中正确的是 A.都含有氢气
- 下列指定微粒的个数比为2:1的是A.Be2+离子中的质子和电子B.原子中的中子和质子C.NaHCO3晶体中的阳离子和阴离
- 对国有重点企业进行股份制改革 ( ) ①可以扩大公有资本的支配范围
- 下列关于生物膜结构探索历程的说法,不正确的是() A.最初通过对现象的推理分析得出细胞膜是由脂质组成的 B.三层结构模型
- 下列叙述中,正确的是 A.1.00 L 1.00 mol·L-1盐酸中含有6.02×1023个HCl分子 B
- 读“美国部分地区轮廓图”,回答问题:有关美国和俄罗斯的叙述,正确的是( ) A.两国领土广大,自然资源丰富,是



