物质的量的相关计算 知识点题库
下列叙述正确的是( )
A . 1 mol H2O 的质量为18g/mol
B . CH4 的摩尔质量为16g
C . 3.01×1023 个SO2 分子的质量为32g
D . 标准状况下,1 mol 任何物质的体积均为22.4L
发射卫星的火箭推进器中大多使用燃料偏二甲肼,其化学式C2H8N2 . 计算:
-
(1) 偏二甲肼的摩尔质量是;480g偏二甲肼的物质的量为.
-
(2) 偏二甲肼中碳原子与氮原子的个数之比是,其物质的量之比是;1mol偏二甲肼中含有的氢原子数目是.
某溶液中只含有K+、Na+、NO3﹣、SO42﹣四种离子(不考虑水的电离)它们的物质的量之比为1:6:3:2,该溶液所含的溶质可能是( )
A . KNO3、Na2SO4
B . K2SO4、NaNO3、KNO3
C . KNO3、Na2SO4、NaNO3
D . K2SO4、Na2SO4、KNO3
在下列条件下,两种气体的分子数一定相等的是( )
A . 同温度、同体积的N2和O2
B . 同压强、同体积的H2和CH4
C . 同质量、不同密度的N2和CO
D . 同体积、同密度的CO2和N2
下列选项中能表示阿伏加德罗常数数值的是( )
A . 1 mol H+含有的电子数
B . 标准状况下,22.4 L酒精所含的分子数
C . 1.6 g CH4含有的质子数
D . 1 L 1 mol·L-1的硫酸钠溶液所含的Na+数
阿伏加德罗常数的值为NA , 下列说法正确的是( )
A . 标准状况下,2.24LCH3OH分子中共价键的数目为0.5NA
B . 1 L1 mol·L-1HCl溶液中含有NA个HCl分子
C . 12.0 g熔融的NaHSO4中含有的阳离子数为0.1NA
D . 1mol SO2与足量O2在一定条件下充分反应生成SO3 , 共转移2 NA个电子
如下图所示的是某溶液稀释过程中,溶液的物质的浓度随溶液体积的变化曲线图,根据图中数据分析得出a值等于( )
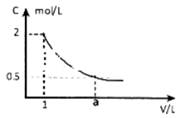
A . 2
B . 3
C . 4
D . 5
现有0.27kg质量分数为10%的CuCl2溶液。试计算:
-
(1) 溶液中CuCl2的物质的量;
-
(2) 溶液中Cu2+和Cl-的物质的量。
已知NaHSO4溶于水时电离出Na+、H+、SO42- , 某同学欲探究其化学性质,称取了12.0gNaHSO4 , 固体配成100mL溶液,做了如下实验:
①取20mL该溶液加入足量Zn粒有大量气体生成;
②取20mL该溶液加入Fe2O3后溶液变黄色;
③取20mL该溶液加入BaCl2溶液后有大量白色沉淀产生。
请回答下列问题:
-
(1) 该实验所配置的NaHSO4溶液物质的量浓度为。
-
(2) 请用离子方程式解释①中的实验现象,该实验过程中产生的气体体积为(请按标准状况下计算)。
-
(3) 请用离子方程式解释②中的实验现象。
-
(4) 请用离子方程式解释③中的实验现象。
将2.3g钠放入91.8g水中,反应完全后,溶液中Na+与H2O分子的个数比为( )
A . 1︰30
B . 1︰40
C . 1︰50
D . 1︰51
科学家制得一种新型分子O4。关于O4和O2的说法错误的是( )
A . 互为同素异形体
B . 等质量的O4和O2所含原子数相同
C . 它们的摩尔质量相同
D . 等物质的量的O4和O2所含原子数之比为2:1
物质的量是联系宏观的和微观的桥梁。
-
(1) 标准状况下,与5.6L的CH4气体含相同H原子数的H2S的质量为g。
-
(2) 将0.2mol·L-1Al2(SO4)3和0.2mol·L-1H2SO4溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中c (SO
 )=mol·L-1。若用容量瓶以质量分数为98%、密度为1.84g·cm-3的浓硫酸,配制500mL浓度成0.2mol·L-1稀硫酸,计算需要量取mL的浓硫酸。
)=mol·L-1。若用容量瓶以质量分数为98%、密度为1.84g·cm-3的浓硫酸,配制500mL浓度成0.2mol·L-1稀硫酸,计算需要量取mL的浓硫酸。
-
(3) 某无土栽培用的营养液,要求KCl、K2SO4和NH4Cl三种固体原料的物质的量之比为1︰4︰8。
①配制该营养液后c(NH
 )=0.016mol·L-1 , 溶液中c(K+)=。
)=0.016mol·L-1 , 溶液中c(K+)=。②若采用(NH4)2SO4和KCl来配制该营养液,则(NH4)2SO4和KCl物质的量之比为。
已知15gA物质和10.5gB物质恰好完全反应生成7.2gC、1.8gD和0.3molE,则E物质的摩尔质量是( )
A . 100g/mol
B . 111g/mol
C . 55g/mol
D . 55g
简单计算题,只填写结果。
-
(1) 标准状况下33.6 L H2中,所含质子个数是。
-
(2) 所含电子的物质的量为4mol的H2 , 标况下的体积是。
-
(3) 20℃时45gH2O ,所含原子个数是。
-
(4) 标况下,16gO2与14gN2的混合气体所占的体积是。
-
(5) 含原子总数约为1.204×1024的NH3 的质量是 。
下列物质中,物质的量最小的是( )
A . 常温常压下  B . 标准状况下
B . 标准状况下 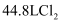 C .
C . 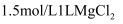 溶液中含有的
溶液中含有的  D .
D . 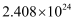 个
个 
 B . 标准状况下
B . 标准状况下 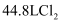 C .
C . 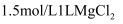 溶液中含有的
溶液中含有的  D .
D . 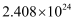 个
个 
在下面的横线上填上适当的内容。
-
(1) 6.02×1023个Na+的物质的量为,其质量为。
-
(2) NO2的摩尔质量为,标准状况下,1molNO2的气体体积为。
-
(3) 标准状况下,1molCO2的体积,含有CO2分子个数。
-
(4) 配制500mL1mol/LNa2CO3溶液,Na2CO3的物质的量为,需要Na2CO3的质量为。
448 mL某气体在标准状况下的质量为1.28 g,该气体的摩尔质量为( )
A . 64 g
B . 64
C . 64 g·mol-1
D . 32 g·mol-1
用 表示阿伏加德罗常数的数值,下列说法正确的是( )
表示阿伏加德罗常数的数值,下列说法正确的是( )
 表示阿伏加德罗常数的数值,下列说法正确的是( )
表示阿伏加德罗常数的数值,下列说法正确的是( )
A . 常温常压下,48g  和
和 含有的氧原子数均为3
含有的氧原子数均为3 B . 标准状况下,22.4L
B . 标准状况下,22.4L  含有的分子数为
含有的分子数为 C . 标准状况下,11.2L
C . 标准状况下,11.2L 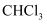 中含有
中含有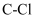 键的数目为0.5
键的数目为0.5 D . 2.7g铝与足量氢氧化钠溶液反应转移的电子数为
D . 2.7g铝与足量氢氧化钠溶液反应转移的电子数为
 和
和 含有的氧原子数均为3
含有的氧原子数均为3 B . 标准状况下,22.4L
B . 标准状况下,22.4L  含有的分子数为
含有的分子数为 C . 标准状况下,11.2L
C . 标准状况下,11.2L 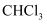 中含有
中含有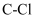 键的数目为0.5
键的数目为0.5 D . 2.7g铝与足量氢氧化钠溶液反应转移的电子数为
D . 2.7g铝与足量氢氧化钠溶液反应转移的电子数为
用10mL0.1mol·L-1BaCl2溶液恰好可分别使相同体积的Fe2(SO4)3、K2SO4和ZnSO4三种溶液中的SO 完全转化为BaSO4沉淀,则三种硫酸盐溶液物质的量浓度之比是( )
完全转化为BaSO4沉淀,则三种硫酸盐溶液物质的量浓度之比是( )
 完全转化为BaSO4沉淀,则三种硫酸盐溶液物质的量浓度之比是( )
完全转化为BaSO4沉淀,则三种硫酸盐溶液物质的量浓度之比是( )
A . 1∶3∶3
B . 1∶2∶3
C . 3∶2∶2
D . 3∶1∶1
回答下列问题
-
(1)
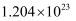 个NH
个NH 的物质的量为mol
的物质的量为mol
-
(2) 在9.5g某二价金属的氯化物中含有0.2mol
 , 该金属元素的相对原子量为。
, 该金属元素的相对原子量为。
-
(3) 在标准状况下,由CO和
 组成的混合气体为6.72L,质量为12g,此混合物中C和O原子个数比是。
组成的混合气体为6.72L,质量为12g,此混合物中C和O原子个数比是。
-
(4) 0.3mol
 分子中所含原子数与个
分子中所含原子数与个 分子中所含原子数相等。
分子中所含原子数相等。
最近更新
- 跨国公司在全球范围内利用各地的优势组织生产,经济活动的触角几乎延伸到了世界的每个角落,其根本目的是 A.促进资金、技术、
- Sometimes we climb the Baochu Hill, _______there is a small
- (2010年厦门市质量检查)The UN officials say it could be many weeks a
- 读 “地球运动示意图”,完成下列问题。 (1)当地球公转到______(字母)位置时,北半球获得太阳光热最多,这一天为
- 点A、B、C在数轴上对应的数分别为1、3、5,点P在数轴上对应的数是﹣2,点P关于点A的对称点为P1,点P1关于点B的对
- 右边电路图中与左边所示实验电路相对应的是
- 下图示细胞中含有的染色体组数目分别是()A.5个、4个 B.10个、8个 C.5
- 蔓延全球的甲流疫情,使一些不法商人借机炒作大蒜,使其价格疯涨的甚至比肉还贵﹣﹣“蒜你狠”一度成为时下流行的网络语.大蒜中
- 中国绘画有其独特的风格,在魏晋之后便梅开两朵,一支注重写实,一支注重非功利的写意。注重写实的是 ①宫廷绘画 宫廷画
- 语文综合运用。(8分) “上海世博会”将于2010年5月1日在中国上海隆重开幕。世博会是与奥林匹克运动会齐名的全球顶级盛
- 关于民族区域自治权的正确表述是 A.民族区域自治权由民族自治地方的人民政府、法院和检察院行使 B.民族区域自治权由民族自
- 下列分子中的中心原子杂化轨道的类型相同的是 A.BF3与NH3 C.BeCl2与SCl2 D.H2O与SO
- 关于植物激素的叙述,正确的是 A.植物激素是由植物体内的内分泌腺合成、分泌的微量有机物 B.植物的向光性可以说明生长素能
- 已知(x﹣2)2+|y+1|=0,则x+y的值是.
- 西亚位于“五海三洲”之地,下面答案不属于“五海”的是 ( ) A.阿拉伯海、黑海 B.红海
- —Who did you stay with yesterday? I couldn’t find you anywhe
- (化学方程式2分,其余每空1分,共7分)某实验小组的同学用碳酸钠粉末、粒状大理石、稀盐酸、浓盐酸、稀硫酸这几种药品,探究
- 下列各句中,没有语病的一句是 A.这个结论,既然有根据,但是如果不能说明地球上的无数生物怎样经历变异而达到它们相当完善
- 关于点电荷的下列说法中正确的是A.体积较大的带电体一定不能看成点电荷B.足够小(例如体积小于1mm3)的电荷,一定可以看
- 一半径为4米的水轮如图,水轮圆心O距离水面2米,已知水轮每分钟转动4圈,如果当水轮上点P从水中浮现时(图中点P0)开始计



