盐类水解的应用 知识点题库
-
(1) 在25℃条件下将pH=11的氨水稀释100倍后溶液的pH为(填序号) .A . 9 B . 13 C . 11~13之间 D . 9~11之间
-
(2) 25℃时,向0.1mol/L的氨水中加入少量氯化铵固体,当固体溶解后,测得溶液pH减小,主要原因是(填序号) .A . 氨水与氯化铵发生化学反应 B . 氯化铵溶液水解显酸性,增加了c(H+) C . 氯化铵溶于水,电离出大量铵离子,抑制了氨水的电离,使c(OH﹣)减小
-
(3) 室温下,如果将0.1mol NH4Cl和0.05mol NaOH全部溶于水,形成混合溶液(假设无损失),
①和两种粒子的物质的量之和等于0.1mol.
②和两种粒子的物质的量之和比OH﹣多0.05mol.
-
(4) 已知某溶液中只存在OH﹣、H+、NH4+、Cl﹣四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
A.c(Cl﹣)>c(NH4+)>c(H+)>c(OH﹣)
B.c(Cl﹣)>c(NH4+)>c(OH﹣)>c(H+)
C.c(Cl﹣)>c(H+)>c(NH4+)>c(OH﹣)
D.c(NH4+)>c(Cl﹣)>c(OH﹣)>c(H+)
①若溶液中只溶解了一种溶质,该溶质的名称是,上述离子浓度大小顺序关系中正确的是(选填序号).
②若上述关系中C是正确的,则溶液中溶质的化学式是.
③若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl) c(NH3•H2O)(填“>”、“<”、或“=).
-
(1) 盐碱地因含较多的NaCl、Na2CO3 , 使得土壤呈碱性,不利于作物生长,通过施加适量石膏粉末(主要含有CaSO4 , 微溶于水)来降低土壤的碱性.用离子方程式和必要的文字解释CaSO4的作用.
-
(2) SOCl2是一种无色或淡黄色液体,遇水剧烈反应得到二氧化硫和氯化氢,是一种常用的脱水剂.将SOCl2与FeCl3•6H2O混合并加热,可得到无水FeCl3 , 得到无水FeCl3的化学方程式为.
①0.1mol/L NH4Cl ②0.1mol/L CH3COONH4③0.1mol/L NH4HSO4④0.1mol/L NH3•H2O和0.1mol/L NH4Cl混合液 ⑤0.1mol/L NH3•H2O
请根据要求填写下列空白:
-
(1) 溶液①呈 性(填“酸”、“碱”或“中”),其原因是(用离子方程式表示)
-
(2) 在上述五种溶液中,pH最小的是;c(NH4+)最小的是 (填序号)
-
(3) 比较溶液②、③中c(NH4+)的大小关系是②③(填“>”、“<”或“=”)
-
(4) 若④溶液显碱性,则溶液中的离子浓度由大到小为.
-
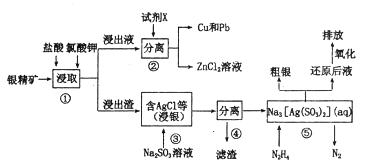
(1) 步骤①当盐酸的浓度和KCO3的量一定时,为提高浸取率可采取的措施是、(问题中要求举两项)。
-
(2) 步骤②试剂X为,步骤④滤渣中除含单质硫外,还含有的成分有。
-
(3) 步骤③反应的化学方程式为。
-
(4) 步骤⑤反应的离子方程式为。
-
(5) “粗银”(含Ag、Cu、Zn、Au)可用立式电解槽电解精炼,纯银作阴极,电解液采用硝酸和硝酸银的混合溶液。硝酸浓度不能过大,其原因是。
-
(6) 此类工厂排出的废水中含有的NO3ˉ对人类健康造成危害。科技人员在碱性条件下用Al粉将NO3ˉ还原成N2。缺点是处理后的水中生成了AlO2ˉ,仍然对人袭健康有害。
已知25℃,Ksp(Al(OH)3]=1.3×10-33 Al(OH)3
 H++H2O+AlO2ˉ K=1.0×10-13
H++H2O+AlO2ˉ K=1.0×10-13①25℃时,欲将上述处理过的水中的AlO2ˉ降到1.0×10-6mol/L,需调节溶液的pH=,此时水中c(Al3+)=mol/L
②25℃时,Al(OH)3溶于NaOH溶液反应的平衡常数K=
-
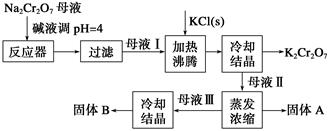
(1) 向Na2Cr2O7母液中加碱液调pH的目的是。
-
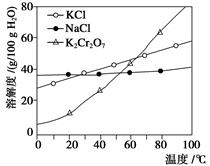
(2) 通过冷却结晶析出大量K2Cr2O7的原因是。
-
(3) 固体A的主要成分为(填化学式),用热水洗涤固体A,回收的洗涤液转移到母液(填“I”“Ⅱ”或“Ⅲ”)中,既能提高产率又可使能耗降低。
-
(4) 测定产品中K2Cr2O7含量的方法如下:称取产品试样2.500 g 配成250 mL溶液,用移液管取出25.00 mL于碘量瓶中,加入10 mL 2 mol·L-l H2SO4溶液和足量KI溶液(铬的还原产物为Cr3+),放置于暗处5 min,然后加入100 mL蒸馏水、3 mL 淀粉指示剂,用0.1200 mol·L-l Na2S2O3标准溶液滴定(已知I2+ 2S2O32-=2I-+S4O62-)。
①酸性溶液中KI 与K2Cr2O7反应的离子方程式为。
②若实验中共用去Na2S2O3标准溶液40.00 mL,则所得产品中重铬酸钾的纯度为%( 保留2 位小数,设整个过程中其他杂质不参与反应)。
| 弱酸化学式 | HX | HY | H2CO3 |
| 电离平衡常数 | 7.8×10-9 | 3.7×10-15 | K1=4.4×10-7 K2=4.7×10-11 |
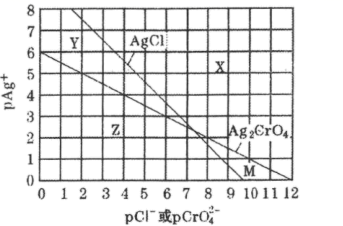
下列推断正确的是( )
 增大
D . 向Cl- , CrO42-均为0.1mol·L-1的混合溶液中逐滴加入稀硝酸银溶液,先析出AgCl沉淀
增大
D . 向Cl- , CrO42-均为0.1mol·L-1的混合溶液中逐滴加入稀硝酸银溶液,先析出AgCl沉淀
 溶液与
溶液与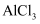 溶液混合制取
溶液混合制取 D . 锅炉水垢中含有
D . 锅炉水垢中含有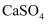 , 可先用饱和
, 可先用饱和 溶液浸泡,再用盐酸除去
溶液浸泡,再用盐酸除去
- 已知正四面体形分子E和直线型分子G反应,生成四面体形分子L和直线型分子M。(组成E分子的元素的原子序数小于10,组成G分
- 有X,Y,Z三种金属,只有Z在自然界中主要以单质形式存在.如果把Y加入X的硝酸盐溶液中,Y表面有X析出.据此判断这三种金
- _______,we have learned about 2,000 English words. A.Instea
- ......
- 以前人们认为,材料的强度和韧性这两种属性不可兼得。但某工程团队利用“电纺”技术,开发出细小的聚丙烯腈纳米纤维,并通过小喷
- .每个词语中都有错别字的一组是 A.突如奇来 措手不及 胫渭分明 鳞次栉比 B.誓不两立 集思广议 砌磋琢磨 直上九宵
- 西汉太中大夫东方朔撰文上书汉武帝,所用竹简需两人抬进宫,以后改变携书不方便现象得益于发明了
- 广西一所学校新校规禁止男女同学在教室或走廊等地单独交谈。就此事,你班进行一场激烈的讨论,有人赞成,有人反对。请你根据下表
- (本题满分14分)在中,角所对的边分别为,且满足,. (1)求的面积; (2)若,求的值.
- 阅读下列材料 材料一:山东自古以来就是中国领土,德国在山东的一切权利应直接归还中国;至于二十一条、1918年中日关于山东
- 食品卫生与健康密切相关,下列做法会导致食品对人体有害的是() ①在棒棒糖中加入过量亮绿颜料(一种含铅、铬的化合物,俗称铅
- 下列说法中,正确的是 ( ) A.分子和原子的区别就在于分子大,原子小 B.由分子构成的物质发生化学变化时,分
- 一定条件下,化学反应2H2+O2═2H2O的能量变化如图所示,则反应的热化学方程式可表示为() A. H2(g)+
- 下列四项基本实验操作中,正确的是 ( )
- 如图,矩形ABCD的顶点A、B的坐标分别为(-4,0)和(2,0),BC=.设直线AC与直线x=4交于点E.(1)求以直
- 已知函数. (Ⅰ)求的最小正周期; (Ⅱ)求在上的最大值和最小值。
- (本小题满分14分)如图5,是△的重心,、分别是边、上的动点,且、、三点共线.(1)设,将用、、表示; (2)设,,证明
- 目前,科学家提出了一种最经济最理想的获得氢能源的循环体系(如图)。下列说法错误的是 ( )A. 燃料电池能
- 下列各句中,加点的成语使用不恰当的一句是 ( ) A.有的父母习惯在饭桌上表
- 100 mL浓度为2 mol·L-1的盐酸跟过量的锌片反应,为加快反应速率,又不影响生成氢气的总量,可采用的方法是(



