水的电离 知识点题库
常温下,下列各组离子一定能在指定溶液中大量共存的是( )
A . 使酚酞变红色的溶液中:Na+、Al3+、SO42﹣、Cl﹣
B .  =1×10﹣13mol•L﹣1的溶液中:NH4+、Ca2+、Cl﹣、NO3﹣
C . 与Al反应能放出H2的溶液中:Fe2+、K+、NO3﹣、SO42﹣
D . 水电离的c(H+)=1×10﹣13mol•L﹣1的溶液中:K+、Na+、AlO2﹣、CO32﹣
=1×10﹣13mol•L﹣1的溶液中:NH4+、Ca2+、Cl﹣、NO3﹣
C . 与Al反应能放出H2的溶液中:Fe2+、K+、NO3﹣、SO42﹣
D . 水电离的c(H+)=1×10﹣13mol•L﹣1的溶液中:K+、Na+、AlO2﹣、CO32﹣
 =1×10﹣13mol•L﹣1的溶液中:NH4+、Ca2+、Cl﹣、NO3﹣
C . 与Al反应能放出H2的溶液中:Fe2+、K+、NO3﹣、SO42﹣
D . 水电离的c(H+)=1×10﹣13mol•L﹣1的溶液中:K+、Na+、AlO2﹣、CO32﹣
=1×10﹣13mol•L﹣1的溶液中:NH4+、Ca2+、Cl﹣、NO3﹣
C . 与Al反应能放出H2的溶液中:Fe2+、K+、NO3﹣、SO42﹣
D . 水电离的c(H+)=1×10﹣13mol•L﹣1的溶液中:K+、Na+、AlO2﹣、CO32﹣
25℃时,水中存在平衡:H2O⇌H++OH﹣△H>0,下列叙述正确的是( )
A . 加入稀氨水,平衡逆向移动,c(OH﹣)降低,Kw不变
B . 加入少量固体CuSO4 , c (H+)增大,Kw不变
C . 加入少量固体CH3COONa,平衡逆向移动,c (H+)降低,Kw不变
D . 加热到90℃,Kw增大,溶液仍呈中性,pH不变
25℃时,水的电离达到平衡: H2O  H++ OH-ΔH > 0 ,下列叙述正确的是( )
H++ OH-ΔH > 0 ,下列叙述正确的是( )
 H++ OH-ΔH > 0 ,下列叙述正确的是( )
H++ OH-ΔH > 0 ,下列叙述正确的是( )
A . 将水加热,Kw增大,pH不变
B . 向水中加入少量盐酸,c(H+)增大,Kw不变
C . 向水中加入NaOH固体,平衡逆向移动,c(OH-) 降低
D . 向水中加入AlCl3固体,平衡逆向移动,c(OH-) 增大
下列各种离子一定能大量共存的是( )
A . 强碱性溶液中:Na+、K+、AlO2-、CO32-
B . 含有大量Fe3+的溶液中:NH4+、SCN-、Cl-、K+
C . pH=7的溶液中:NH4+、Al3+、SO42-、CO32-
D . c(OH-)=1×10-13mol/L的溶液中:K+、Fe2+、Cl-、NO3-
25℃时,部分物质的电离平衡常数如表所示:
|
化学式 |
CH3COOH |
NH3·H2O |
H2CO3 |
H2SO3 |
|
电离平衡常数 |
1.7×10-5 |
1.7×10-5 |
K1=4.3×10-7 K2=5.6×10-11 |
K1=1.3×10-2 K2=6.3×10-8 |
请回答下列问题:
-
(1) H2CO3的第二级电离平衡常数的表达式K2=。
-
(2) 相同温度下,等pH的CH3COONa溶液、Na2CO3溶液和Na2SO3溶液,三种溶液的物质的量浓度c(CH3COONa)、c(Na2CO3)、c(Na2SO3)由大到小排序为。
-
(3) 用足量Na2CO3溶液吸收工业尾气中少量SO2气体,发生反应的离子方程式为。
-
(4) 25℃时,向0.1 mol•L-1的氨水中缓缓少量CO2气体的过程中(忽略溶液体积的变化),下列表达式的数值变小的是______。A .
 B .
B .  C .
C .  D .
D . 
-
(5) 能证明醋酸是弱酸的实验事实是(填写序号)。
① 相同条件下,浓度均为0.1 mol•L-1的盐酸和醋酸,醋酸的导电能力更弱
② 25℃时,一定浓度的CH3COOH、CH3COONa混合溶液的pH等于7
③ CH3COOH溶液能与NaHCO3反应生成CO2
④ 0.1mol•L-1 CH3COOH溶液可使紫色石蕊试液变红
-
(6) 向冰醋酸中逐滴加水,溶液导电性随加入水的体积变化如图所示。
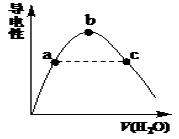
① a、b、c三点溶液中CH3COOH的电离程度由大到小的顺序是。
② a、c两点对应的溶液分别吸收氨气,若两溶液最终pH均为7(25℃时),则a点溶液中的c(CH3COO-)c点溶液中的c(NH4+)。(填“<”、“>”或“=”)
在常温下,某无色溶液中,由水电离出的c(H+)=1×10-14mol·L-1 , 则该溶液中,一定能大量共存的离子是( )
A . K+、Na+、MnO4-、SO42-
B . Na+、CO32-、AlO2-、Cl-
C . K+、Na+、Cl-、Br-
D . K+、Cl-、Ba2+、HCO3-
常温下将pH=8的NaOH溶液稀释1000倍,稀释后溶液中c(Na+)与c(OH-)之比接近( )
A . 1:1
B . 1:102
C . 102:1
D . 1:103
下列溶液中的离子关系正确的是( )
A . 相同温度下,0.2 mol·L-1的醋酸溶液与0.1mol·L-1的醋酸溶液中c(H+)之比大于2 : 1
B . pH=3的醋酸和pH=3的FeCl3溶液中,由水电离出的c(H+)相等
C . 0.1 mol﹒L-1NaHSO4溶液中:c(H+)=c(SO 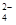 ) +c(OH-)
D . pH=4、浓度均为0.1 mol·L-1的CH3COOH、CH3COONa 混合溶液中:c(CH3COO-)-c(CH3COOH)=10-4-10-10mol/L
) +c(OH-)
D . pH=4、浓度均为0.1 mol·L-1的CH3COOH、CH3COONa 混合溶液中:c(CH3COO-)-c(CH3COOH)=10-4-10-10mol/L
25℃时,某稀溶液中由水电离产生的c(H+)为1×10-10 , 下列说法错误的是( )
A . 该溶液一定不是中性
B . NH4+、Na+、Cl-、HCO3- 在该溶液不能共存
C . 该溶液的pH一定是10
D . 该溶液中水的电离受到抑制
下列操作会使H2O的电离平衡向正方向移动,且所得溶液呈酸性的是( )
A . 向水中加入少量的CH3COONa
B . 向水中加入少量的NaHSO4
C . 加热水至100 ℃,pH=6
D . 向水中加少量的CuSO4
将1 mL 0.1 mol·L-1的H2SO4溶液加入纯水中制成200 mL溶液,该溶液中由水自身电离产生的c(H+)最接近于( )
A . 1×10-3 mol·L-1
B . 1×10-11 mol·L-1
C . 1×10-7 mol·L-1
D . 1×10-13 mol·L-1
弱电解质电离情况可以用电离度和电离平衡常数表示,下表是常温下几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb),请回答下面问题:
|
酸或碱 |
电离平衡常数(Ka或Kb) |
|
CH3COOH |
1.8×10-5 |
|
HNO2 |
4.6×10-4 |
|
HCN |
5×10-10 |
|
HClO |
3×10-8 |
|
NH3•H2O |
1.8×10-5 |
-
(1) CH3COONH4的水溶液呈(选填“酸性”、“中性”或“碱性”)。理由是。溶液中各离子浓度大小关系是。
温度t℃时,某NaOH稀溶液中c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12,请回答下列问题:
-
(2) 该温度下水的离子积常数Kw=。
-
(3) 该NaOH溶液中由水电离出的c(OH-)是mol/L。
-
(4) 给该NaOH溶液加热(水不挥发),pH=。(填变大、变小或不变)
下列说法错误的是( )
A . 常温下,pH=5的氯化铵溶液中由水电离出的c(H+)=1×10-5mol·L-1
B . 将Na2CO3溶液从常温加热至80℃,溶液的碱性增强
C . 常温下,0.1mol·L-1CH3COOH溶液pH=3,说明CH3COOH是弱电解质
D . 常温下,pH为11的氨水溶液中加入氯化铵固体,溶液pH增大
下列说法错误的是( )
A . 0.1mol/L 的硫酸铵溶液中:C(NH  )>C(SO
)>C(SO  )
B . 25℃ 时 pH=2 的醋酸溶液中水电离出的 C(H+)=10-12mol/L
C . 配制 FeCl3溶液,应加少量盐酸
D . 将 Al2(SO4)3溶液蒸干,灼烧得 Al2O3
)
B . 25℃ 时 pH=2 的醋酸溶液中水电离出的 C(H+)=10-12mol/L
C . 配制 FeCl3溶液,应加少量盐酸
D . 将 Al2(SO4)3溶液蒸干,灼烧得 Al2O3
 )>C(SO
)>C(SO  )
B . 25℃ 时 pH=2 的醋酸溶液中水电离出的 C(H+)=10-12mol/L
C . 配制 FeCl3溶液,应加少量盐酸
D . 将 Al2(SO4)3溶液蒸干,灼烧得 Al2O3
)
B . 25℃ 时 pH=2 的醋酸溶液中水电离出的 C(H+)=10-12mol/L
C . 配制 FeCl3溶液,应加少量盐酸
D . 将 Al2(SO4)3溶液蒸干,灼烧得 Al2O3
下列有关水的叙述正确的是( )
A . 水是一种非电解质
B . 纯水中c(H+)随着温度的升高而降低
C . 由液态水结成冰的过程是一个熵增的过程
D . 25℃时浓度相同的氢氧化钠溶液与醋酸钠溶液,水的电离度前者小于后者
常温下,向20 mL 0.1 mol·L-1 NaHC2O4溶液中缓慢滴加等浓度的NaOH溶液,混合溶液的温度与滴加NaOH溶液体积的关系如图所示,下列说法错误的是( )
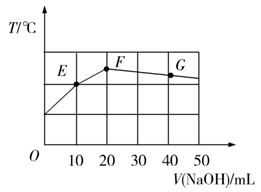
A . E点存在:2c(Na+)=3c(H2C2O4)+3c(HC2O  )+3c(C2O
)+3c(C2O  )
B . F点存在:c(OH-)>c(H+)+c(HC2O
)
B . F点存在:c(OH-)>c(H+)+c(HC2O  )+c(H2C2O4)
C . G点存在:c(Na+)>c(C2O
)+c(H2C2O4)
C . G点存在:c(Na+)>c(C2O  )>c(OH-)>c(HC2O
)>c(OH-)>c(HC2O  )
D . 滴加过程中,水的电离程度先变大,后变小
)
D . 滴加过程中,水的电离程度先变大,后变小
 )+3c(C2O
)+3c(C2O  )
B . F点存在:c(OH-)>c(H+)+c(HC2O
)
B . F点存在:c(OH-)>c(H+)+c(HC2O  )+c(H2C2O4)
C . G点存在:c(Na+)>c(C2O
)+c(H2C2O4)
C . G点存在:c(Na+)>c(C2O  )>c(OH-)>c(HC2O
)>c(OH-)>c(HC2O  )
D . 滴加过程中,水的电离程度先变大,后变小
)
D . 滴加过程中,水的电离程度先变大,后变小
下列有关电解质溶液的说法正确的是( )
A . 向0.1mol•L-1氨水中滴加等浓度的CH3COOH溶液至过量,水的电离程度一直增大
B . 常温下,pH=2的某酸HA与pH=12的某碱BOH等体积混合溶液呈酸性,则HA为强酸,BOH为弱碱
C . 0.2mol•L-1CH3COOH溶液中的c(H+)是0.1mol•L-1CH3COOH溶液中的c(H+)的2倍
D . 浓度均为0.1mol•L-1的NH4HSO4溶液与NaOH溶液等体积混合后:c(SO  )=c(Na+)>c(NH
)=c(Na+)>c(NH  )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
 )=c(Na+)>c(NH
)=c(Na+)>c(NH  )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
常温下,向20mL浓度均为0.1mol·L-1的HA与NaA的混合溶液中,分别滴加浓度均为0.1mol·L-1的HCl、NaOH两种溶液,混合溶液的pH变化情况如图所示。已知Ka(HA)=10-4.76。下列说法正确的是( )
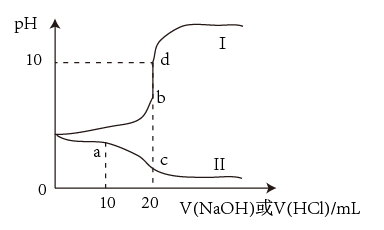
A . 滴加HCl溶液的曲线为Ⅰ
B . 水的电离程度:b>a>c
C . d点时,lg  =5.24
D . b点溶液中存在:c(Na+)=2[c(A-)+c(HA)]
=5.24
D . b点溶液中存在:c(Na+)=2[c(A-)+c(HA)]
 =5.24
D . b点溶液中存在:c(Na+)=2[c(A-)+c(HA)]
=5.24
D . b点溶液中存在:c(Na+)=2[c(A-)+c(HA)]
25℃时,向25mL0.1mol·L-1邻苯二甲酸(H2A)溶液中加入KOH固体,混合溶液的pH随-lgc(HA-)以及-lgc(A2-)的关系如图所示(忽略溶液体积变化和邻苯二甲酸的挥发)。下列有关叙述错误的是( )
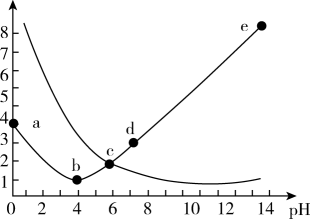
A . 邻苯二甲酸的Ka1约为1.0×10-3
B . b点有关微粒浓度大小关系为(HA-)>c(A2-)>c(H2A)
C . 从b点到e点,水电离产生的c(H+)先增大后减小
D . c点c(K+)>3c(A2-)
甘氨酸盐酸盐 的水溶液呈酸性,溶液中存在以下平衡:
的水溶液呈酸性,溶液中存在以下平衡:
 的水溶液呈酸性,溶液中存在以下平衡:
的水溶液呈酸性,溶液中存在以下平衡: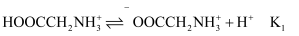
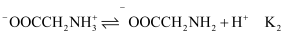
常温时,向10mL一定浓度的 的水溶液中滴入同浓度的NaOH溶液。混合溶液pH随加入NaOH溶液体积的变化如图所示。下列说法正确的是( )
的水溶液中滴入同浓度的NaOH溶液。混合溶液pH随加入NaOH溶液体积的变化如图所示。下列说法正确的是( )
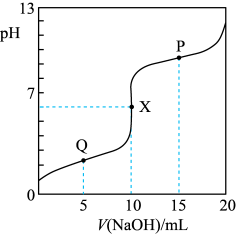
A . 水的电离程度:Q>X
B . X→P过程中: 逐渐增大
C . P点的溶液中:
逐渐增大
C . P点的溶液中: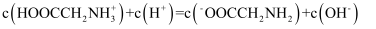 D . 当
D . 当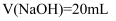 时,混合溶液中的溶质主要为
时,混合溶液中的溶质主要为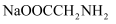 和NaCl
和NaCl
 逐渐增大
C . P点的溶液中:
逐渐增大
C . P点的溶液中: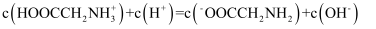 D . 当
D . 当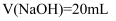 时,混合溶液中的溶质主要为
时,混合溶液中的溶质主要为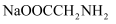 和NaCl
和NaCl
最近更新
- Kalong Community Centre provides enrichment activities at re
- 20 ℃时,把一定量的浓度为20%的某物质水溶液加热蒸发掉10 g水,再冷却至20 ℃,析出2 g晶体后,溶液浓度变为2
- 展开式中含项的系数为 A.60 B.80 C.120
- 跳伞运动员做低空跳伞表演,他在离地面224 m高处,由静止开始在竖直方向做自由落体运动.一段时间后,立即打开降落伞,以1
- 青少年在安静思考问题时,心脏推动血液流动的功率约为1.5W,则你在考试10分钟内,心脏做功约为_____J,用这些功可以
- 认真观察下面我国四个省级行政区轮廓图,回答1~3题。1.关于四省的简称对应正确的一组是( ) A. ①--滇、②-
- 有学者认为,中华人民共和国最初十年的成就相当卓著。下列选项能证明上述观点的有 ①奠定了国家基本政治制度的基础②在国际舞台
- 1.依次填入下列各句横线处的成语,最恰当的一组是( ) (1)当时,盐官、铁官并不是通过考试选拔而来,而是由经营盐铁
- 已知A、B、C、D、E是核电荷数依次增大的五种短周期元素,原子半径按D、E、B、C、A的顺序依次减小,B和E同主族,下列
- 氯化铁溶液与氢氧化铁胶体具有的共同性质是( ) A.分散质颗粒直径都在l~100nm之间 B.能透过半
- 如图,四棱锥中,底面是正方形,是正方形的中心,底面,是的中点。求证: (1)∥平面; (2)平面平面;
- 一些高校提倡大学生勤工俭学,其目的是为了 ( ) A.赚钱弥补学费的不足 B.培养自立能力大胆投身社会实践 C
- (本题满分15分) 某产品生产厂家根据以往的生产销售经验得到下面有关生产销售的统计规律:每生产产品(百台),其总成本为(
- The Spring Festival ________ in January or February.
- 张先生驾车从广州到肇庆旅游,汽车以90km/h的平均速度行驶0.5 h到达三水,休息0.5 h后,再以80 km/h的平
- 汉译英;按要求完成下面各句。每空一词。 1.她过去常常骑自行车去上学,现在步行了。 She
- 14.填入下面文段空白处的词语,最恰当的一组是 李白的诗歌__①__有高度的艺术技巧,__②__若论章法的严密、用典的巧
- 耳的结构中与身体平衡有关的是( ) A.听小骨 B.外耳道 C.耳蜗 D.半规
- 补写出下列名句名篇和文学常识的空缺部分。(6分) (1)秦人不暇自哀,而后人哀之;后人哀之而不鉴之,
- (10无锡36)某化学兴趣小组在甲、乙两个充满()2的密闭容器中各加入一定量的碳粉,在高温条件下使其充分反应,待反应结束



