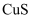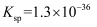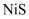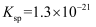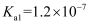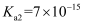水的电离 知识点题库
25℃时,某稀溶液中由水电离产生的c(H+)为1×10﹣10 , 下列说法正确的是( )
A . 该溶液的pH不可能是7
B . 该溶液不可能存在
C . 该溶液的pH一定是10
D . 该溶液的pH一定是4
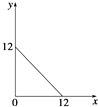
某温度(T℃)下的溶液中,c(H+)=10﹣x mol•L﹣1 , c(OH﹣)=10﹣y mol•L﹣1 , x与y的关系如图所示,请回答下列问题:
-
(1) 此温度下,水的离子积Kw为,则该温度T25(填“>”、“<”或“=”).
-
(2) 在此温度下,向Ba(OH)2溶液中逐滴加入pH=a的盐酸,测得混合溶液的部分pH如表所示.
实验序号
Ba(OH)2溶液的体积/mL
盐酸的体积/mL
溶液的pH
①
22.00
0.00
8
②
22.00
18.00
7
③
22.00
22.00
6
假设溶液混合前后的体积变化忽略不计,则a=,实验②中由水电离产生的c(OH﹣)=mol•L﹣1.
-
(3) 在此温度下,将0.1mol•L﹣1的NaHSO4溶液与0.1mol•L﹣1的Ba(OH)2溶液按下表中甲、乙、丙、丁不同方式混合:
甲
乙
丙
丁
0.1mol•L﹣1 Ba(OH)2溶液体积/mL
10
10
10
10
0.1mol•L﹣1 NaHSO4溶液体积/mL
5
10
15
20
①按丁方式混合后,所得溶液显(填“酸”、“碱”或“中”)性.
②写出按乙方式混合后,反应的离子方程式:.
③按甲方式混合后,所得溶液的pH为.
相同条件下,在①pH=2的CH3COOH溶液、②pH=2的HCl溶液、③pH=12的氨水、④pH=12的NaOH溶液中,下列说法不正确的是( )
A . 水电离的c(H+):①=②=③=④
B . 等体积的①、②溶液分别与足量铝粉反应,生成H2的量:②>①
C . 若将②、③溶液混合后,pH=7,则消耗溶液的体积:②>③
D . 将四种溶液分别稀释100倍后,溶液的pH:③>④>②>①
中学化学实验中,淡黄色的pH试纸常用于测定溶液的酸碱性.在25℃时,若溶液的pH=7,试纸不变色;若pH<7,试纸变红色;若pH>7,试纸变蓝色.
-
(1) 已知水中存在如下平衡:H2O+H2O⇌H3O++OH﹣△H>0,现欲使平衡向右移动,且所得溶液呈酸性,选择的方法是中(填字母).A . 向水中加入NaHSO4 B . 向水中加入Cu(NO3)2 C . 加热水至100℃[其中c(H+)=1×10﹣6 mol•L﹣1 D . 在水中加入(NH4)2SO4
-
(2) 现欲测定100℃沸水的pH及酸碱性,若用pH试纸测定,则试纸显 色,溶液呈 性(填“酸”、“碱”或“中”);若用pH计测定,则pH 7(填“>”、“<”或“=”),溶液呈 性(填“酸”、“碱”或“中”).
下列图示与对应的叙述相符的是( )
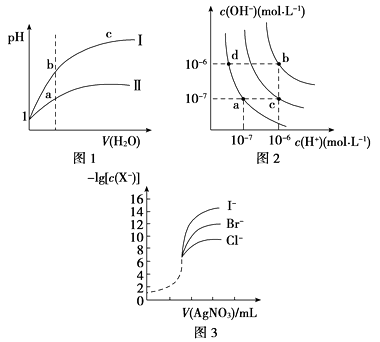
A . 图1表示同温度下,pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强
B . 图2中纯水仅升高温度,就可以从a点变到c点
C . 图2中在b点对应温度下,将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,溶液显中性
D . 用0.010 0 mol/L硝酸银标准溶液,滴定浓度均为0.100 0 mol/L Cl-、Br-及I-的混合溶液,由图3曲线,可确定首先沉淀的是Cl-
能促进水的电离且溶液呈酸性的是( )
A . Al2 (SO4)3
B . Na2CO3
C . HNO3
D . NaCl
-
(1) 氯化铁水溶液呈性,原因是(用离子方程式表示):;把FeCl3溶液蒸干,灼烧,最后得到的主要固体产物是;热的纯碱溶液去油污能力强,纯碱水解的离子方程式为(写第一步即可)。
-
(2) 普通泡沫灭火器是利用NaHCO3溶液跟Al2(SO4)3溶液混合,产生大量的气体和沉淀,气体将混合物压出灭火器,相关反应的离子方程式是。
-
(3) 已知:在相同条件下醋酸与氨水电离程度相同,现有浓度均为0.1mol/L的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸铵、⑦硫酸氢铵、⑧氨水。
①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号);
④、⑤、⑥、⑦、⑧五种溶液中NH4+浓度由大到小的顺序是(填序号)。
某温度下,向10mL0.1mol/LCuCl2溶液中滴加0.1mol/L的Na2S溶液,滴加过程中溶液中﹣lgc(Cu2+)与Na2S溶液体积(V)的关系如图所示,下列有关说法正确的是( )
(已知:Ksp(ZnS)=3×10﹣25mol2/L2)
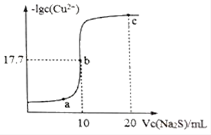
A . a、b、c三点中,水的电离程度最大的为b点
B . Na2S溶液中:c(S2-)+c(HS-)+c(H2S)=2c(Na+)
C . 该温度下Ksp(CuS)=10﹣35.4mol2/L2
D . 向100 mLZn2+、Cu2+浓度均为10-5mol/L的混合溶液中逐滴加入10-4mol/L的Na2S溶液,Zn2+先沉淀
下列溶液一定呈中性的是( )
A . pH=7的溶液
B . c(H+)=c(OH-)=10-6mol/L溶液
C . 使石蕊试液呈紫色的溶液
D . 等体积等浓度的酸与碱反应后的溶液
某温度下,向10 mL 0.1 mol/L CuCl2溶液中滴加0.1 mol/L的Na2S溶液,滴加过程中溶液中-lgc(Cu2+)与Na2S溶液体积(V)的关系如图所示,下列有关说法不正确的是( )
(已知:Ksp(ZnS)=3×10-25mol2/L2)
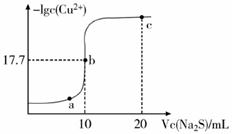
A . a、b、c三点中,水的电离程度最大的为b点
B . Na2S溶液中:2c(S2-)+2c(HS-)+2c(H2S)=c(Na+)
C . 该温度下Ksp(CuS)=10-35.4 mol2/L2
D . 向100 mL Zn2+、Cu2+浓度均为10-5 mol/L的混合溶液中逐滴加入10-4 mol/L的Na2S溶液,Cu2+先沉淀
25℃时纯水的 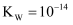 ,100℃时,
,100℃时, 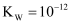 ,这说明( )
,这说明( )
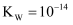 ,100℃时,
,100℃时, 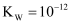 ,这说明( )
,这说明( )
A . 100℃水的电离程度较小
B . 前者  较后者的大
C . 水的电离是吸热的
D . 100℃时水的电离程度是室温时的100倍
较后者的大
C . 水的电离是吸热的
D . 100℃时水的电离程度是室温时的100倍
 较后者的大
C . 水的电离是吸热的
D . 100℃时水的电离程度是室温时的100倍
较后者的大
C . 水的电离是吸热的
D . 100℃时水的电离程度是室温时的100倍
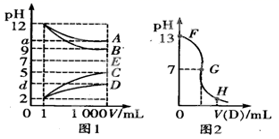
物质A—E都是由下表中的离子组成或生成的,常温下各物质从1mL稀释到1000mL,pH的变化如图l所示,其中A与D反应得到E。请回答:
|
阳离子 |
NH |
| 阴离子 | OH-、CH3COO-、Cl- |
-
(1) 根据图1中各物质的pH变化关系,写出下列物质的化学式:B:。
-
(2) 图l中a>9的理由是。
-
(3) 另取浓度为C1的B溶液25ml,向其中逐滴滴加0.2mol/L的D溶液,滴定过程中溶液pH的变化曲线如图2所示。
①C1为。
②G点溶液呈中性,则加入D溶液的体积V(填“>”、“<’’或“=”)12.5mL。
③常温下B、C溶液的pH分别是a、b且a+b=13,则将B、C混合恰好完全反应时所消耗B、C溶液的体积比VB:VC=。
已知温度T时水的离子积常数为KW , 该温度下,将浓度为a mol·L-1的一元酸HA与b mol·L-1的一元碱BOH等体积混合,可判定该溶液呈中性的依据是( )
A . a=b
B . 混合溶液的pH=7
C . 混合溶液中,c(H+)=  mol.L-1
D . 混合溶液中c(H+)+c(B+)=c(OH-)+C(A-)
mol.L-1
D . 混合溶液中c(H+)+c(B+)=c(OH-)+C(A-)
 mol.L-1
D . 混合溶液中c(H+)+c(B+)=c(OH-)+C(A-)
mol.L-1
D . 混合溶液中c(H+)+c(B+)=c(OH-)+C(A-)
一定温度下,水溶液中H+和OH-的浓度变化曲线如图所示,下列说法正确的是( )
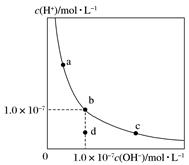
A . 升高温度,可能引起由c向b的变化
B . 该温度下,水的离子积常数为1.0×10-13
C . 该温度下,加入FeCl3可能引起由b向a的变化
D . 该温度下,稀释溶液可能引起由c向d的变化
在25 ℃时,向纯水中加入少量的KHSO4固体,则( )
A . 溶液c(H+)减小
B . 水的离子积常数Kw减小
C . 水的电离平衡向正方向移动
D . 溶液的c(OH-)减小
下列说法错误的是( )
A . 含  与
与 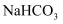 共1mol的溶液中,
共1mol的溶液中,  B . 25℃时,
B . 25℃时,  溶液的
溶液的 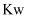 大于
大于  溶液的
溶液的 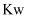 C .
C .  受热分解为
受热分解为 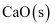 和
和  ,
, 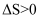 D . 误将钡盐
D . 误将钡盐 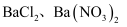 当作食盐食用后,常用0.5%的
当作食盐食用后,常用0.5%的  溶液解毒
溶液解毒
 与
与 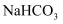 共1mol的溶液中,
共1mol的溶液中,  B . 25℃时,
B . 25℃时,  溶液的
溶液的 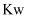 大于
大于  溶液的
溶液的 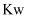 C .
C .  受热分解为
受热分解为 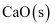 和
和  ,
, 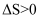 D . 误将钡盐
D . 误将钡盐 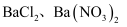 当作食盐食用后,常用0.5%的
当作食盐食用后,常用0.5%的  溶液解毒
溶液解毒
已知25℃下水的离子积Kw=1×10-14 , 此温度下,下列说法错误的是( )
A . 纯水加入NaOH固体,水的电离程度减小
B . 纯水加入FeCl3固体,pH升高
C . 0.005 mol·L-1的硫酸溶液,pH=2
D . 0.01 mol·L-1的氢氧化钠溶液,pH=12
25℃时,向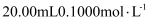 的两种酸HX、HY中分别滴加
的两种酸HX、HY中分别滴加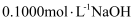 溶液,测得两溶液pH随NaOH溶液体积变化的曲线如图所示。下列说法不正确的是( )
溶液,测得两溶液pH随NaOH溶液体积变化的曲线如图所示。下列说法不正确的是( )
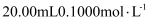 的两种酸HX、HY中分别滴加
的两种酸HX、HY中分别滴加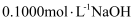 溶液,测得两溶液pH随NaOH溶液体积变化的曲线如图所示。下列说法不正确的是( )
溶液,测得两溶液pH随NaOH溶液体积变化的曲线如图所示。下列说法不正确的是( )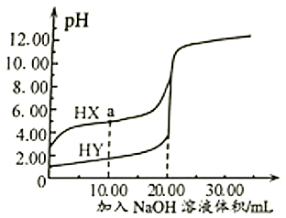
A . 酸性: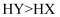 B . a点溶液中微粒浓度:
B . a点溶液中微粒浓度: C . 滴加NaOH溶液至
C . 滴加NaOH溶液至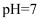 时,两溶液中
时,两溶液中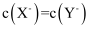 D . 从开始滴加至
D . 从开始滴加至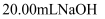 溶液时,两溶液中
溶液时,两溶液中 的电离程度均逐渐增大
的电离程度均逐渐增大
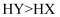 B . a点溶液中微粒浓度:
B . a点溶液中微粒浓度: C . 滴加NaOH溶液至
C . 滴加NaOH溶液至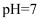 时,两溶液中
时,两溶液中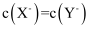 D . 从开始滴加至
D . 从开始滴加至 溶液时,两溶液中
溶液时,两溶液中 的电离程度均逐渐增大
的电离程度均逐渐增大
废水中的重金属离子通常用沉淀法除去。已知常温下各物质的溶度积或电离平衡常数如下表所示,请回答下列问题:
|
|
|
|
|
|
-
(1)
 溶液中加入一定量的
溶液中加入一定量的 反应后溶液呈中性,该溶液中
反应后溶液呈中性,该溶液中 (用
(用 ,
, 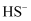 、
、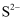 等物质的浓度来表示)
等物质的浓度来表示)
-
(2)
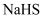 溶液中
溶液中
 (填“>”、“<”、“=”),若向此溶液中加入
(填“>”、“<”、“=”),若向此溶液中加入 溶液,恰好完全反应,所得溶液的
溶液,恰好完全反应,所得溶液的 7(填“>”、“<”、“=”)。
7(填“>”、“<”、“=”)。
-
(3) 向浓度均为0.1
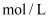 的
的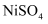 和
和 的混合溶液中加
的混合溶液中加 溶液,当加入
溶液,当加入 溶液至出现两种沉淀时,则溶液中
溶液至出现两种沉淀时,则溶液中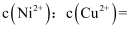 。
。
-
(4) 向
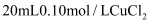 溶液中滴加
溶液中滴加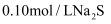 溶液,滴加过程中
溶液,滴加过程中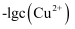 与
与 溶液体积(V)的关系如图所示。
溶液体积(V)的关系如图所示。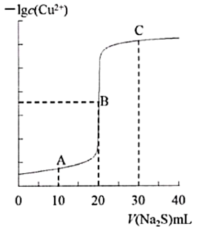
A、B、C三点溶液中,水的电离程度最小的是点;溶液碱性最强的是点;
 和
和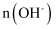 的乘积最小的是点。
的乘积最小的是点。
下列说法正确的是( )
A . 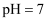 的溶液中
的溶液中 、
、 、
、 、
、 能大量共存
B . 相同温度下,
能大量共存
B . 相同温度下,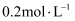 醋酸溶液与
醋酸溶液与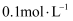 醋酸溶液中
醋酸溶液中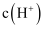 之比小于
之比小于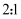 C . 等物质的量浓度①
C . 等物质的量浓度① 、②NH4Al(SO4)2溶液中
、②NH4Al(SO4)2溶液中 浓度的大小顺序为①>②
D . 常温下,
浓度的大小顺序为①>②
D . 常温下, 均为
均为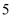 的氯化铵溶液和醋酸溶液中水的电离程度相同
的氯化铵溶液和醋酸溶液中水的电离程度相同
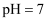 的溶液中
的溶液中 、
、 、
、 、
、 能大量共存
B . 相同温度下,
能大量共存
B . 相同温度下,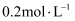 醋酸溶液与
醋酸溶液与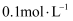 醋酸溶液中
醋酸溶液中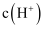 之比小于
之比小于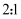 C . 等物质的量浓度①
C . 等物质的量浓度① 、②NH4Al(SO4)2溶液中
、②NH4Al(SO4)2溶液中 浓度的大小顺序为①>②
D . 常温下,
浓度的大小顺序为①>②
D . 常温下, 均为
均为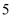 的氯化铵溶液和醋酸溶液中水的电离程度相同
的氯化铵溶液和醋酸溶液中水的电离程度相同
最近更新
- 补写下列名旬名篇中的空缺部分口 (1)子日:“ ,思而不学则殆。”
- 作为中学生,我们不仅要学习文化知识,而且要关注社会问题。(1)进来,瘦肉精、染色馒头、三聚氰胺等事件频频曝光,食品安全再
- 阅读《背影》选段 我说道:“爸爸,你走吧。”他往车外看了看说:“我买几个橘子去。你就在此地,不要走动。”我看那边月台的栅
- 下列变化属于化学变化的是A . 干冰升华B . 滤纸折叠C . 石蜡熔化D . 红磷燃烧
- 下列各句中,加点的成语使用不恰当的一句是 A.最令我敬佩的是钱学森老人的人品,他胸无城府,朴实无华,心灵如蓝天一般透明,
- 下图示意为某专题研究建立的地理信息系统(GIS)图层。该专题研究可能是() A.耕地分类和评价 B.
- 下图中,能正确表示基态硅原子的是( )A B C
- x2﹣2x﹣2=0;
- 阅读下面的文言文,完成下题。 寇准字平仲,华州下邽人也。准少英迈,通《春秋》三传。年十九,举进士。太宗取人,多临轩顾问,
- 有一实心铜块的密度是8.9×103kg/m3,它的物理意义是__________________________;若将它
- Trip 1 One Week in The Mountains Bring your strong shoes an
- 如图,四个半径为1的小圆都过大圆圆心且与大圆相内切,阴影部分的面积为【 】A. B.-4
- Many students are now facing with problems likedeciding whet
- “文革”中二月抗争、全面整顿、四五运动的出现说明的共同问题是 ( )A.老一辈无产阶级革命家一直在同“
- 常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g)Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×10−5
- This T-shirt looks ______and sells ______. A. well…well
- The young man is handsome and ___________(精力充沛的).
- “蚁穴溃堤”这一成语主要揭示了生物对环境造成的影响。( )
- 某种饮料每箱装有6听,其中有2听不合格,问质检人员从中随机抽出2听,检测出不合格产品的概率是多大。
- 如下图,镐京与曲阜的关系是A.王都与封国都邑 B.均为封国都邑 C.王都与郡府
 、H+、Na+
、H+、Na+