比较弱酸的相对强弱的实验 知识点题库
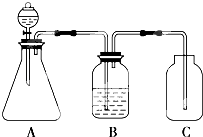
请据此回答:
-
(1) 锥形瓶中装某可溶性正盐溶液,分液漏斗中所盛试剂应为.
-
(2) 装置B所盛的试剂是,其作用是.
-
(3) 装置C所盛的试剂是,C中反应的离子方程式.
-
(4) 由引得出的结论是:酸性>>.
A | B | C | D | |
实验方案 |
|
|
|
|
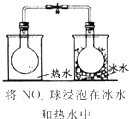
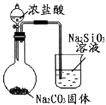
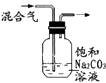
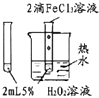
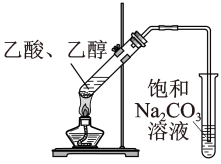
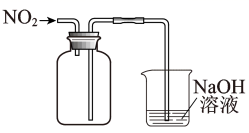
实验目的 | 探究温度对平衡的影响 2NO2→N2O4 | 比较HCl、H2CO2和 H2SiO3的酸性强弱 | 除去CO2气体中混有的SO2 | 验证FeCl3对H2O2分解反应有催化作用 |
 B . 加稀硫酸共热后,再加入足量NaOH溶液
C . 加热该物质溶液,再通入足量的
B . 加稀硫酸共热后,再加入足量NaOH溶液
C . 加热该物质溶液,再通入足量的  D . 与稀硫酸共热后,加入足量的
D . 与稀硫酸共热后,加入足量的 
-
(1) 硫酸铵是某地PM2.5雾霾的主要成分,收集一定量的雾霾固体进行验证。取一定量的雾霾固体于试管中,加入适量的水溶解,把溶液分成两份盛于试管中:
操作步骤
实验现象
结论
①向其中一份
有白色沉淀生成
证明雾霾固体中含有SO42-
②向另一份中加适量NaOH浓溶液并加热,用镊子夹持湿润的红色石蕊试纸靠近试管口
③试管中有气泡产生,靠近试管口的红色石蕊试纸
证明雾霾固体中含有NH4+。综合上面实验,初步说明雾霾固体颗粒中含有(NH4)2SO4
-
(2) 用如图所示简易装置测定空气中SO2的含量。
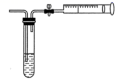
①测定原理:SO2通入碘的淀粉溶液中,溶液由蓝色变为无色,反应的化学方程式为。
②测定方法:在某监测点,量取5.0mL5.0×10-4mol/L的碘溶液,注入图中的试管中,加几滴淀粉指示剂,此时溶液呈蓝色,按图中装置连接好仪器,利用止水夹控制,进行抽气,取下注射器排气,重复操作直到溶液的蓝色全部褪尽为止,共抽取空气8.0L,则测得该监测点空气中SO2的含量为mg/L。
-
(3) 探究H2SO3的部分性质。选用下面的装置和药品探究H2SO3与HClO的酸性强弱。
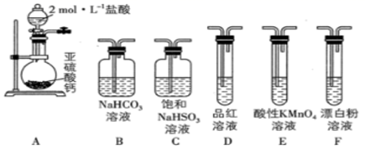
①甲同学认为按照A→C→F→尾气处理的顺序连接装置,可以证明H2SO3与HClO的酸性强弱,乙同学认为该方案不合理,其理由是。
②丙同学采用间接法证明,实验方案为按照A→C→→→→(填字母)→尾气处理顺序连接装置,证明H2SO3的酸性强于HClO的实验现象是。
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀产生 | 该溶液中一定含有SO42- |
| B | 向某溶液中加入盐酸,将生成的气体通入品红溶液中,品红溶液褪色 | 该溶液一定含有 SO32- |
| C | 将某气体通入品红溶液中,品红溶液褪色 | 说明酸性:H2SO3>H2CO3 |
| D | 某气体先通入足量的酸性 KMnO4 溶液,再通入澄清石灰水中有浑浊 | 该气体一定是 CO2 |
|
实验目的 |
实验操作 |
|
|
A |
验证酸性:碳酸>苯酚 |
向碳酸钠溶液中加入浓盐酸,将产生的气体通入苯酚钠溶液中,溶液变浑浊。 |
|
B |
提纯含有乙酸杂质的乙酸乙酯 |
向乙酸乙酯中加入氢氧化钠溶液再蒸馏 |
|
C |
比较水和乙醇中羟基氢的活泼性强弱 |
用金属钠分别与水和乙醇反应 |
|
D |
检验葡萄糖中含有醛基 |
向3mL5%NaOH溶液中加入几滴2%CuSO4溶液,振荡后加入0.5mL葡萄糖溶液,加热 |
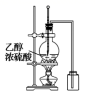 B . 实验室制硝基苯
B . 实验室制硝基苯 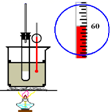 C . 比较碳酸与苯酚的酸性强弱
C . 比较碳酸与苯酚的酸性强弱  D . 实验室制乙酸乙酯
D . 实验室制乙酸乙酯 
|
选项 |
实验操作 |
现象 |
结论 |
|
A |
某有机物与溴水混合 |
溶液褪色 |
有机物中一定含碳碳双键 |
|
B |
向乙醇中加入浓硫酸并加热,产生的气体通入酸性KMnO4溶液 |
溶液褪色 |
产生的气体为乙烯 |
|
C |
向乙醛中加2mL 10%CuSO4溶液,再加3滴10%NaOH溶液,加热 |
无红色沉淀 |
乙醛已变质 |
|
D |
向苯酚乳浊液中加入Na2CO3溶液,振荡、静置 |
溶液变澄清 |
苯酚的酸性比 |
-
(1) I.探究SO2性质
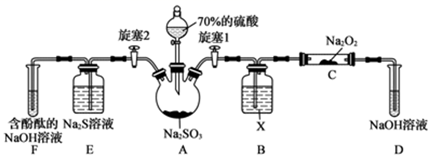
装置B中试剂X是
-
(2) 关闭旋塞1后,打开旋塞2,装置E中的Na2S溶液用于验证SO2的性,化学方程式
-
(3) II.探究H2SO3的酸性强于HClO(可能所需要的装置和试剂如图所示)
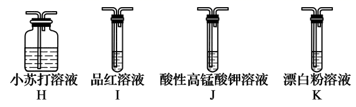
所需装置的连接顺序为:纯净的SO2→→→→, (填装置标号),装置K中反应的离子方程式为。
-
(4) Ⅲ.葡萄酒常用SO2作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:

(已知:滴定时化学方程式为:SO2+I2+2H2O=H2SO4+2HI)
按上述方案实验,消耗标准I2溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为g·L-1。
-
(5) 在上述实验过程中,若有部分HI被空气氧化,则测得结果(填“偏高”“偏低”或“不变”)。
| 实验 | 结论 | |
| A | 将乙烯通入溴的四氯化碳溶液,溶液最终变为无色透明 | 生成的1,2—二溴乙烷无色、可溶于四氯化碳 |
| B | 乙醇和水都可与金属钠反应产生可燃性气体 | 乙醇分子中的氢与水分子中的氢具有相同的活性 |
| C | 用乙酸浸泡水壶中的水垢,可将其清除 | 乙酸的酸性弱于碳酸的酸性 |
| D | 甲烷与氯气在光照下反应后的混合气体能使湿润的石蕊试纸变红 | 生成的氯甲烷具有酸性 |
| 选项 | 实验操作 | 实验现象 | 解释与结论 |
| A | 向甲苯中滴入适量溴水,振荡、静置 | 溶液下层呈橙红色,上层几乎无色 | 甲苯萃取溴单质 |
| B | 1-溴丙烷与氢氧化钠溶液共热后,滴加硝酸银溶液 | 未出现淡黄色沉淀 | 1-溴丙烷未水解 |
| C | 向苯酚钠的水溶液中通入二氧化碳 | 溶液变浑浊 | 苯酚的酸性比碳酸弱,生成了溶解度较小的苯酚 |
| D | 向蔗糖溶液中加入稀硫酸水浴加热后,再加入新制氢氧化铜悬浊液,加热 | 产生砖红色沉淀 | 蔗糖水解生成葡萄糖,葡萄糖分子中含有醛基 |
| 验证溴乙烷消去反应的气体产物为乙烯 | 实验室制乙酸乙酯 | 收集NO2气体 | 酸性:碳酸>苯酚 |
| | | | |
| A | B | C | D |
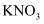 溶液和
溶液和 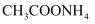 溶液pH均为7,两溶液中水的电离程度相同
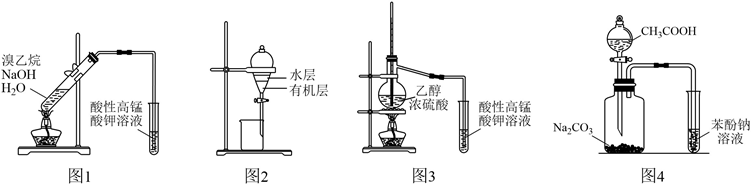
B . NaHA溶液呈酸性,说明
溶液pH均为7,两溶液中水的电离程度相同
B . NaHA溶液呈酸性,说明  是强酸
C . 氨水的pH不一定比NaOH溶液的pH小
D . pH均为3的盐酸和醋酸,分别与足量金属Mg反应,醋酸中产生的气体多
是强酸
C . 氨水的pH不一定比NaOH溶液的pH小
D . pH均为3的盐酸和醋酸,分别与足量金属Mg反应,醋酸中产生的气体多
| 选项 | 操作 | 现象 | 结论 |
| A | 向FeCl3和KSCN混合溶液中,加入少量KCl的固体 | 溶液颜色变浅 | FeCl3+2KSCN |
| B | 浓度均为0.10mol/L的Na2CO3和Na2S的混合溶液中滴入少量AgNO3溶液 | 产生黑色沉淀 | Ksp(Ag2S)>Ksp(Ag2CO3) |
| C | 向装有X溶液的试管中滴入NaOH溶液,将干燥的红色石蒸试纸置于试管口 | 无明显现象 | X溶液中无NH |
| D | 常温下,向浓度、体积都相同的Na2CO3和NaHCO3溶液中各滴加1滴酚酞 | 变红,前者红色更深 | 结合质子的能力:CO |
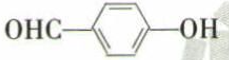 )和邻羟基苯甲醛(
)和邻羟基苯甲醛(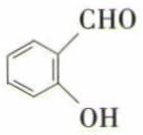 )的沸点
C . I2在水中的溶解度和I2在CCl4溶液中的溶解度
D . H2SO3和H2SO4的酸性
)的沸点
C . I2在水中的溶解度和I2在CCl4溶液中的溶解度
D . H2SO3和H2SO4的酸性
选项 | 实验操作 | 现象 | 结论 |
A | 向 | 紫红色退去 |
|
B | 加热某盐与 | 红色石蕊试纸变蓝 | 该盐为铵盐 |
C | 将用硫酸酸化的 | 溶液变黄色 | 氧化性: |
D | 向一定浓度的 | 产生黑色沉淀 |
|
- 东晋王羲之被后人称为“书圣”,他的书法作品《兰亭序》被称为“天下第一( )”。 A.行书
- 列宁曾说:“公社被镇压了,但鲍狄埃的《国际歌》却把它的思想传遍了全世界。”“公社”是思想是指( )A.无产阶级革命思
- 中国商人历来推崇“薄利多销”,而犹太商人则认为“一种商品既然利薄,何不弃之。选择利厚的产品去生产和销售不是更好吗?”以上
- 下列各句中,加点的熟语使用恰当的一项是() A.在填报志愿时,凭感觉、靠想象、顾名思义等,都是客观存在的。一旦如此选择的
- 柏拉图和亚里士多德同声赞誉梭伦是“优良的改革家”,是因为梭伦 A.推翻王权,以贵族制取而代之 B.实行改
- With April 18’s railway speedup, highway and air transport
- – I can’t get my car ___on cold winter mornings. ---Have yo
- 有学者指出:如果说文艺复兴为人本主义者们“清理了场地”,那么启蒙运动则是“大兴土木”。这里的“大兴土木”是指 A
- The police an organization which protects the public
- 依次填入句中横线上的词语,最恰当的一组是 ①老舍先生在作品中偶尔也说一些灰心的话,混杂在诙谐的语句中。别人笑的时候,他却
- 如图,点D在以AC为直径的⊙O上,如果∠BDC=20°,那么∠ACB=.
- 下列能正确标注图中天体系统名称的是A.①——地月系 B.②——太阳系 C.③——总星系 D.④—
- 已知在定义域上是减函数,且,则的取值范围是 .
- 蝗虫与家蚕个体发育比较,蝗虫生活史中不具有的时期是( ) A.受精卵 B.幼虫
- 我国法定的公司形式有两种,即有限责任公司和股份有限公司,它们的共同点在于( ) ①都是依法成立的企业法人
- 如图12-3-15所示,有一磁感应强度为B=0.40T的匀强磁场,其磁感线垂直地穿过半径的金属环,OA是一根金属棒,它贴
- 下列人类常见疾病中,能依据孟德尔遗传规律预测后代患病几率的是 A.地方性甲状腺肿 B.原发性高血压 C.艾滋
- 把下面文字中画线的部分改写成整句。(4分) 小屋的出现,点破了山的寂寞,增加了风景的内容。山上有了小屋,好比一望无际
- --Mum, I don’t think I am qualified enough to do this. --Hon
- Cindy ,Jerry and Mary are giving their opinions about a good
 强
强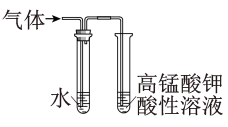
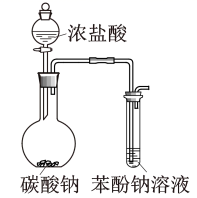
 Fe(SCN)3+3KCl平衡向逆反应方向移动
Fe(SCN)3+3KCl平衡向逆反应方向移动
 >HCO
>HCO 
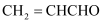 中滴加
中滴加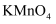 酸性溶液
酸性溶液 的混合溶液,用湿润的红色石蕊试纸检验产生的气体
的混合溶液,用湿润的红色石蕊试纸检验产生的气体 溶液滴入
溶液滴入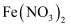 溶液中
溶液中 (酸性条件)
(酸性条件) 溶液中通入适量
溶液中通入适量 气体
气体 强
强


