比较弱酸的相对强弱的实验 知识点题库
物质 | H2CO3 | HClO | HAlO2 |
电离常数 (25℃) | Ka1=4.4×10- | Ka=3×10-8 | Ka=6.3×10-13 |
Ka2=4.7×10-11 |
| 编号 | 实验内容 | 实验目的 |
| A | 等体积pH=2的HX和HY两种酸分别与足量的铁反应,排水法收集气体,HX放出的氢气多且反应速率快 | 证明HX酸性比HY强 |
| B | 室温下,用pH试纸分别测定浓度为0.1 mol·L-1NaClO溶液和0.1 mol·L-1NaF溶液的pH | 比较HClO和HF溶液的酸性 |
| C | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| D | 向MgCl2溶液加入NaOH溶液 | 除去MgCl2溶液中的Fe3+ |
| 选项 | 操作 | 现象 | 结论 |
| A | 将新制氯水滴到淀粉KI试纸上 | 试纸变蓝色 | 氧化性:I2>Cl2 |
| B | 将过量的CO2通入CaCl2溶液中 | 产生白色沉淀 | 酸性:HCl>H2CO3 |
| C | FeSO4溶液中滴入酸性高锰酸钾溶液 | 紫色褪色 | Fe2+有还原性 |
| D | SO2通入溴水中 | 溶液褪色 | SO2有漂白性 |
| A | B | C | D | |
| 操作 | | | | |
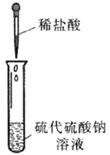
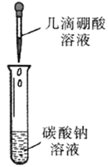
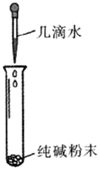
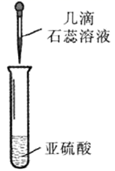
| 现象 | 溶液变浑浊 | 无气泡生成 | 固体结块,试管底部温度升高 | 溶液先变红,后褪色 |
| 解释或结论 | 稀盐酸将硫代硫酸钠还原为硫单质 | 硼酸的酸性弱于碳酸 | 生成纯碱晶体的反应是放热反应 | 亚硫酸既有酸性又有漂白性 |
| 选项 | 实验操作和现象 | 结论 |
| A | 向某溶液中先滴加稀硝酸,再滴加Ba(NO3)2溶液,出现白色沉淀 | 该溶液中一定含有 |
| B | 用pH试纸测定浓度均为0.1mol·L-1HCOONa溶液与CH3COONa溶液的pH,CH3COONa溶液的pH较大 | CH3COOH电离出H+的能力比HCOOH的强 |
| C | 向0.1mol·L-1H2O2溶液中滴加0.1mol·L-1KMnO4溶液,溶液褪色并放出能使带火星木条复燃的气体 | H2O2具有氧化性 |
| D | 向2.0mL浓度均为0.1mol·L-1的KCl、KI混合溶液中滴加1~2滴0.01mol·L-1AgNO3溶液,振荡,出现黄色沉淀 | Ksp(AgI)<Ksp(AgCl) |
- 阅读下面文字,完成后面的问题。 世界上许多国家过母亲节,但母亲节的日期不尽相同:美国、意大利等国都在5月的第二个星期日,
- 城市的发展包括①人口向城市集中 ②工业向城市集中 ③城市内涵的提升 ④城市产业结构的优化A.①②③ B
- 如果两个相似三角形的相似比为2:3, 那么这两个相似三角形的面积比为__
- 有关英国责任制内阁的表述,正确的是( ) ①由多数党领袖组阁 ②实际上对议会负责 ③首相有权
- 某大学8名学生准备拼车去旅游,其中大一、大二、大三、大四每个年级各两名,分乘甲、乙两辆汽车,每车限坐4名同学(乘同一辆车
- 3(a﹣3)﹣4(2a﹣1)
- 下表是四地一年中昼长最大差值(R)和正午太阳高度最大差值(H)资料,据此回答下列各题。① ② ③ ④ R 2小时26分
- 下列河流中,自南向北注入北冰洋的是( ) A.塔里木河 B.额尔齐斯河 C.雅鲁藏布江
- 铁和钛是生活、生产中的重要金属,下列说法不正确的是 ( ) A.铁在潮湿的空气
- 如图,在菱形ABCD中,对角线AC=6,BD=8,若过点A作AE⊥BC,垂足为E,则AE的长为
- 一个不等式组中的两个不等式的解集如图所示,则这个不等式组的解集为() A.﹣1<x≤2 B. ﹣1≤x<2
- 2005年4月28—30日,华北地区经历了一次沙尘天气,造成许多地方空气污染指数(API)增高,主要污染物是可吸入颗粒物
- 新鲜水果、蔬菜、乳制品中富含的维生素C具有明显的抗衰老作用,但易被空气氧化。某课外小组利用碘滴定法测某橙汁中维生素C的含
- ......
- 已知,如图,边长为2cm的正方形ABCD的顶点B在OP上,C在OQ上且,求出点A到OP的距离.
- 改革开放三十年来,国民生产总值由1978年的3645亿元增长到2007年的246619亿元,经济增长速度保持在9%以上,
- —It’s a top secret.—Yes, I see. I will keep the secret _____
- 嫦娥一号”探月成功是我国航天事业的又一伟大成就,卫星正常工作的能源有的来自于太阳能,为了顺利完成能量转化需一种良好的半
- 语意明确,没有语病的一句是: A.据近日公布的《社会蓝皮书》指出:2002年百姓最想荷包满。 B.2月21日结束会
- —Thelittle girl ________ her seat to an old man on the bus.