比较弱酸的相对强弱的实验 知识点题库
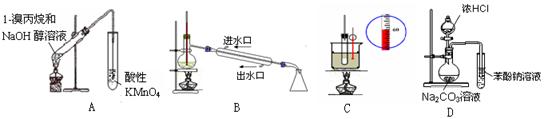
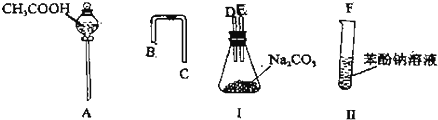
-
(1) 利用如图所示的仪器可以组装实验装置,则仪器的连接顺序为:接接接(填字母)
-
(2) 写出装置Ⅰ和Ⅱ中的实验现象:
Ⅰ中
Ⅱ中.
-
(3) 写出装置Ⅰ和装置Ⅱ中发生反应的方程式
Ⅰ中
Ⅱ中.
-
(4) 由强到弱排序三者的酸性顺序>>(填结构简式)
甲:①称取一定质量的HA配制0.1mol•L﹣1的溶液100mL;
②用pH试纸测出该溶液的pH,即可证明HA是弱电解质.
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各100mL;
②分别取这两种溶液各10mL,加水稀释为100mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质.
-
(1) 在两个方案的第①步中,都要用到定量仪器是.
-
(2) 甲方案中,说明HA是弱电解质的理由是测得溶液的pH1(选填“>”、“<”、“=”).乙方案中,说明HA是弱电解质的现象是.
a.装HCl溶液的试管中放出H2的速率快;
b.装HA溶液的试管中放出H2的速率快;
c.两个试管中产生气体速率一样快.
(H2SiO3是一种难溶于水的弱酸,呈白色)的酸性强弱顺序:CH3COOH>H2CO3>H2SiO3 . 该校学生设计了如图的实验装置(夹持仪器已略去):
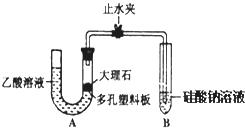
-
(1) 某学生检查装置A的气密性时,先关闭止水夹,从左管向U型管内加水,至左管液面高于右管液面,静置一段时间后,若U型管两侧液面差不发生变化,则气密性良好.你认为该学生的操作正确与否?(填“正确”或“错误”),大理石与乙酸溶液反应的离子方程式为:
-
(2) 试描述能证明三种酸的酸性强弱的现象
-
(3) 有学生认为上述现象不足以证明H2CO3的酸性比H2SiO3强,理由是乙酸有挥发性,挥发出的CH3COOH也可以和Na2SiO3溶液反应,生成H2SiO3 . 改进该装置的方法是在装置A和B之间连一个盛有饱和溶液(选填Na2CO3、NaHCO3或Na2SiO3)的洗气瓶.
| 选项 | 实验目的 | 实验过程 |
| A. | 比较碳酸和醋酸的酸性 | 常温下,用pH计测量等浓度醋酸钠和碳酸氢钠溶液的pH |
| B. | 探究浓度对反应速率的影响 | 向盛有4mL浓度分别为0.01mol/L和0.05mol/LKMnO4酸性溶液的两支试管中,同时加入4mL0.1mol/L的草酸溶液,记录褪色所需时间 |
| C. | 证明Ksp[Fe(OH)3]<Ksp[Al (OH)3] | 向1mL0.1mol·L-1NaOH溶液中滴加2滴0.1mol·L-1AlCl3溶液,充分反应后再滴加2滴0.1mol·L-1FeCl3溶液,观察沉淀颜色变化 |
| D. | 探究温度对反应速率的影响 | 将2支盛有5mL同浓度NaHSO3溶液的试管和两支盛有2mL5%H2O2溶液的试管分成两组,一组放入冷水中,另一组放入热水中,经过一段时间分别混合并搅拌,观察实验现象 |
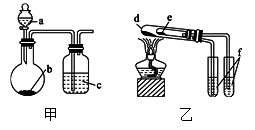
| 选项 | 实验试剂 | 实验结论 | ||
| A | a.稀硫酸 | b.碳酸氢钠 | c.硅酸钠溶液 | 酸性:硫酸>碳酸>硅酸 |
| B | a.浓盐酸 | b.二氧化锰 | c.溴化钠溶液 | 氧化性: MnO2>Cl2>Br2 |
| C | d.小苏打 | e.苏打 | f.石灰水 | 热稳定性:苏打>小苏打 |
| D | d.氯化钠 | e.氯化铵 | f.硝酸银溶液 | 沸点:氯化钠>氯化铵 |
甲:①称取一定量的冰醋酸准确配制0.1mol/L的醋酸溶液100mL
②用pH试纸测出该溶液的pH,即可证明醋酸是弱酸。
乙:分别配制盐酸和醋酸溶液,在相同温度下比较两溶液的导电性。
回答下列问题:
-
(1) 简要说明pH试纸的使用方法:。
-
(2) 甲方案中,说明醋酸是弱酸的理由是测得醋酸溶液的pH1(选填“>”“<”“=”,下同);乙方案中,若达目的,配制的两溶液应满足的条件是必须相等,证明醋酸是弱酸的现象是
|
化学式 |
CH3COOH |
H2CO3 |
HClO |
|
电离平衡常数 |
1.7×10-5 |
| 4.7×10-8 |
请回答下列问题。
-
(1) CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为。
-
(2) 同浓度的CH3COO-、
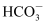 、
、  、ClO-结合H+的能力由强到弱的顺序为
、ClO-结合H+的能力由强到弱的顺序为
-
(3) 将少量CO2气体通入NaClO溶液中,写出反应的离子方程式:。
-
(4) 10mLpH=2的醋酸与一元酸HX分别加水稀释至1000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数(填“大于”“等于”或“小于”)醋酸的电离平衡常数,理由是。

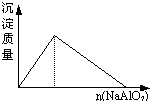 盐酸溶液中逐滴加入NaAlO2
B .
盐酸溶液中逐滴加入NaAlO2
B . 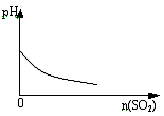 SO2气体逐渐通入溴水中
C .
SO2气体逐渐通入溴水中
C . 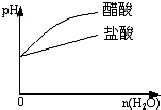 pH=1的醋酸与盐酸溶液分别加水稀释
D .
pH=1的醋酸与盐酸溶液分别加水稀释
D . 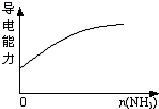 氨气逐渐通入醋酸中
氨气逐渐通入醋酸中
-
(1) 当三种酸物质的量浓度相同时,
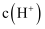 由大到小的顺序是。
由大到小的顺序是。
-
(2) 同体积、同物质的量浓度的三种酸,中和
 的能力由大到小的顺序是。
的能力由大到小的顺序是。
-
(3) 当三者pH相同、体积相同时,分别放入足量的
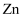 充分反应,开始产生H2的速率大小顺序是;反应结束时(相同状况下)产生气体的体积由大到小的顺序是。
充分反应,开始产生H2的速率大小顺序是;反应结束时(相同状况下)产生气体的体积由大到小的顺序是。
| 选项 | 实验操作 | 实验目的 |
| A | 向电石中滴加饱和食盐水,将产生的气体通入溴水 | 检验产生的乙炔气体 |
| B | 乙醇与浓硫酸混合加热至170℃,将产生的气体先通入NaOH溶液,再通入Br2的CCl4溶液 | 检验产生的乙烯气体 |
| C | 向纯碱中滴加足量浓盐酸,将产生的气体通入苯酚钠溶液 | 验证酸性:盐酸>碳酸>苯酚 |
| D | 向盛有2mL鸡蛋清溶液的试管中滴加数滴浓硝酸,微热 | 检验蛋白质具有碱性 |
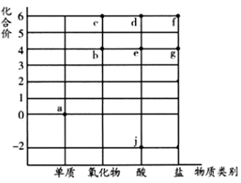
请回答下列问题:
-
(1) 硫元素在周期表中的位置。
-
(2) 氧元素比硫元素的非金属性(填“强"或“弱"”)。请用化学方程式证明该结论:。
-
(3) 写出b与j混合,发生反应的化学方程式。
-
(4) 已知硒(Se)与硫是相邻周期同主族元素。
①画出硒原子结构示意图。
②判断硒元素的主要化合价有。
③硒最高价氧化物的水化物与d相比较,酸性强弱关系为>(填化学式)。
| 选项 | X | Y | Z | Z实验现象或结论 | 装置 |
| A | 稀硫酸 | 亚硫酸钠 | 品红溶液 | SO2能氧化品红 | |
| B | 双氧水 | MnO2 | 氢硫酸溶液 | 产生浑浊 | |
| C | 浓盐酸 | 石灰石 | 硅酸钠溶液 | 非金属性:C>Si | |
| D | 稀硫酸 | 硫化亚铁 | 硫酸铜溶液 | 无明显现象,弱酸不能制强酸 |
-
(1) A元素原子的半径最大,写出A在元素周期表中的位置,其原子核外电子排布式为,A与上述元素中原子半径最小的元素B形成的化合物晶体类型为。
-
(2) C元素的单质能溶解于C与D形成的化合物中,写出该化合物的分子式,推断该化合物(难、微、易)溶于水。
-
(3) C、D元素均可与B元素形成化合物,此2种化合物都可与水反应形成对应的酸,2种酸的分子式相似,写出2种酸的分子式,简述证明2种酸酸性相对强弱的方法。
Cu2S和CuS均可被KMnO4酸性溶液氧化,在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下:
①
 + Cu2S +
+ Cu2S +  →
→  + SO2↑ +
+ SO2↑ +  + H2O(未配平)
+ H2O(未配平)②
 + CuS +
+ CuS +  →
→  + SO2↑ +
+ SO2↑ +  + H2O(未配平)
+ H2O(未配平) -
(4) 下列关于反应①的说法中错误的是(选填编号)。
a.还原性的强弱关系是:
 > Cu2S
> Cu2Sb.氧化剂与还原剂的物质的量之比为
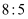
c.生成2.24L(标况下)SO2 , 转移电子的物质的量是0.8mol
d.被氧化的元素是正一价的Cu和负二价的S
-
(5) 写出反应②中反应物配平后的系数并标出电子转移方向和数目:
_
 +_CuS +_
+_CuS +_ 
已知:KMnO4在稀硫酸存在下能将H2O2氧化为O2 , KMnO4被还原为
 ;H2O2在前面反应生成
;H2O2在前面反应生成  的催化下能发生分解反应生成H2O和O2。
的催化下能发生分解反应生成H2O和O2。 -
(6) 稀硫酸中,某KMnO4和H2O2发生氧化还原反应方程式如下:
2KMnO4 + 7H2O2 + 3H2SO4 → K2SO4 + 2MnSO4 + 6O2↑ + 10H2O,反应中1mol KMnO4氧化H2O2的物质的量是mol, 反应中的氧化剂是,氧化剂与还原剂的物质的量比为。
-
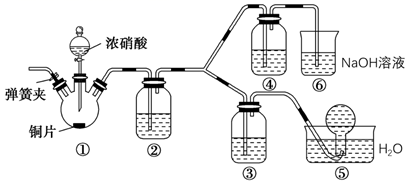
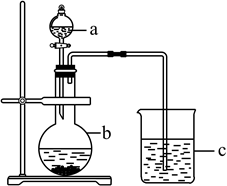
(1) 仪器a的名称是,应盛放下列药品中的(填字母)。
A.稀硫酸 B.亚硫酸 C.氢硫酸 D.盐酸
-
(2) 仪器b的名称是,应盛放下列药品中的(填字母)。
A.碳酸钙 B.硫酸钠 C.氯化钠 D.碳酸钠
-
(3) 仪器c中盛放的试剂是澄清石灰水,如果看到的现象是,说明b中发生反应的化学方程式为,即可证明H2SO4比H2CO3酸性强。
-
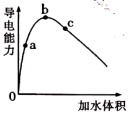
(1) 取冰醋酸配制250mL 0.4mol/L的醋酸溶液,用0.4mol/L的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对该醋酸溶液的浓度进行标定。
①将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示。解稀释过程中a、b、c点对应溶液的pH由大到小的顺序为。
②为标定稀释所得醋酸溶液的准确浓度,用0.2000mol/L的NaOH标准溶液对20.00mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如表:
实验序号
1
2
3
4
消耗NaOH溶液的体积(mL)
20.05
20.00
18.80
19.95
该醋酸溶液的准确浓度为mol/L。上述标定过程中,会造成测定结果偏高的原因可能是(填字母)。
A.未用标准液润洗碱式滴定管
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
-
(2) 该小组同学探究浓度对醋酸电离程度的影响时,用pH计测定25℃时不同浓度醋酸的pH,其结果如表:
醋酸浓度(mol/L)
0.0010
0.0100
0.0200
0.1000
0.2000
pH
3.88
3.38
3.23
2.88
2.73
①根据表中数据,可得出醋酸是弱电解质的结论,你认为得出此结论的依据是。
②从表中数据还可得出另一结论:随着醋酸浓度的增大,醋酸的电离程度将(填“增大”、“减小”或“不变”)。
③利用水解理论设计实验证明醋酸的酸性比碳酸的强:。
选项 | 操作 | 现象 | 结论 |
A | 向澄清的苯酚钠溶液中通入 | 溶液出现浑浊 | 碳酸酸性强于苯酚 |
B | 向淀粉水解液中加入 | 溶液未变蓝 | 淀粉已水解 |
C | 将一小块金属钠放入盛有少量无水乙醇的试管中 | 金属钠下沉,产生气泡 | 乙醇中含有少量水 |
D | 将电石和饱和食盐水反应产生的气体直接通入酸性高锰酸钾溶液 | 紫红色褪去 | 产生的气体为乙炔 |
- 2011年9月,国家统计局举办了第二届“中国统计开放日”,向来自全国各地各行各业的 社会公众代表详细展示了统计数据的产
- 抛物线y=x2-4x-7的顶点坐标是 A.(2,-11) B.(-2,7) C.(2,1
- 下列属于传统工业的有( ) A.航天工业
- (07年南开区检测)如图所示的装置,放置在温度较低的空气中,物体沿斜面缓慢匀速下滑过程中,下列判断正确的是 (
- 在下面语段的横线上填上合适的句子,使之与上下文句式相仿,意境相近。 如果生命是一杯酒,我愿相信它是世上最醇美的酒。 它是
- 规定将乌苏里江以东、包括库页岛在内的中国领土割让给俄国的不平等条约是()A、中俄《瑷珲条约》
- (四)阅读下面的词,完成下面试题。 临江仙 [宋]陈与义① 夜登小阁,忆洛中旧游②。 忆昔午桥桥上饮③,坐中多是
- 阅读填空 Look at the p 1 .It’s a picture o 2 a classroom.
- 用一种试剂鉴别苯酚、甲苯、福尔马林、四氯化碳、乙醇五种无色液体,该试剂是:A.FeCl3溶液
- 1915年兴起的新文化运动( )①加速了中国自然科学进步 ②促进了中国人民的进一步觉醒 推动③了中国新
- 根据句意用括号中单词的适当形式填空,使句子的意思完整、正确。 1. Here's a list of the most
- 近代史上,英、法、美、德都建立了代议制民主,其主要的共同点是() A.国家元首都拥有行政实权 B.内阁成员都由选举产生
- 读图1-4“一年内太阳辐射的纬度分布图”回答: 图1-4“一年内太阳辐射的纬度分布图” ⑴ 一月份,太阳辐射量最大的最大
- 某校综合实践活动小组准备以“居民参与民主管理”为主要内容进行研究性学习活动,那么他们最应该选择去的地方是 A.居民委员会
- 对中学生来讲,培养完美的人格,升华高尚的人品,需要“生活从叠被抓起,品德从孝心抓起,文明从说话抓起,学习从习惯抓起”。下
- 图中电表的示数分别为:甲图是 ,乙图是 。
- 一个铀核()放出一个α粒子后衰变成钍核(),其衰变方程为 ▲ ;已知静止的铀核、钍核和α粒子的质量分别为m1、m2和m
- 8牙齿在脊椎动物中是普遍存在的,哺乳动物发展到了高级阶段,它们的牙齿属于:A.同型齿 B.异型齿 C.多出齿 D.侧生齿
- 瓷器是中国古代文明象征之一,长期居于世界领先水平。我们浙江是中国的瓷器大省,唐宋以来涌现出名窑无数,下列属于浙江的名窑有
- A Kentucky young manwas taken to a hospital and then to coun
 =4.3×10-7
=4.3×10-7 =5.6×10-11
=5.6×10-11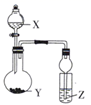
 气体
气体 溶液
溶液


