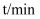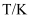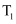化学平衡状态的判断 知识点题库
 CO2(g)+H2(g),达到平衡后,有关化学反应限度的说法正确的是( )
CO2(g)+H2(g),达到平衡后,有关化学反应限度的说法正确的是( )
请回答下列问题:
-
(1) 判断该反应达到平衡状态的标志是(填字母).
a.SO2和SO3浓度相等 b.SO2百分含量保持不变
c.容器中气体的压强不变 d.SO3的生成速率与SO2的消耗速率相等
-
(2) 当该反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高SO2平衡转化率的是.(填字母)
a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.降低温度
-
(3) 将0.050mol SO2(g)和0.030mol O2(g)放入容积为1L的密闭容器中,在一定条件下达到平衡,测得c(SO3)=0.040mol/L.计算该条件下反应的平衡常数K和SO2的转化率(不必写出计算过程).
①平衡常数K=;②平衡时,SO2的转化率α(SO2)=
-
(4) SO2尾气常用饱和Na2SO3溶液吸收,减少SO2气体污染并可得到重要的化工原料NaHSO3 . 已知NaHSO3
溶液同时存在以下两种平衡:①HSO3﹣⇌SO32﹣+H+ , ②HSO3﹣+H2O⇌H2SO3+OH﹣;常温下,0.1mol/L NaHSO3溶液的pH<7,则该溶液中c(H2SO3) c(SO32﹣)(填“>”、“=”或“<”).
请回答下列问题:
-
(1) 判断该反应达到化学平衡状态的标志是(填字母).
a.SO2、O2、SO3三者的浓度之比为2:1:2 b.容器内气体的压强不变
c.容器内混合气体的密度保持不变 d.SO3的物质的量不再变化
e.SO2的生成速率和SO3的生成速率相等
-
(2) SO2的转化率.
①在该温度时,取1mol N2和3mol H2放在密闭容器中,在催化剂存在下进行反应,测得反应放出的热量总是92.4kJ.(填“小于”,“大于”或“等于”)
②一定条件下,上述可逆反应在体积固定的密闭容器中进行,下列叙述能说明反应已达到平衡的是.
A.NH3生成的速率与NH3分解的速率相等 B.混合气体的反应速率 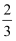 v正(NH3)=v逆(H2)
v正(NH3)=v逆(H2)
C.容器内的密度不再变化 D.单位时间内消耗a mol N2 , 同时生成2a mol NH3 .
X(g)+2Y(g) 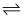 2Z(g) 此反应达到平衡的标志是( )
2Z(g) 此反应达到平衡的标志是( )
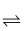 CO(g) + H2O(g),化学平衡常数K和温度t的关系如下表:
CO(g) + H2O(g),化学平衡常数K和温度t的关系如下表: t/℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
请回答下列问题:
-
(1) 该反应的化学平衡常数表达式为K = ;
-
(2) 该反应为反应(填“吸热”或“放热”。)
-
(3) 能判断该反应达到化学平衡状态的是(填字母)。
a.容器中总压强不变
b.混合气体中c(CO)不变
c.H2消耗的速率与H2O消耗的速率相等
d.c(CO2)= c(CO)
 C(g)+2D(g)。5min后达到平衡,测得容器内B的浓度减少了0.2mol/L,则下列叙述错误的是( )
C(g)+2D(g)。5min后达到平衡,测得容器内B的浓度减少了0.2mol/L,则下列叙述错误的是( )
 SO3(g)+NO(g),下列能说明反应达到反应限度的是( )
SO3(g)+NO(g),下列能说明反应达到反应限度的是( )
 2SO3(g)
2SO3(g)  H<0,向某体积恒定的密闭容器中按体积比2:1充入SO2和O2在一定条件下发生反应(纵坐标Y表示SO3的浓度)。下列说法正确的是( )
H<0,向某体积恒定的密闭容器中按体积比2:1充入SO2和O2在一定条件下发生反应(纵坐标Y表示SO3的浓度)。下列说法正确的是( ) 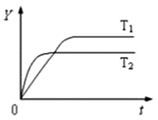
-
(1) N2O是一种强温室气体,且易形成颗粒性污染物,研究N2O的分解对环境保护有重要意义。碘蒸气存在能大幅度提高N2O的分解速率,反应历程为:
第一步I2(g)→2I(g)(快反应)
第二步I(g)+N2O(g)→N2(g)+IO(g)(慢反应)
第三步IO(g)+N2O(g)→N2(g)+O2(g)+I2(g)(快反应)
实验表明,含碘时N2O分解速率方程v=k·c(N2O)·[c(I2)]0.5(k为速率常数)。下列表述正确的是__________。
A . N2O分解反应中:分解速率与是否含碘蒸气有关 B . 第三步对总反应速率起决定作用 C . 第二步活化能比第三步小 D . IO为反应的催化剂 -
(2) 汽车尾气中含有较多的氮氧化物和不完全燃烧的CO,汽车三元催化器可以实现降低氮氧化物的排放量。汽车尾气中的NO(g)和CO(g)在催化剂的作用下转化成两种无污染的气体。如,
反应I:2CO +2NO → N2+2CO2 △H1; 反应II:4CO +2NO2 → N2+4CO2 △H2<0。
针对反应I:①已知:反应N2(g)+O2(g)=2NO(g) △H3=+180.0kJ·mol−1 , 若CO的燃烧热为-283.5kJ·mol−l 则反应I的△H1=kJ·mol−1。
②若在恒容的密闭容器中,充入2molCO和1molNO,发生反应I,下列选项中不能说明该反应已经达到平衡状态的是。
A.CO和NO的物质的量之比不变 B.混合气体的密度保持不变
C.混合气体的压强保持不变 D.2v(N2)正=v(CO)逆
-
(3) 根据原电池原理和电解原理进行如图回答。请回答: 用如图所示装置进行实验(K闭合).
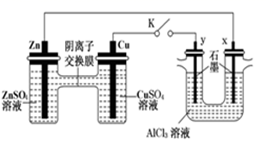
①Zn极为极;实验过程中,SO42-(填“从左向右”、“从右向左”或“不”)移动。
②y极的电极反应现象为;
③写出生活中对钢闸门的一种电化学保护方法。
④有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl−NH4Cl为电解质溶液制取新型燃料电池,请写出该电池的正极反应式。
 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表: | 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
-
(1) 写出该反应的平衡常数表达式:K=,已知:K(300℃)>K(350℃),该反应是反应(填“放热”或“吸热”)。
-
(2) 下图中表示NO2的变化的曲线是,用O2的浓度变化表示从0~2 s内该反应的平均速率v=。
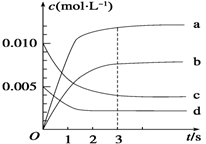
-
(3) 能说明该反应已经达到平衡状态的是()。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内物质的密度保持不变
-
(4) 能使该反应的反应速率增大,且平衡向正反应方向移动的是()。
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效的催化剂
|
化学键 |
C=C |
C—C |
C—O |
C—H |
O—H |
|
键能/kJ·mol-1 |
a |
b |
c |
d |
e |
-
(1) 工业上采用乙烯水化法制乙醇:CH2=CH2(g)+H2O(g)=CH3CH2OH(g) ΔH,根据表中键能数据计算ΔH=kJ·mo1-1。
-
(2) 工业上也可采用二氧化碳加氢合成乙醇:2CO2(g)+6H2(g)⇌CH3CH2OH(g)+3H2O(g)。恒容密闭容器中投入一定量CO2和H2发生上述反应,CO2的平衡转化率与温度、投料比m[m=
 ]的关系如图所示:
]的关系如图所示: 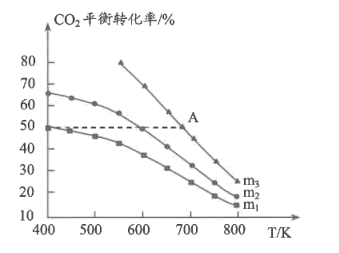
①投料比由大到小的顺序为(用m1 , m2 , m3表示)。
②某温度下,若投料比m=3,下列可判断反应达到平衡状态的是。
a.容器内气体压强不再变化
b.容器内气体平均相对分子质量不再变化
c.消耗3NA个氢气分子同时生成l.5NA个水分子
d.容器内
 不再变化
不再变化③若开始时投入6molH2和2molCO2 , 容器体积为3L。计算A点温度下该反应的平衡常数K=L4•mol-4;若换为恒压密闭容器,其它条件不变,则A点温度下平衡时CO2的转化率50%(填“>”、“=”或“<”)。
-
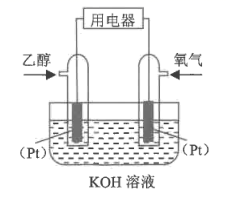
(3) 乙醇燃料电池是一种无污染电池,装置如图所示,写出该电池负极的电极反应式。
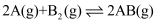
 ,在不同温度T下测得A的物质的量与时间t的关系如表所示。下列说法正确的是( )
,在不同温度T下测得A的物质的量与时间t的关系如表所示。下列说法正确的是( ) | | 0 | 5 | 8 | 13 |
| | 2.0 | 1.5 | 1.3 | 1.0 |
| | 2.0 | 1.15 | 1.0 | 1.0 |
 相比,
相比,  时分子动能大,活化分子百分数增大
B .
时分子动能大,活化分子百分数增大
B .  ,5~8min内,
,5~8min内, 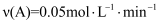 C .
C .  ,到13min时,反应已达到平衡状态
D . 反应达到平衡后,升高温度,平衡左移
,到13min时,反应已达到平衡状态
D . 反应达到平衡后,升高温度,平衡左移
 NH3(g)+H2O(g)+CO2(g) △H= a kJ·mol-1(a>0)。下列有关说法错误的是( )
NH3(g)+H2O(g)+CO2(g) △H= a kJ·mol-1(a>0)。下列有关说法错误的是( )
反应Ⅰ(主) :CH3OH(g)+ H2O(g)  CO2(g)+ 3H2(g) ΔH1=+49kJ/mol
CO2(g)+ 3H2(g) ΔH1=+49kJ/mol
反应Ⅱ(副) :H2(g)+ CO2(g)  CO(g)+ H2O(g) ΔH2=+41kJ/mol
CO(g)+ H2O(g) ΔH2=+41kJ/mol
温度高于300℃则会同时发生反应Ⅲ: CH3OH(g)  CO(g)+2H2(g) ΔH3
CO(g)+2H2(g) ΔH3
-
(1) 计算反应Ⅲ的ΔH3= 。
-
(2) 反应1能够自发进行的原因是,升温有利于提高CH3OH转化率,但也存在一个明显的缺点是。
-
(3) 下图为某催化剂条件下,CH3OH转化率、CO生成率与温度的变化关系。
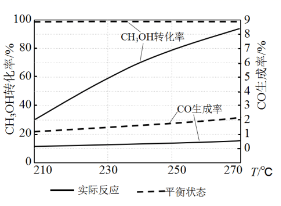
①随着温度的升高,CO的实际反应生成率没有不断接近平衡状态生成率的原因是 (填标号)。
A.反应Ⅱ逆向移动
B.部分CO 转化为CH3OH
C.催化剂对反应Ⅱ的选择性低
D.催化剂对反应Ⅲ的选择性低
②随着温度的升高,CH3OH 实际反应转化率不断接近平衡状态转化率的原因是。
③写出一条能提高CH3OH转化率而降低CO生成率的措施。
-
(4) 250℃,一定压强和催化剂条件下,1.00molCH3OH 和1.32molH2O 充分反应(已知此条件下可忽略反应Ⅲ ),平衡时测得H2为2.70mol,CO有0.030mol,试求反应Ⅰ中CH3OH 的转化率,反应Ⅱ的平衡常数(结果保留两位有效数字)
 。
。
-
(1) 反应过程中的能量变化如图所示。
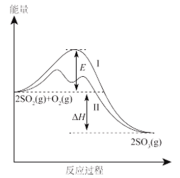
①该反应的
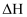 0(填“>”或“<”);加入催化剂后,反应历程为图中的路线(选填“Ⅰ”或“Ⅱ”)。
0(填“>”或“<”);加入催化剂后,反应历程为图中的路线(选填“Ⅰ”或“Ⅱ”)。②催化剂
 的催化机理为:
的催化机理为:  首先氧化
首先氧化 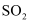 , 自身转化为四价钒化合物,然后四价钒化合物再被
, 自身转化为四价钒化合物,然后四价钒化合物再被  氧化。该催化过程发生反应的化学方程式依次为和
氧化。该催化过程发生反应的化学方程式依次为和  。
。 -
(2)
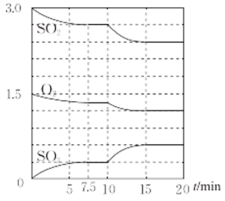
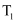 ℃时,向2L密闭固定容积容器中充入
℃时,向2L密闭固定容积容器中充入 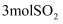 和
和 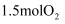 发生反应,各物质的物质的量随时间变化如图所示。
发生反应,各物质的物质的量随时间变化如图所示。
①下列可以判断该反应达到化学平衡状态的是(填序号)。
A.容器内混合气体密度不再变化 B.容器内混合气体压强不再变化
C.
 D.
D. 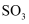 的体积分数不再变化
的体积分数不再变化②10min时改变了一个条件,该条件可能为(填序号)。
A.加催化剂 B.缩小容器容积
C.升高温度 D.加入一定量
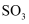
③0~7.5min内,用
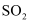 表示的平均速率
表示的平均速率  ;15min时,
;15min时,  的转化率为。若反应在15~20min对应温度和容积下,向该容器中充入
的转化率为。若反应在15~20min对应温度和容积下,向该容器中充入 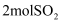 、
、 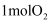 和
和 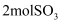 的瞬间
的瞬间 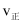
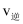 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
 与
与 为原料制备
为原料制备 , 发生反应
, 发生反应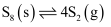 、
、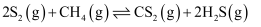 , 在密闭容器中,原料为1∶1时,部分物质变化曲线如图所示,下列说法正确的是( )
, 在密闭容器中,原料为1∶1时,部分物质变化曲线如图所示,下列说法正确的是( )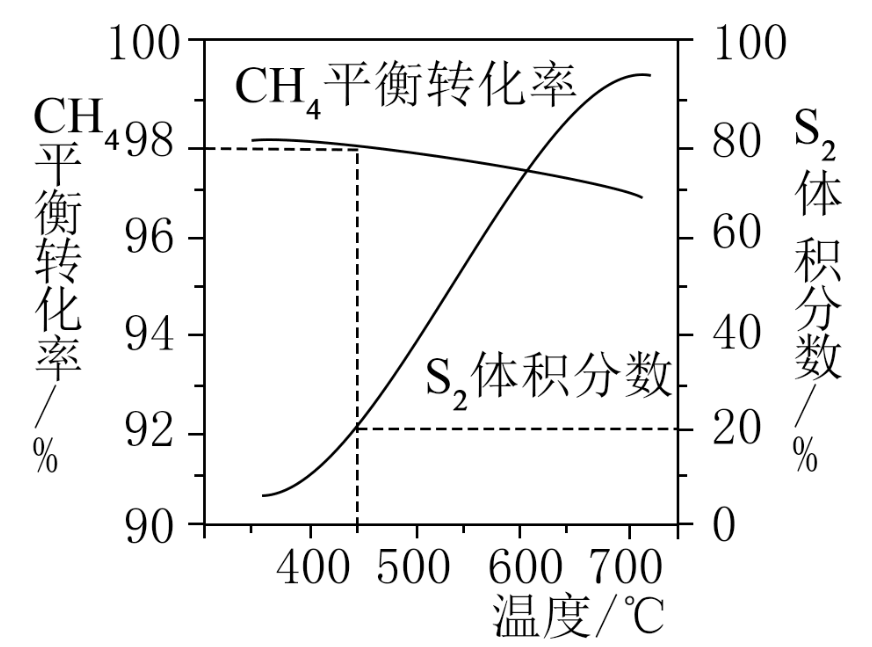
 的反应为吸热反应
B . 一定温度下,气体总压不变反应达平衡状态
C . 应在低温下进行反应以提高产出效率
D . 当温度为450℃时,
的反应为吸热反应
B . 一定温度下,气体总压不变反应达平衡状态
C . 应在低温下进行反应以提高产出效率
D . 当温度为450℃时, 转化率为67.5%
转化率为67.5%
-
(1) 在两个固定容积为2L的恒容密闭容器中均充入2molCO和2molNO,在不同条件下发生反应2CO(g)+2NO(g)
 2CO2(g)+N2(g),测得反应体系的压强与时间t的变化曲线如图。
2CO2(g)+N2(g),测得反应体系的压强与时间t的变化曲线如图。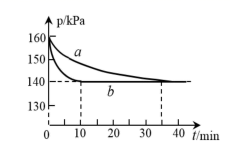
①与实验a相比,实验b采取的措施可能是;
②0~10min内,实验b对应条件下v(NO)=;
-
(2) CO和H2在一定条件下可以合成甲醇:CO(g)+2H2(g)
 CH3OH(g) ΔH。
CH3OH(g) ΔH。已知:v(正)=k(正)·x(CO)·x2(H2),v(逆)=k(逆)·x(CH3OH),其中x为各组分的体积分数。在密闭容器中按物质的量之比为1:2充入CO和H2 , 测得平衡混合气体中CO的平衡转化率随温度、压强的变化关系如图所示。
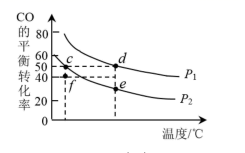
①p1p2(填“>”“<”);升高温度,
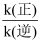 (“增大”“减小”或“不变”);
(“增大”“减小”或“不变”);②c、d、e三点平衡常数Kc、Kd、Ke三者之间的关系为
-
(3) 在一绝热恒容容器中,H2和CO按等物质的量混合反应,以下能说明反应达到平衡的是____。A . 容器内的总压强不再变化时 B . CO的体积分数保持不变时 C . 容器内气体平均密度不变时 D . 容器内气体温度恒定不变时
-
(4) 一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)
 2CO(g),平衡时,体系中气体体积分数与温度的关系如下图所示:已知:气体分压(p分)=气体总压(p总)×体积分数。925℃时,已知总压为p总 , 用平衡分压代替平衡浓度表示的化学平衡常数Kp=。
2CO(g),平衡时,体系中气体体积分数与温度的关系如下图所示:已知:气体分压(p分)=气体总压(p总)×体积分数。925℃时,已知总压为p总 , 用平衡分压代替平衡浓度表示的化学平衡常数Kp=。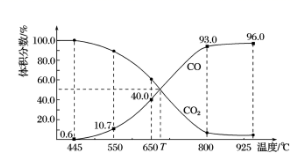
- 提供热量最多的一餐应该是 A.早餐 B.晚餐 C.午餐
- 根据要求填空: (1)FeSO4可转化为FeCO3,FeCO3在空气中加热可制得铁系氧化物材料 已知25℃,101kPa
- 利用化学方程式进行计算的依据是 A. 化学方程式表示了一种化学反应的过程 B. 化学方程式表示了反应物、生成物和反应条件
- 指出下列句子所使用的表达方式,依次判断正确的是( ) (1)秋目的艳阳在森林的树梢上欢乐地跳跃,把林子里墨绿的
- 如图,三条直线交于同一点,则∠1+∠2+∠3=_____.
- 已知,,,其中e是无理数且e=2.71828…,. (1)若a=1,求的单调区间与极值; (2)求证:在(1)的条件下,
- The teacher’s talk made us so i____________ that we were all
- 默写 (1) ,雪却输梅一段香。 (2)
- 如图,AB是⊙O的直径,且经过弦CD的中点H,已知sin∠CDB=,BD=5,则AH的长为()A.
- 下列中国近代史上的爱国和进步口号,其中最能揭示五四运动内容和性质的是() A.“打倒帝国主义”
- 与打点计时器一样,光电计时器也是一种研究物体运动情况的常用计时仪器,其结构如图甲所示, a、b分别是光电门的光发射和接收
- 下列有关化学实验操作中的“先”与“后”的说法正确的是 (填字母编号)A.给试管加热时,先给试管均匀加热,后固
- 在四边形ABCD中,=a+2b,=-4a-3b,=-5a-5b,那么四边形ABCD的形状是 A.矩形
- 为缓解能源紧张状况,国家页岩气十二五规划出台。 (1)页岩气与天然气的主要成份都是甲烷,甲烷在空气中完全燃烧的化学方程式
- Let ussuppose it is now about A.D. 2060. Let’s make believe
- 【探究名称】探究凸透镜成像的大小与哪些因素有关【提出问题】小明通过前面物理知识的学习,知道放大镜就是凸透镜.在活动课中,
- 抛物线与y轴交点的横坐标为( ) A.—3 B.—4 C.—5
- 长期以来,很多学者将中国近代史的基本线索概括为“两个过程”,即帝国主义和封建主义相结合,把中国变为半殖民地和殖民地的过程
- 平面向量与的夹角为60°,,则等于( ) A. B. C.
- (08年沈阳二中月考)如图所示为一只多用电表的原理图,它的正确使用是 A.只合上K1可当安培表用 B.只合上K2可当伏