化学平衡状态的判断 知识点题库
在2L的密闭容器中进行如下反应:mX(g) 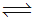 pZ(g)+qQ(g)
pZ(g)+qQ(g)
在2秒钟内用X表示的平均反应速率为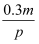 mol/(L·s),则2秒钟内Q物质增加了( )
mol/(L·s),则2秒钟内Q物质增加了( )
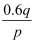 mol
B .
mol
B . 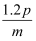 mol
C .
mol
C . 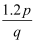 mol
D .
mol
D . 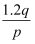 mol
mol
①C的生成速率与C的分解速率相等
②单位时间内生成a molA,同时生成3a molB
③A,B,C的浓度不再变化
④混合气体的总压强不再变化
⑤混合气体的物质的量不再变化
⑥A,B,C,D的分子数之比为1:3:2:2.
-
(1) 已知25℃,1.01×105Pa时,8.0g CH4完全燃烧生成二氧化碳气体和液态水放出444.8kJ热量。写出该反应的热化学反应方程式:。
-
(2) 为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量及有效地开发利用CO2 , 工业上可以用CO2来生产燃料甲醇。在体积为2L的密闭容器中,充入1mol CO2和3mol H2 , 一定条件下发生反应:CO2(g) + 3H2(g)
 CH3OH(g) + H2O(g)。经测得CO2和CH3OH(g)的物质的量随时间变化如图所示。
CH3OH(g) + H2O(g)。经测得CO2和CH3OH(g)的物质的量随时间变化如图所示。 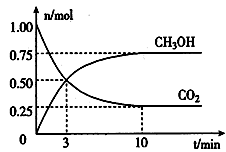
①从反应开始到平衡,CO2的平均反应速率v(CO2)=。
②达到平衡时,H2的转化率为。
③该反应的平衡常数K=(表达式)。
④下列措施不能提高反应速率的是。
A.升高温度
B.加入催化剂
C.增大压强
D.及时分离出CH3OH
-
(3) 工业上也用CO和H2为原料制备CH3OH,反应方程式为:CO(g) + 2H2(g)
 CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是______。
A . 反应中CO与CH3OH的物质的量之比为1:1 B . 混合气体的压强不随时间的变化而变化 C . 单位时间内每消耗1 mol CO,同时生成1 mol CH3OH D . CH3OH的质量分数在混合气体中保持不变 E . 混合气体的密度保持不变
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是______。
A . 反应中CO与CH3OH的物质的量之比为1:1 B . 混合气体的压强不随时间的变化而变化 C . 单位时间内每消耗1 mol CO,同时生成1 mol CH3OH D . CH3OH的质量分数在混合气体中保持不变 E . 混合气体的密度保持不变
 2Z(g),10min后反应达到平衡,其中Z的含量(体积分数)为25%。
2Z(g),10min后反应达到平衡,其中Z的含量(体积分数)为25%。
-
(1) 平衡吋,Y的物貭的量浓度为。
-
(2) 10 min内,Z的平均反应速率为 。
-
(3) 达到平衡时,容器内起始吋与平衡吋的圧強之比是 。
-
(4) 不能証明该反应达到化学平衡状态的标志是_______ (填字母)A . 圧強不再发生变化 B . 混合气体的相对分子貭量不再发生变化 C . X、Y、Z的分子数之比内1:3:2 D . 混合气体的密度不变
-
(1) 反应(Ⅰ)中氧化剂是。
-
(2) 火箭残骸中常出现红棕色气体,原因为:N2O4(g)
 2NO2(g)(Ⅱ)当温度升高时,气体颜色变深,则反应(Ⅱ)为(填“吸热”或“放热”)反应。
2NO2(g)(Ⅱ)当温度升高时,气体颜色变深,则反应(Ⅱ)为(填“吸热”或“放热”)反应。
-
(3) 一定温度下,反应(Ⅱ)的焓变为ΔH。现将1 mol N2O4充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是。
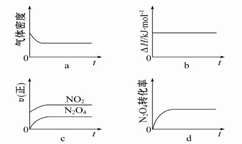
若在相同温度下,上述反应改在体积为1 L的恒容密闭容器中进行,平衡常数(填“增大”“不变”或“减小”),反应3 s后NO2的物质的量为0.6 mol,则0~3 s内的平均反应速率v(N2O4)= mol·L-1·s-1。
-
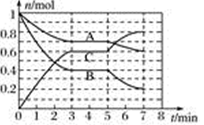
(1) 该反应的化学方程式。
-
(2) 在min时反应刚好达到平衡。
-
(3) 在0~3minA物质的平均速率为,此时A物质的转化率为,3min末时A物质的浓度为。
-
(4) 5~7 min内B的平均速率1~3min内B的平均速率(填大于、小于、等于)。
-
(5) 下列措施可加快该反应速率的是__________。A . 扩大容器体积 B . 使用恰当的催化剂 C . 提高反应的温度 D . 液化并转移出C物质
 2NO+O2在密闭容器反应,达到平衡状态的标志是( )
2NO+O2在密闭容器反应,达到平衡状态的标志是( ) ⑴单位时间内生成n molO2的同时,生成2n molNO2
⑵单位时间内生成n molO2的同时,生成2n mol NO
⑶用NO2、NO、O2的物质的量浓度变化表示反应速率的比为2:2:1的状态
⑷混合气体的颜色不再改变的状态
⑸混合气体的平均相对分子质量不再改变的状态
 2NO2(g),该反应体系中n(NO)随时间的变化如下表:
2NO2(g),该反应体系中n(NO)随时间的变化如下表: | 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.022 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
下列有关说法错误的是( )
-
(1) 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
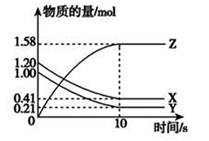
①写出该反应的化学方程式。
②计算反应开始到10s,用X表示的反应速率是。
③下列叙述中能说明上述反应达到平衡状态的是 (填写序号)。
a.当X与Y的反应速率之比为1:1
b.混合气体中X的浓度保持不变
c.X、Y、Z的浓度之比为1:1:2
④为使该反应的反应速率增大,可采取的措施是 (填写序号)。
A.适当降低温度 b.扩大容器的体积 c.充入一定量Z
-
(2) 某学生为了探究锌与盐酸反应过程中的速率变化,在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(表中气体体积为累计值,且已转化为标准状况):
时间(min)
1
2
3
4
5
氢气体积(mL)
50
120
232
290
310
①2—3min反应速率最大,原因是。
②如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,在盐酸中分别加入等体积的下列溶液:A.蒸馏水;B.NaCl溶液;C.NaNO3溶液;D.CuSO4溶液;E.Na2CO3溶液,你认为可行的是(填选项代号)。
-
(3) 氢气用于工业合成氨N2(g)+3H2(g)
 2NH3(g)△H=-92.2kJ/mol,一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如图所示,其中t4、t5、t7时刻所对应的实验条件改变分别是:t4,t5,t7。
2NH3(g)△H=-92.2kJ/mol,一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如图所示,其中t4、t5、t7时刻所对应的实验条件改变分别是:t4,t5,t7。 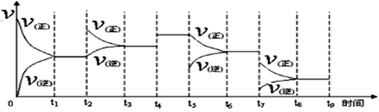
-
(1) 一种脱硫工艺为:真空K2CO3-克劳斯法。
①K2CO3溶液吸收H2S的反应为K2CO3+H2S=KHS+KHCO3 , 该反应的平衡常数的对数值为lgK=。(已知:H2CO3 lgK1= -6.4,lgK2=-10.3; H2S lgK1ˊ= -7,lgK2ˊ= -19)
②已知下列热化学方程式:
2H2S(g) +3O2(g)=2SO2(g)+2H2O(l) ΔH1= -1172kJ·mol-1
2H2S(g) +O2(g)=2S (s) +2H2O(l) △H2 = -632 kJ·mol-1
克劳斯法回收硫的反应为SO2气体和H2S气体反应生成S(s),则该反应的热化学方程式为。
-
(2) 工业采用高温分解H2S制取氢气,2H2S(g)
 2H2(g) +S2(g),在膜反应器中分离出H2。在容积为2L的恒容密闭容器中,控制不同温度进行此反应。H2S的起始物质的量均为1mol,实验过程中测得H2S的转化率如图所示。曲线a表示H2S的平衡转化率与温度的关系,曲线b表示不同温度下反应经过相同时间时H2S的转化率。
2H2(g) +S2(g),在膜反应器中分离出H2。在容积为2L的恒容密闭容器中,控制不同温度进行此反应。H2S的起始物质的量均为1mol,实验过程中测得H2S的转化率如图所示。曲线a表示H2S的平衡转化率与温度的关系,曲线b表示不同温度下反应经过相同时间时H2S的转化率。
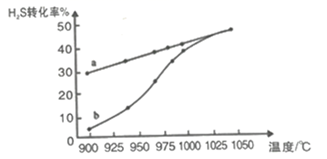
①反应2H2S(g)⇌2H2(g) + S2(g) 的ΔH(填“>”“<”或“=”) 0。
②985℃ 时,反应经过5 s达到平衡状态,此时H2S的转化率为40%,则用H2表示的反应速率为v(H2) =,下列各项不能作为该反应达到平衡状态的标志的是。
A.压强不再变化
B.气体密度不再变化
C.气体的平均相对分子质量不再变化
D.H2的消耗速率与S2的消耗速率之比为2:1
E. S2 的在体系中质量分数保持不变
③随着H2S分解温度的升高,曲线b向曲线a逐渐靠近,其原因是。
-
(3) 科学家设计出质子膜H2S燃料电池,实现了利用H2S废气资源回收能量并得到单质硫。质子膜H2S燃料电池的结构示意图如图所示。
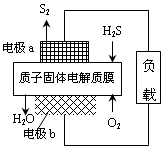
①装置中微电池负极的电极反应式:
②当有16gS2析出时,有mol H+ 经质子膜进入正极区。
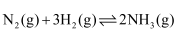 。在反应过程中反应物和生成物的物质的量随时间的变化如图所示。下列说法错误的是( )
。在反应过程中反应物和生成物的物质的量随时间的变化如图所示。下列说法错误的是( ) 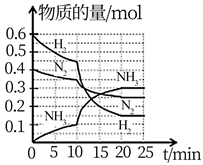
 表示的平均反应速率为
表示的平均反应速率为 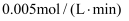 B . 10~20min内,
B . 10~20min内,  浓度变化的原因可能是缩小容器容积
C .
浓度变化的原因可能是缩小容器容积
C .  的平衡转化率与
的平衡转化率与  平衡转化率相等
D . 该反应在20min时达到化学平衡状态
平衡转化率相等
D . 该反应在20min时达到化学平衡状态
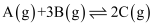 ;经3s后达到平衡,测得C气体的浓度为
;经3s后达到平衡,测得C气体的浓度为 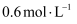 ,下列说法中不正确的是( )
,下列说法中不正确的是( )
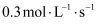 B . 平衡后,向容器中充入无关气体(如Ne),反应速率增大
C . 3s时生成C的物质的量为1.2 mol
D . 平衡后,
B . 平衡后,向容器中充入无关气体(如Ne),反应速率增大
C . 3s时生成C的物质的量为1.2 mol
D . 平衡后, 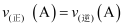
反应Ⅰ: 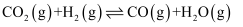
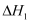
反应Ⅱ: 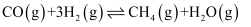
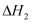
反应Ш: 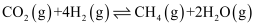

其对应的平衡常数分别为K1、K2、K3 , 其中K1、K2随温度变化如下表所示:
|
250℃ |
300℃ |
350℃ |
|
|
K1 |
0.01 |
0.05 |
0.1 |
|
K2 |
2 |
0.2 |
0.05 |
回答下列问题:
-
(1) △H20(填“>”、“<”或“=”),△H2△H3(填“>”、“<”或“=”)。
-
(2) 往容积可变的密闭容器中通入1molCO2和4molH2 , 在一定条件下发生反应Ⅲ,测得H2的平衡转化率与压强、温度的关系如图所示。
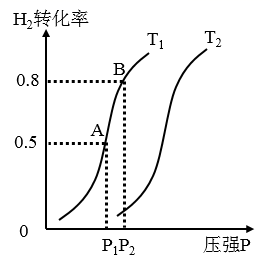
①能说明上述反应已达到平衡状态的是(选填字母)。
A.
 B.CO2与H2的物质的量之比保持不变
B.CO2与H2的物质的量之比保持不变C.H-H键、H-O键断裂速率相等 D.CH4的体积分数保持不变
②据图可知,T1T2(填“>”或“<”)。
③若反应达到平衡点A,此时容器的体积为2L,则该温度下反应Ⅲ的平衡常数K=。
-
(3) 若容器的容积固定不变,在坐标系中画出从常温时通入1 mol CO2和4molH2开始(仅发生反应Ⅲ),随温度不断升高,浓度商Q值(
 )的变化趋势图。
)的变化趋势图。
-
(4) 某研究小组研究了不同电压(电压影响催化剂活性)、不同C/H比对反应Ⅲ的影响如图所示(控制其他条件相同),下列说法正确的是_______。
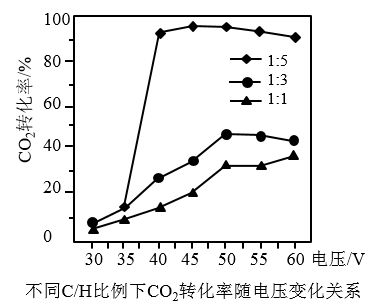 A . 当C/H比一定时,电压越高,CO2的转化率越高 B . 考虑到CO2的转化率和经济成本,应尽可能减小C/H比 C . 在合适的电压范围内,增大H2的比例可能有利于消除积碳,提高催化剂的活性 D . 为使CO2的转化率达到90%,C/H比应控制在1:5为宜
A . 当C/H比一定时,电压越高,CO2的转化率越高 B . 考虑到CO2的转化率和经济成本,应尽可能减小C/H比 C . 在合适的电压范围内,增大H2的比例可能有利于消除积碳,提高催化剂的活性 D . 为使CO2的转化率达到90%,C/H比应控制在1:5为宜
 ,该反应一般认为通过如下步骤来实现,反应进程与体系能量变化关系如图所示:
,该反应一般认为通过如下步骤来实现,反应进程与体系能量变化关系如图所示: 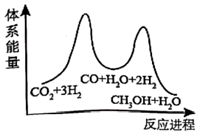
① 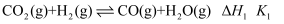
② 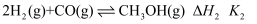
回答下列问题:
-
(1)
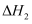 0(填“>”或“<”,)。
0(填“>”或“<”,)。
-
(2) 对于合成甲醇总反应,要加快其反应速率并使其在一定条件下建立的平衡正向移动,可采取的措施有___________(填字母,后同)。A . 增大反应容器的容积 B . 缩小反应容器的容积 C . 从平衡体系中及时分离出
 D . 升高温度
E . 使用合适的催化剂
D . 升高温度
E . 使用合适的催化剂
-
(3) 一定温度下,将
 和
和  以物质的量之比为1:1充入盛有催化剂的密闭容器中,发生合成甲醇总反应;某时刻t1 , 当下列量不再变化时,一定能说明该反应处于平衡状态的是___________(填字母)
A . 平衡常数K不再变化 B .
以物质的量之比为1:1充入盛有催化剂的密闭容器中,发生合成甲醇总反应;某时刻t1 , 当下列量不再变化时,一定能说明该反应处于平衡状态的是___________(填字母)
A . 平衡常数K不再变化 B . 的体积分数不再变化
C .
的体积分数不再变化
C .  的体积分数不再变化
D . 反应的焓变
的体积分数不再变化
D . 反应的焓变 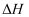 不再变化
不再变化
-
(4) 500℃时,已知
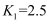 ,
,  。往2L恒容密闭容器中充入
。往2L恒容密闭容器中充入 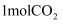 和
和 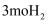 ,测得某时刻t2 , 合成甲醇总反应中
,测得某时刻t2 , 合成甲醇总反应中  的转化率为66.67%(约转化了
的转化率为66.67%(约转化了 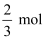 ),则t2时合成甲醇总反应的
),则t2时合成甲醇总反应的 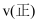
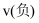 (填“>、<”或“=”),并通过计算说明理由。
(填“>、<”或“=”),并通过计算说明理由。
 2C(g)达到平衡状态标志的是( )
2C(g)达到平衡状态标志的是( ) ①C生成的速率与C分解的速率相等
②单位时间内生成a mol A,同时生成3a mol B
③A、B、C的浓度不再变化
④A、B、C的百分含量不再变化
⑤混合气体的总压强不再变化
⑥混合气体的物质的量不再变化
⑦单位时间内消耗a mol A,同时生成3a mol B
⑧A、B、C的分子数之比为1∶3∶2
-
(1) I.将CO2转化成甲醇燃料是减排、环保的一种科学方法。
已知:2H2(g)+O2(g) =2H2O(g);△H=-483.6kJ·mol-1 ①
2CO2(g)+4H2O(g) = 2CH3OH(g)+3O2(g);ΔH=+1352.8kJ·mol-1②
则用CO2与H2反应制备 CH3OH(g),同时生成水蒸气的热化学方程式为:
CO2(g)+3H2(g) = CH3OH(g)+H2O(g) ΔH=。
-
(2) II.在容积为2L的密闭容器中,进行如下反应:A(g)+2B(g)
 C(g)+D(g),最初加入1.0molA和2.2molB,在不同温度下,D的物质的量n(D)和时间t的关系如图。
C(g)+D(g),最初加入1.0molA和2.2molB,在不同温度下,D的物质的量n(D)和时间t的关系如图。 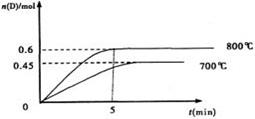
试回答下列问题:
800℃时,0—5min内,以B表示的平均反应速率为。
-
(3) 能判断该反应达到化学平衡状态的依据是。
a.容器中压强不变 b.混合气体中c(A)不变
c.2v正(B)=v逆(D) d.c(A)=c(C)
-
(4) 若最初加入1.0molA和2.2molB,利用图中数据计算800℃时的平衡常数K=,该反应为反应(填吸热或放热),判断理由是。
-
(5) 800℃时,某时刻测得体系中各物质的量如下:n(A)=0.9mol,n(B)=2.0mol,n(C)=0.9mol,n(D)=0.9mol,则此时该反应进行(填“向正反应方向”“向逆反应方向”或“处于平衡状态”)。
 2Z(g),一段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g),一段时间后达到平衡。反应过程中测定的数据如下表:t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是( )
- 关于化学反应与能量变化的叙述不正确的是A.在化学反应中只有燃烧才能放出热量B.物质的缓慢氧化均放出热量C.物质发生化学反
- 在下图所示的实例中,通过热传递改变物体内能的是( )
- 烯烃与氢气加成生成烷烃,但烷烃不一定都能由烯烃与氢气加成得到。下列烷烃不能由烯烃和氢气通过加成反应制得的是()A.正戊
- How about taking ___ short break?I want to make ___ call. A.
- 依次填入下列各句横线处的词语,最恰当的一组是 ①要解决我国法律服务市场监管_______的问题,就必须完善相关立法,改革
- In January , 2004, the United States successfully launched “
- 关于质点,下列描述中正确的是( )A.质点就是体积很小的物体B.只有低速运动的物体才可看成质点,高速运动的
- ―Three _____ injured students died in a hospital ineast Chin
- 已知锐角α满足sin(α-)=,则cosα等于( )A. B.C.
- 近几年,不满足于在国内购物的消费者开始将眼光转向境外,轻点鼠标,去海外“淘宝”,这种购物方式被称为“海淘”。现在,越来越
- 列宁说:我们原来打算“直接用无产阶级的国家法令,在一个小农国家里按共产主义原则来调整国家的生产和产品分配,现实生活中说明
- “禅让”是我国原始社会民主推举部落联盟首领的办法,这种办法实行顺序是( ) A.舜→禹→尧 B.
- 下列各组中两个变化所发生的反应,属于同一类型的是 ①由甲苯制甲基环己烷、由乙烷制溴乙烷②乙烯使溴水褪色、乙炔使酸性高锰酸
- 西周时期,一位诸侯王娶了一位妻子,这位妻子为他生了一个女儿,后来又娶了一个妾.该妾为他生了大儿子,后来妻子又为他生了二儿
- 关于下列力的说法中,正确的是( ) A.合力必大于分力 B.运动物体所受摩擦力的方向一定和它运动方向相反 C.
- 用如图装置测定空气中氧气的体积分数。 (1)燃烧匙中红磷反应的文字表达式______该实验的现象是______。 (2)
- 一做直线运动的物体,其位移s与时间t的关系是s=3t-t2,则物体的初速度是________.
- 下列四幅不同比例尺的地图.图幅大小相同,其中表示范围最大的是( )
- I know this is not quite the right word, but I can’t be both
- 氨和联氨(N2H4)是氮的两种常见化合物。在科学技术和生产中有重要的应用。根据题意完成下列计算: (1)联氨用亚硝酸氧化



