化学反应的可逆性 知识点题库
下列关于可逆反应的叙述正确的是( )
A . 可逆反应是指既能向正反应方向进行,同时又能向逆反应方向进行的反应
B . 2H2O 2H2+O2与2H2+O2
2H2+O2与2H2+O2 2H2O互为可逆反应
C . 对于可逆反应,当正反应速率增大时,逆反应速率就会减小
D . 外界条件对可逆反应的正、逆反应速率影响的程度不一定相同
2H2O互为可逆反应
C . 对于可逆反应,当正反应速率增大时,逆反应速率就会减小
D . 外界条件对可逆反应的正、逆反应速率影响的程度不一定相同
 2H2+O2与2H2+O2
2H2+O2与2H2+O2 2H2O互为可逆反应
C . 对于可逆反应,当正反应速率增大时,逆反应速率就会减小
D . 外界条件对可逆反应的正、逆反应速率影响的程度不一定相同
2H2O互为可逆反应
C . 对于可逆反应,当正反应速率增大时,逆反应速率就会减小
D . 外界条件对可逆反应的正、逆反应速率影响的程度不一定相同
在一密闭容器中,用等物质的量的A和B发生如下反应A(g)+ 2B(g) 2C(g),反应达到平衡时,若混和气体中A和B的物质的量之和与C的物质的量相等,则这时A的转化率为( )
2C(g),反应达到平衡时,若混和气体中A和B的物质的量之和与C的物质的量相等,则这时A的转化率为( )
A . 40%
B . 50%
C . 60%
D . 70%
在密闭容器中进行如下反应:X2(g)+Y2(g)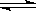 2 Z(g)。已知X2、Y2 、Z的起始浓度分别为0.2mol/L、0.6mol/L、0.4mol/L,在一定条件下反应达到平衡,各物质的浓度有可能是( )
2 Z(g)。已知X2、Y2 、Z的起始浓度分别为0.2mol/L、0.6mol/L、0.4mol/L,在一定条件下反应达到平衡,各物质的浓度有可能是( )
A . X2为0.4mol/L
B . Y2为0.4mol/L
C . Z为0.6mol/L
D . Z为0.8mol/L
298K时,合成氨反应的热化学方程式为:N2(g)+3H2(g) 2NH3(g);△H=﹣92.4kJ•mol﹣1 , 在该温度下,取1molN2和3molH2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量总是小于92.4KJ.其原因是
2NH3(g);△H=﹣92.4kJ•mol﹣1 , 在该温度下,取1molN2和3molH2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量总是小于92.4KJ.其原因是
在密闭容器中进行如下反应:X(g)+Y(g)⇌2Z(g).已知X、Y、Z的起始浓度分别为0.2mol/L、0.4mol/L、0.3mol/L,当反应在一定条件下达到平衡状态时.X的浓度范围 Y的浓度范围为 ,Z的浓度范围为
在密闭容器中进行如下反应:X2(g)+Y2(g)⇌2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol•L﹣1、0.3mol•L﹣1、0.2mol•L﹣1 , 在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )
A . X2为0.2 mol•L﹣1
B . Y2为0.2 mol•L﹣1
C . Z为0.3 mol•L﹣1
D . Z为0.45 mol•L﹣1
下列叙述错误的是( )
A . 任何可逆反应都有一定的限度
B . 化学反应达到平衡状态时,正、逆反应速率相等
C . 化学反应达到平衡状态与时间的长短无关
D . 化学平衡状态是不可改变的
对于反应2HI(g)  H2(g) +I2(g),下列叙述能够说明己达平衡状态的是( )
H2(g) +I2(g),下列叙述能够说明己达平衡状态的是( )
 H2(g) +I2(g),下列叙述能够说明己达平衡状态的是( )
H2(g) +I2(g),下列叙述能够说明己达平衡状态的是( )
A . 混合气体的颜色不再变化
B . 温度和体积一定时,容器内压强不再变化
C . 1molH-H键生成的同时有2molH-I键断裂
D . 各物质的物质的量浓度之比为2:1:1
恒温恒容条件下,不能表明反应: 2NO2(g)  2NO(g)+O2(g) 已达平衡状态的是( )
2NO(g)+O2(g) 已达平衡状态的是( )
 2NO(g)+O2(g) 已达平衡状态的是( )
2NO(g)+O2(g) 已达平衡状态的是( )
A . 容器中颜色不再改变
B . 混合气平均相对分子质量不再改变
C . 混合气密度不再改变
D . 单位时间内生成n mol O2的同时生成2n mol NO2
某温度下,密闭容器中发生反应N2(g)+3H2(g)  2NH3(g) △H=-92.4 kJ/mol。下列说法正确的是( )
2NH3(g) △H=-92.4 kJ/mol。下列说法正确的是( )
A . 将1.0 mol N2、3.0 mol H2置于1 L密闭容器中发生反应,放出热量为92.4 kJ
B . 上述反应达平衡后,若容积不变,再充入1.0 mol氦气,N2的转化率提高
C . 上述反应在达到平衡后,缩小容积增大压强,H2的转化率提高
D . 升高温度,平衡向逆反应方向移动,说明逆反应速率增大,正反应速率减小
已知2SO2+O2  2SO3 , 在体积为VL的密闭容器中通入amolSO2和bmolO2 , 充分反应后容器内硫原子数和氧原子数之比为( )
2SO3 , 在体积为VL的密闭容器中通入amolSO2和bmolO2 , 充分反应后容器内硫原子数和氧原子数之比为( )
A . 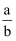 B .
B . 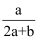 C .
C . 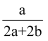 D .
D . 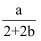
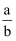 B .
B . 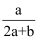 C .
C . 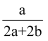 D .
D . 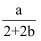
已知反应:NO2(g) + SO2(g)  SO3(g) + NO(g) ,起始时向某密闭容器中通入1 mol NO2、2 mol S18O2 , 反应达到平衡后,下列有关说法正确的是:( )
SO3(g) + NO(g) ,起始时向某密闭容器中通入1 mol NO2、2 mol S18O2 , 反应达到平衡后,下列有关说法正确的是:( )
 SO3(g) + NO(g) ,起始时向某密闭容器中通入1 mol NO2、2 mol S18O2 , 反应达到平衡后,下列有关说法正确的是:( )
SO3(g) + NO(g) ,起始时向某密闭容器中通入1 mol NO2、2 mol S18O2 , 反应达到平衡后,下列有关说法正确的是:( )
A . NO2中不可能含18O
B . 有1 mol N18O生成
C . S18O2的物质的量不可能为0. 8 mol
D . SO2、SO3、NO、NO2均含18O时,说明该反应达到平衡
在密闭容器中于一定条件下进行下列反应:2SO2+O2  2SO3 , 当达到平衡时通入18O2 , 再次平衡时,18O存在于( )
2SO3 , 当达到平衡时通入18O2 , 再次平衡时,18O存在于( )
 2SO3 , 当达到平衡时通入18O2 , 再次平衡时,18O存在于( )
2SO3 , 当达到平衡时通入18O2 , 再次平衡时,18O存在于( )
A . SO2、O2
B . SO2、SO3
C . SO2、O2、SO3
D . O2、SO3
CO2 + 4H2 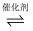 CH4 + 2H2O是CO2综合利用的一种方法。下列关于该反应的说法正确的是( )
CH4 + 2H2O是CO2综合利用的一种方法。下列关于该反应的说法正确的是( )
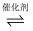 CH4 + 2H2O是CO2综合利用的一种方法。下列关于该反应的说法正确的是( )
CH4 + 2H2O是CO2综合利用的一种方法。下列关于该反应的说法正确的是( )
A . 适当升温能加快反应速率
B . 催化剂对反应速率无影响
C . 达到平衡时,正反应速率为0
D . 达到平衡时,CO2能100%转化为CH4
NA为阿伏加德罗常数,下列说法正确的是( )
A . 将1molN2与3molH2在一定条件下充分反应生成NH3分子数为2NA
B . 7.8g  中含有的碳碳双键数为0.3NA
C . 30g甲醛和乙酸的混合物中含有的碳原子数为NA
D . 100g质量分数34%的H2S溶液中极性键数目为2NA
中含有的碳碳双键数为0.3NA
C . 30g甲醛和乙酸的混合物中含有的碳原子数为NA
D . 100g质量分数34%的H2S溶液中极性键数目为2NA
下列说法正确的是( )
A . 《抱朴子》中“丹砂烧之成水银,积变又还成丹砂”两个反应互为可逆反应
B . 电热水器用镁棒防止内胆腐蚀,原理是牺牲阴极的阳极保护法
C . 门捷列夫根据元素的性质随着相对原子质量递增呈现周期性变化规律,制出了第一张元素周期表
D . 石灰乳与海水混合,过滤得 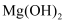 ,将其溶于盐酸,再蒸发结晶得到
,将其溶于盐酸,再蒸发结晶得到 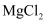 ,电解熔融
,电解熔融 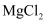 可得到金属镁
可得到金属镁
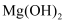 ,将其溶于盐酸,再蒸发结晶得到
,将其溶于盐酸,再蒸发结晶得到 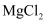 ,电解熔融
,电解熔融 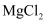 可得到金属镁
可得到金属镁
当可逆反应2SO2(g)+O2(g)=2SO3(g),达到平衡后通入18O2再次达到平衡时18O存在于( )
A . SO3、O2中
B . SO2、SO3中
C . SO2、O2、SO3中
D . SO2、O2中
根据下列实验操作和现象得出的结论正确的是( )
编号 | 实验操作 | 实验现象 | 解释与结论 |
A | 常温下,等体积等pH的HA、HB两种酸溶液分别与足量的锌反应 | 相同时间内,HB收集到的H2多 | 酸性强弱:HA > HB |
B | 将炽热的木炭加入到浓硝酸中 | 产生红棕色气体 | 木炭与浓硝酸反应生成NO2 |
C | 向盛有2mL 0.1mol/L AgNO3溶液的试管中滴加几滴0.1mol/L NaCl溶液,再向其中滴加0.1mol/L KI溶液 | 先得到白色沉淀后变为黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
D | 向1mL 0.5 mol/L KI溶液加入1mL 1mol/LFeCl3溶液,充分反应后向水层滴加KSCN溶液 | 溶液变红 | Fe3+与I-反应是可逆反应 |
A . A
B . B
C . C
D . D
在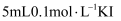 溶液中滴加5~6滴
溶液中滴加5~6滴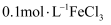 溶液充分反应后,再进行下列实验,其中可以证明
溶液充分反应后,再进行下列实验,其中可以证明 溶液和
溶液和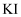 溶液的反应有一定限度的是( )
溶液的反应有一定限度的是( )
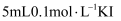 溶液中滴加5~6滴
溶液中滴加5~6滴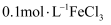 溶液充分反应后,再进行下列实验,其中可以证明
溶液充分反应后,再进行下列实验,其中可以证明 溶液和
溶液和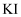 溶液的反应有一定限度的是( )
溶液的反应有一定限度的是( )
A . 取反应后的溶液少许,再滴加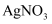 溶液,观察是否有
溶液,观察是否有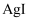 沉淀产生
B . 加入
沉淀产生
B . 加入 振荡后静置,取出下层液体,观察下层液体颜色
C . 加入
振荡后静置,取出下层液体,观察下层液体颜色
C . 加入 振荡后静置,取出上层液体,滴加
振荡后静置,取出上层液体,滴加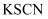 溶液观察是否变红
D . 加入
溶液观察是否变红
D . 加入 振荡后静置,取出上层液体,滴加
振荡后静置,取出上层液体,滴加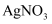 溶液观察是否有白色沉淀
溶液观察是否有白色沉淀
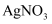 溶液,观察是否有
溶液,观察是否有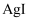 沉淀产生
B . 加入
沉淀产生
B . 加入 振荡后静置,取出下层液体,观察下层液体颜色
C . 加入
振荡后静置,取出下层液体,观察下层液体颜色
C . 加入 振荡后静置,取出上层液体,滴加
振荡后静置,取出上层液体,滴加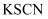 溶液观察是否变红
D . 加入
溶液观察是否变红
D . 加入 振荡后静置,取出上层液体,滴加
振荡后静置,取出上层液体,滴加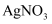 溶液观察是否有白色沉淀
溶液观察是否有白色沉淀
将0.2mol/L KI溶液和0.05mol/LFe2(SO4)3溶液等体积混合,充分反应后,取混合溶液分别完成下列实验,能说明溶液中存在化学平衡2Fe3+ + 2I- 2Fe2+ + I2的是(已知:Fe2+与K3 [Fe(CN)6]溶液反应有蓝色沉淀生成)( )
2Fe2+ + I2的是(已知:Fe2+与K3 [Fe(CN)6]溶液反应有蓝色沉淀生成)( )
 2Fe2+ + I2的是(已知:Fe2+与K3 [Fe(CN)6]溶液反应有蓝色沉淀生成)( )
2Fe2+ + I2的是(已知:Fe2+与K3 [Fe(CN)6]溶液反应有蓝色沉淀生成)( )实验编号 | 实验操作 | 实验现象 |
① | 滴入KSCN溶液 | 溶液变为红色 |
② | 滴入 | 有黄色沉淀生成 |
③ | 滴入K3 [Fe(CN)6]溶液 | 有蓝色沉淀生成 |
④ | 滴入淀粉溶液 | 溶液变为蓝色 |
A . ①
B . ①和②
C . ②和④
D . ③和④
最近更新
- 下图中,美国农业带的连接正确的是 A.①—乳畜带 B.②—玉米带 C.③—小麦区 D.④—
- 有人说“杂交水稻专家袁隆平培育的优质水稻若申请专利,它将超过比尔·盖茨成为全球首富”。而杂交水稻专家袁隆平培育的水稻良种
- 已知一次函数y1=kx+b与反比例函数y2=在同一直角坐标系中的图象如图所示,则当y1<y2时,x的取值范围是【 】
- 下图是某高等生物细胞局部结构模式图,请分析回答:(1)请判断该生物是________,理由:______________
- 明清时期中国瓷器外传的最重要路径是 ( )A.丝绸之路 B.海上丝绸之路 C.阿拉伯商人 D.波斯商
- 据《国语•周语》记载:周文王时曾与姒姓诸候国杞、缯联姻,周武王以太公望女为王后,并将长女太姬嫁给陈国。它反映了周初 A.
- 从上世纪90年代后期起,中国法律制度中开始逐渐建立起一些允许公众参与的制度,这种“开门立法”模式正在兴起,在一些与民众关
- 在《离骚》里有一个“香草美人”世界,请从课文里找出这些香花美草,并分析它们的作用。
- 下列反应中,电子转移方向和数目正确的是( )
- 阅读下文,回答问题。 给生命配乐 有时候走在街上,总想哼一种调子。不管是什么调子,也不管跑调不跑调,就是很随便地
- 阅读下文,完成23—题(10分) 子曰:“学而时习之,不亦说乎?有朋自远方来,不亦乐乎?人不知而不愠,不亦君子乎?” 子
- 假定英语课上老师要求同桌之间交换修改作文,请你修改你同桌写的以下作文。文中共 有10处错误,每句中最多有两处。错误涉及一
- 选出标点符号使用正确的一句 A.俗话说“到什么山唱什么歌”,又说“看菜吃饭,量体裁衣。”我们无论做什么事都要看情形办理,
- 读“某河流干流和流域范围示意图”(图15),回答37~38题。37.图中河流的甲—乙河段流域范围非常狭窄,其主要原因是A
- 写作 阅读下面的材料,根据要求作文。 女孩生下来就是唇腭裂,六岁时她发现了自己的“与众不同”。 女孩:“妈妈,我为什么与
- 同学们在观看体育节目时,经常看到黑人体育明星,如“飞人”乔丹、“拳王”泰森,虽然他们现在是美国人,但是他们的祖先是A.南
- 如图所示,物体A在水平推力F的作用下从甲图位置匀速运动到乙图位置。此过程中,物体A受到的摩擦力________水平推力F
- 工业上将Na2CO3和Na2S以1∶2的物质的量之比配成溶液,再通入SO2,可制取Na2S2O3,同时放出CO2。在该反
- (22分)阅读材料,回答问题。 材料一 刘邦接受了皇帝的称号,皇帝之下设三公九卿……地方行政系统仍是郡、县、乡、亭、里
- “我们不把任何未经验证的意见接受作为真理,而是遵照必要的次序,从一步推演到下一步……不论多么深奥,最终都能发现。”与这句



