化学反应的可逆性 知识点题库
工业制硫酸中一步重要的反应是:SO2在400~500℃的条件下进行催化氧化:2SO2+O2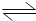 2SO3 , 其正反应为放热反应.如果该反应是在密闭容器中进行的,下述有关说法中错误的是( )
2SO3 , 其正反应为放热反应.如果该反应是在密闭容器中进行的,下述有关说法中错误的是( )
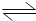 2SO3 , 其正反应为放热反应.如果该反应是在密闭容器中进行的,下述有关说法中错误的是( )
2SO3 , 其正反应为放热反应.如果该反应是在密闭容器中进行的,下述有关说法中错误的是( )
A . 使用催化剂是为了加快反应速率,提高生产效率
B . 在上述条件下,反应达平衡时容器中存在SO2、O2、SO3三种物质
C . 生产中一定要不断提供热量,使温度达到400~500℃
D . 达到平衡时,SO2的浓度与SO3的浓度可能相等
在密闭容器中于一定条件下进行下列反应:2SO2+O2⇌2SO3当到达平衡时通入18O2 , 再次平衡时,18O存在于( )
A . SO2、O2
B . SO2、SO3
C . O2、SO3
D . SO2、O2、SO3
已知298K时,合成氨反应N2(g)+3H2(g)═2NH3(g)(可逆反应)△H=﹣92.2kJ•mol﹣1 , 此温度下,将1mol N2和3mol H2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量(忽略能量损失) ( )
A . 一定大于92.2 kJ
B . 一定小于92.2 kJ
C . 一定等于92.2 kJ
D . 无法确定
若在一定条件下得到的尿素为固体,2NH3(g)+CO2(g)⇌CO(NH2) 2 (s)+H2O(g),开始在一密闭容器中充入0.1molNH3、0.65molH2O(g),保持温度不变,达到平衡时,混合气体的平均摩尔质量与起始相比 (填“变大”、“变小”或“不变”)
在一密闭容器中进行如下反应:2SO2(气)+O2(气)═2SO3(气),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L,0.1mol/L,0.2mol/L,当反应达平衡时,可能存在的数据是( )
A . SO2为0.4mol/L、O2为0.2mol/L
B . SO2为0.25mol/L
C . SO2、SO3均为0.15mol/L
D . SO3为0.4mol/L
已知299K时,合成氨反应 N2(g)+3H2(g)⇌2NH3(g)△H=﹣92.0kJ/mol,将此温度下的1mol N2和3mol H2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(忽略能量损失)( )
A . 一定大于92.0kJ
B . 一定等于92.0kJ
C . 一定小于92.0kJ
D . 不能确定
N2+3H2  2NH3 , 是工业上制造氮肥的重要反应.下列关于该反应的说法正确的是( )
2NH3 , 是工业上制造氮肥的重要反应.下列关于该反应的说法正确的是( )
 2NH3 , 是工业上制造氮肥的重要反应.下列关于该反应的说法正确的是( )
2NH3 , 是工业上制造氮肥的重要反应.下列关于该反应的说法正确的是( )
A . 增加N2的浓度能加快反应速率
B . 降低体系温度能加快反应速率
C . 使用催化剂不影响反应速率
D . 若反应在密闭容器中进行,N2和H2能100%转化为NH3
将0.1mol•L﹣1的KI溶液和0.05mol•L﹣1 Fe2(SO4)3溶液等体积混合后,取混合液分别完成下列实验,能说明溶液中存在化学平衡“2Fe3++2I﹣⇌2Fe2++I2”的是( )
实验编号 | 实验操作 | 实验现象 |
① | 滴入KSCN溶液 | 溶液变红色 |
② | 滴入AgNO3溶液 | 有黄色沉淀生成 |
③ | 滴入K3[Fe(CN)6]溶液 | 有蓝色沉淀生成 |
④ | 滴入淀粉溶液 | 溶液变蓝色 |
A . ①和②
B . ②和④
C . ③和④
D . ①和③
一定条件下,可逆反应X(g)+3Y(g)⇌2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),平衡时X、Y、Z的浓度分别为0.1mol•L﹣1、0.3mol•L﹣1、0.08mol•L﹣1 , 则下列判断正确的是( )
A . c1:c2的值不能确定
B . 平衡时,Y和Z的生成速率之比为1:1
C . 0.48mol•L﹣1<c1+c2+c3<0.56mol•L﹣1
D . c1的取值范围为0<c1<0.14 mol•L﹣1
在一定条件下的密闭容器中,加入 2molSO2和 1molO2 , 充分反应后能证明2SO2+O2 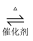 2SO3是可逆反应的事实是( )
2SO3是可逆反应的事实是( )
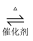 2SO3是可逆反应的事实是( )
2SO3是可逆反应的事实是( )
A . O2仍然为 1mol
B . 反应足够长时间后,速率变为零
C . SO2、O2和 SO3 同时存在
D . SO2完全转化为 SO3
对可逆反应2SO2+O2  2SO3 , 在混合气体中充入一定量的18O2 , 足够长的时间后, 18O原子()
2SO3 , 在混合气体中充入一定量的18O2 , 足够长的时间后, 18O原子()
 2SO3 , 在混合气体中充入一定量的18O2 , 足够长的时间后, 18O原子()
2SO3 , 在混合气体中充入一定量的18O2 , 足够长的时间后, 18O原子()
A . 只存在于O2中
B . 只存在于O2和SO3中
C . 只存在于O2和SO2中
D . 存在于O2、SO2和SO3中
下列对于可逆反应2A(g)+B(g)  2C(g) +3D(g)达到平衡时的说法正确的是( )
2C(g) +3D(g)达到平衡时的说法正确的是( )
 2C(g) +3D(g)达到平衡时的说法正确的是( )
2C(g) +3D(g)达到平衡时的说法正确的是( )
A . A,B全部转化成了C,D
B . 反应已经停止
C . 反应混合物中各组分的浓度不再改变
D . c (C)∶c(D)=2∶3
下列说法错误的是( )
A . 催化剂可以改变化学反应速率
B . 食物放在冰箱中会减慢食物变质的速率
C . 2mol SO2与1mol O2混合一定能生成2mol SO3
D . 锌与稀硫酸反应时,加入少量铜粉能加快产生氢气的速率
我们主要从三个方面讨论一个化学反应的原理,其中不属于这三个方面的是
A . 反应进行的方向
B . 反应的快慢
C . 反应进行的限度
D . 反应物的颜色
在一个密闭容器中发生反应:2SO2(g)+O2(g)  2SO3(g)。已知反应过程中的某一时间SO2、O2和SO3的浓度分别为:0.2mol/L、0.1mol/L和0.2mol/L。当反应达到平衡时可能存在的数据正确的是( )
2SO3(g)。已知反应过程中的某一时间SO2、O2和SO3的浓度分别为:0.2mol/L、0.1mol/L和0.2mol/L。当反应达到平衡时可能存在的数据正确的是( )
 2SO3(g)。已知反应过程中的某一时间SO2、O2和SO3的浓度分别为:0.2mol/L、0.1mol/L和0.2mol/L。当反应达到平衡时可能存在的数据正确的是( )
2SO3(g)。已知反应过程中的某一时间SO2、O2和SO3的浓度分别为:0.2mol/L、0.1mol/L和0.2mol/L。当反应达到平衡时可能存在的数据正确的是( )
A . c(O2)=0.2mol/L
B . c(SO2)=0.25mol/L
C . c(SO3)=0.4mol/L
D . c(SO2)=c(SO3)=0.15mol/L
在不同条件下,用O2氧化一定浓度的FeCl2溶液,其实验数据如图所示。下列说法错误的是( )
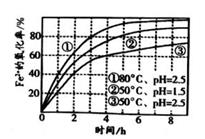
A . 实验过程中,溶液颜色逐渐加深
B . 由①和③可知,温度越高,Fe2+氧化越快
C . 由②和③可知,pH越大,Fe2+氧化越快
D . 温度低、pH小,有利于FeCl2溶液的保存
-
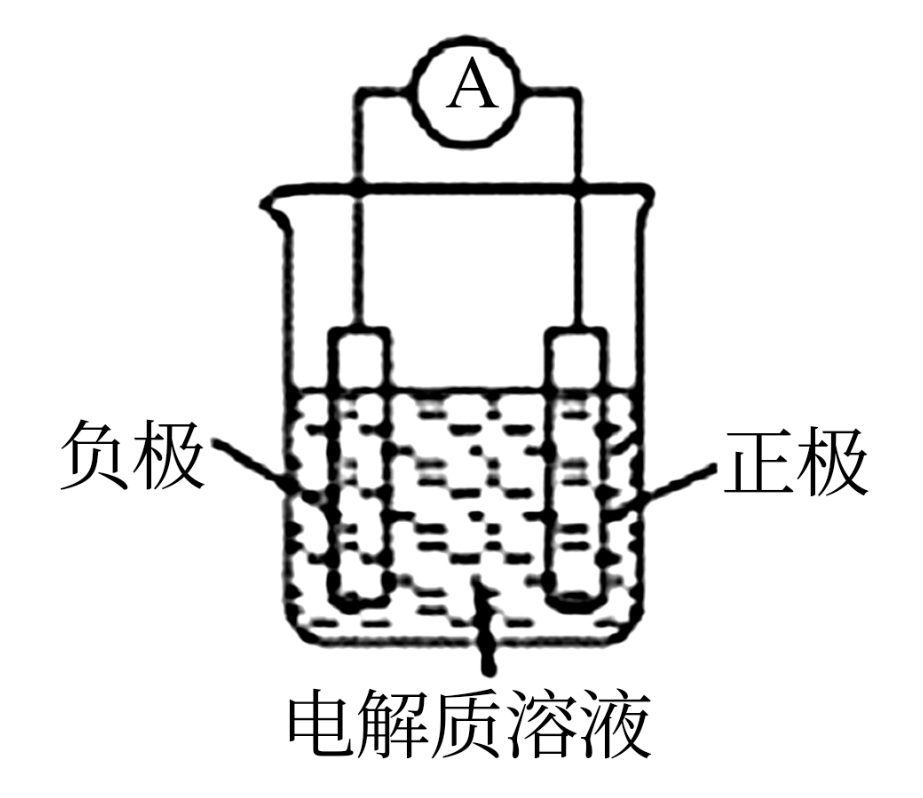
(1) 利用原电池装置可以验证Fe3+与Cu2+氧化性相对强弱,如图所示。写出该氧化还原反应的离子方程式:。该装置中的负极材料是(填化学式),正极反应式是。
-
(2) 某研究性学习小组为证明
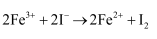 为可逆反应,设计如下两种方案(已知:酸性溶液中Fe2+易被空气氧化为Fe3+)。
为可逆反应,设计如下两种方案(已知:酸性溶液中Fe2+易被空气氧化为Fe3+)。方案一:取5mL0.1mol/LKI溶液,滴加2mL0.1mol/L的FeCl3济液,滴入5滴稀盐酸,再继续加入2mLCCl4 , 充分振荡、静置、分层,取上层清液,滴加KSCN溶液,现象是,即可证明该反应为可逆反应。你认为此方案(“不严密”或“严密”),理由是(用离子方程式表示)。
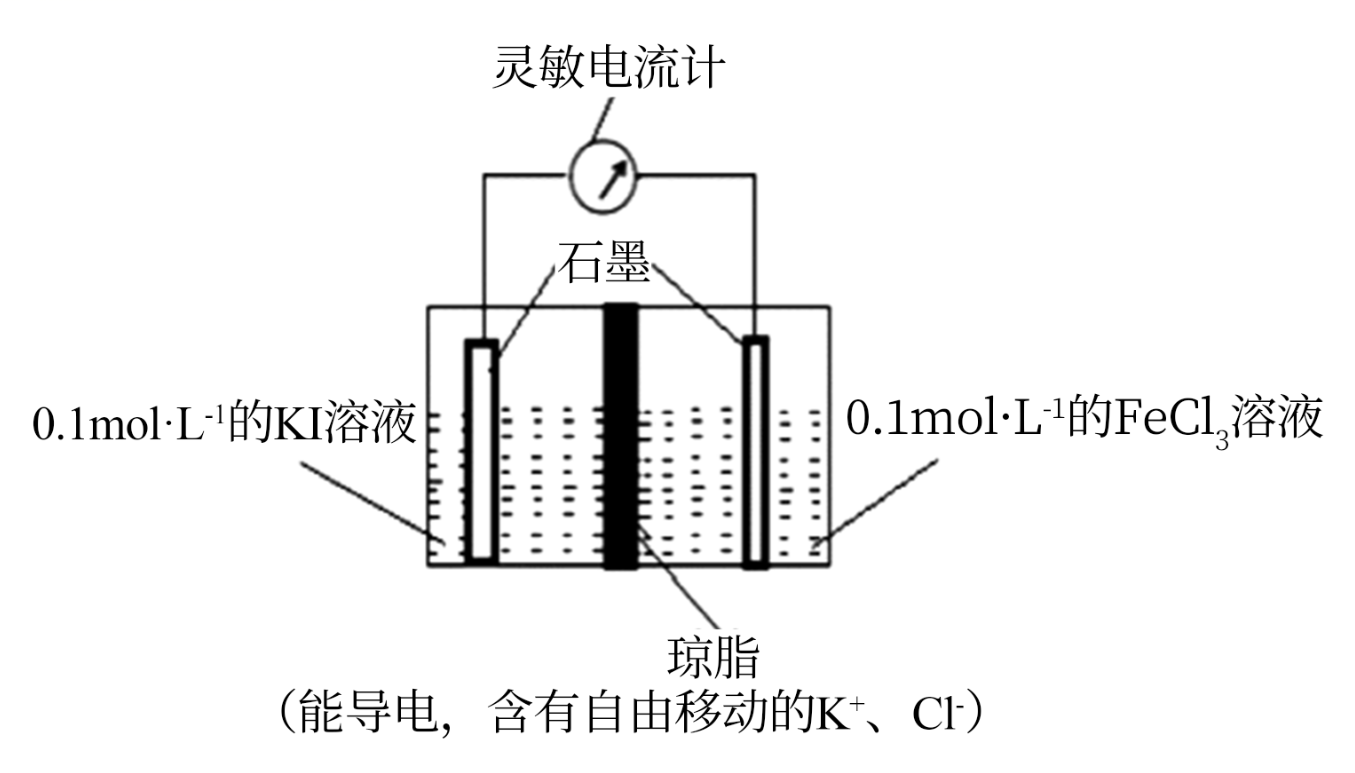
方案二:设计如图原电池装置,接通灵敏电流计,指针向右偏转,随着反应时间进行;电流计读数逐渐变小,最后读数变为零。当指针读数变零后,在右边的池了中加入1mol/L FeCl2溶液,灵敏电流计指针向左偏转,即可证明该反应为可逆反应。你认为灵敏电流计“读数变为零”的原因是。
2SO2+O2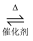 2SO3 ∆H<0。实验发现,一定条件下向一密闭容器中充入SO2和18O2 , 反应一段时间后,核素18O存在于SO2、O2、SO3中。下列分析不正确的是( )
2SO3 ∆H<0。实验发现,一定条件下向一密闭容器中充入SO2和18O2 , 反应一段时间后,核素18O存在于SO2、O2、SO3中。下列分析不正确的是( )
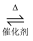 2SO3 ∆H<0。实验发现,一定条件下向一密闭容器中充入SO2和18O2 , 反应一段时间后,核素18O存在于SO2、O2、SO3中。下列分析不正确的是( )
2SO3 ∆H<0。实验发现,一定条件下向一密闭容器中充入SO2和18O2 , 反应一段时间后,核素18O存在于SO2、O2、SO3中。下列分析不正确的是( )
A . 18O2与O2的化学性质基本相同
B . 断裂2molSO2+1molO2中的共价键的能量小于断裂2molSO3中的共价键的能量
C . 化合反应与分解反应可同时发生,说明反应存在可逆性
D . 平衡时,18O2初始浓度c0(18O2)与平衡时各组分浓度c之间一定存在:2c0(18O2)=2c(S18O2)+3c(S18O3)+2c(18O2)
某温度下,恒容密闭容器中发生反应: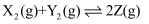 。已知
。已知 、
、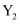 、Z的起始浓度分别为
、Z的起始浓度分别为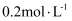 、
、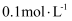 、
、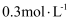 。一段时间后,反应达平衡时,各物质的浓度不可能是( )
。一段时间后,反应达平衡时,各物质的浓度不可能是( )
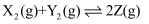 。已知
。已知 、
、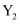 、Z的起始浓度分别为
、Z的起始浓度分别为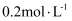 、
、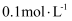 、
、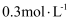 。一段时间后,反应达平衡时,各物质的浓度不可能是( )
。一段时间后,反应达平衡时,各物质的浓度不可能是( )
A . 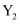 为
为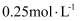 B .
B .  为
为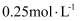 C .
C .  为
为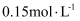 D . Z为
D . Z为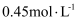
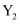 为
为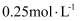 B .
B .  为
为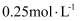 C .
C .  为
为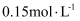 D . Z为
D . Z为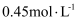
一定温度下,向2 L某恒容密闭容器中加入1 mol X气体和2 molY气体,发生如下反应: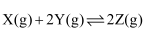 , 5 min时测得Z的物质的量为1.2 mol,下列说法正确的是( )
, 5 min时测得Z的物质的量为1.2 mol,下列说法正确的是( )
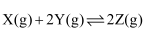 , 5 min时测得Z的物质的量为1.2 mol,下列说法正确的是( )
, 5 min时测得Z的物质的量为1.2 mol,下列说法正确的是( )
A . 此时Y的浓度为0.6 mol/L
B . 5 min内v(X)=0.06 mol/(L·min)
C . 容器内X、Y、Z的浓度之比为1:2:2,则该反应达到平衡状态
D . 单位时间消耗0.1 mol X同时生成0.2 mol Z,则该反应达到平衡状态
最近更新
- A harmonious society is like a symphony orchestra—each perso
- The busier he is,the he feels.
- 请认真阅读下面两篇文章,完成下列各题。(一)活在往事中①旧历小年第二天,正当人们忙着迎接春节的时候,我则坐在电脑前用冰凉
- 已知二次函数y=x2+x+ ,当自变量x取m时对应的值小于0,当自变量x分别取m-1、m+1时对应的函数值为y1、y2,
- It is necessary ___ me ___my studiesbefore a new term.A. for
- 液体温度计是根据测量液体____________的性质制成的,图示体温计的示数是____℃。
- 已知反应A+B=C+D,且A与B参加反应的总质量为20g,若反应后生成的C和D的质量比为2:3,则参加反应的C的质量为
- “大街小巷叫卖食品杂物的小贩吟叫百端,大小商店铺席连绵不断,夜市直至三更尽,五更又开晓市。”以下选项中最早出现上述现象的
- 人类的Down氏综合症(先天愚型)是21染色体引起的,一般不能生育后代,偶尔也可生育。如果两个患者婚配,其子女患病的概率
- “1914年至1918年的战争,从双方来说,都是帝国主义的(即侵略的、掠夺的、强盗的)战争。”这是列宁对下列哪次战争的
- 设a、b是两条不同的直线,α、β是两个不同的平面,则下列四个命题 ①若 ②若
- E市位于内蒙古西南部,自然资源丰富,以羊(羊毛和羊绒制品)、煤(煤炭)、土(稀土)、气(天然气)著称。根据下列材料,结合
- 阅读下面的文字,完成后面的题。 水力压裂法,我们应该知道的事情 北美非常规油气的大热,令其开采过程中最常使用的“水力压裂
- 上海世博会运行6个月来,上海宗教界以开放的心态服务广大境内外参展者和参观者的合理宗教生活需求。他们共设立44个世博接待宗
- 下列做法符合科学常识的是( )A.与灯泡串联的开关安装在火线上B.稀释浓硫酸时,把水直接倒入浓硫酸中C.用金属容器盛装
- 已知:,:,若是的充分不必要条件,则实数的取值范围是.
- c(N0048)相同的下列溶液①NH4Cl②(NH4)2SO4③NH4HSO4④NH4HCO3,其物质的量浓度由大到
- 如图4所示,一点电荷形成的电场中一条竖直电场线上有A、B两点,将某带电微粒从A点由静止释放,微粒沿电场线下落,到达B点时
- D Influenced by their families and society, many yout
- 阿拉伯数字的发明者是( )A 阿拉伯人 B 古埃及人 C 古印度人 D



