中和热的测定 知识点题库
-
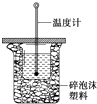
(1) 从实验装置上看,图中尚缺少的一种玻璃用品是;
-
(2) 用相同浓度和体积的醋酸代替稀盐酸溶液进行实验,求得的中和热数值(填“偏 大”、“偏小”或“无影响”);
-
(3) 实验中改用60mL 0.50mol/L 盐酸跟50mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量(填“相等”或“不相等”),所求中和热(填“相等”或“不相等”),简述理由.
-
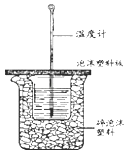
(1) 从实验装置上看,图中尚缺少的一种玻璃用品是
-
(2) 在实验过程中,该同学需要测定并记录的实验数据有 (填序号).A . 盐酸的浓度 B . 盐酸的温度 C . 氢氧化钠溶液的浓度 D . 氢氧化钠溶液的温度 E . 水的比热容 F . 反应后混合溶液的终止温度
-
(3) 中和反应,三次实验温度平均升高3.4℃.已知中和后生成的溶液的比热容为4.18J/(g•℃),酸与碱溶液的密度均为1g/cm3 . 通过计算可得中和热△H=
-
(4) 实验中改用60mL0.50mol•L﹣1盐酸跟50mL0.55mol•L﹣1NaOH溶液进行反应,与上述正确的实验操作相比,所放出的热量(填“相等”或“不相等”),所求中和热(填“相等”或“不相等”).
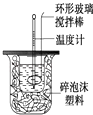
①用量筒量取50mL 0.25mol/L硫酸倒入小烧杯中,并测出其温度;
②用另一量筒量取50mL 0.55mol/L NaOH溶液,并测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液最高温度.
回答下列问题:
-
(1) 写出稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式(中和热数值为57.3kJ/mol):.
-
(2) 倒入NaOH溶液的正确操作是 .A . 沿玻璃棒缓慢倒入 B . 分三次少量倒入 C . 一次迅速倒入
-
(3) 实验数据如表:
①请填写下表中的空白:
温度
实验次数
起始温
度t1℃
终止温度t2/℃
温度差平均值
(t2﹣t1)/℃
H2SO4
NaOH
平均值
1
26.2
26.0
26.1
29.5
3
25.9
25.9
25.9
29.2
3
26.4
26.2
26.3
29.8
②近似认为0.55mol/L NaOH溶液和0.25mol/L硫酸溶液的密度都是1g/cm3 , 中和后生成溶液的比热容c=4.18J/(g•℃).则中和热△H=( 保留一位小数).
-
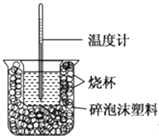
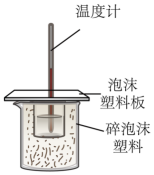
(1) 该图中有两处未画出,它们分别是、.
-
(2) 做一次完整的中和热测定实验,温度计需使用次.
-
(3) 把温度为13℃,浓度为1.0mol/L的酸溶液和1.1mol/L的碱溶液各50mL混合(溶液密度均为1g/mL),生成溶液的比热容c=4.184J/(g•℃),轻轻搅动,测得酸碱混合液的温度变化数据如下:
反应物
起始温度t1/℃
终止温度t2/℃
中和热
HCl+NaOH
13
19.8
△H1
HCl+NH3•H2O
13
19.3
△H2
①比较△H1和△H2的相对大小:△H1△H2(填“>”“<”或“=”).
②两组实验结果差异的原因是.
③写出HCl和NH3•H2O反应的热化学方程式:.
-
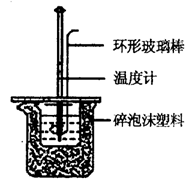
(1) 实验时使用环形玻璃棒搅拌溶液的方法是。不能用铜丝搅拌棒代替环形玻璃棒的理由。
-
(2) 向盛装稀盐酸的烧杯中加入NaOH溶液的正确操作是_________________________。A . 沿玻璃棒缓慢加入 B . 一次性迅速加入 C . 分三次加入
-
(3) 用一定浓度的盐酸和NaOH溶液测中和热为△H1 , 若将盐酸改为相同体积、相同浓度的醋酸,测得中和热为△H2 , 则△H1与△H2的关系为△H1△H2(填“<”“>”或“=”),理由是。
-
(1) 实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、0.5mol· L-1盐酸、0.55mol· L-1NaOH溶液,尚缺少的实验玻璃用品是、。
-
(2) 实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?(填“能”或“否”),其原因是。
-
(3) 他们记录的实验数据如下:
实验用品
溶液温度
中和热
△Ht1
t2
①
50mL0.55mol.L-1NaOH
50mL.0.5mol.L-1HCl
20℃
23.3℃
②
50mL0.55mol.L-1NaOH
50mL.0.5mol.L-1HCl
20℃
23.5℃
已知:Q=Cm(t2-t1),反应后溶液的比热容C为4.18KJ·℃-1· Kg-1 , 各物质的密度均为1g·cm-3。
①计算完成上表。△H=
②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式:
-
(4) 若用KOH代替NaOH,对测定结果(填“有”或“无”)影响;若用醋酸代替HCl做实验,对测定结果(填“有”或“无”)影响。
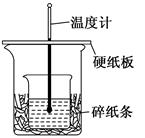
| A | B | C | D |
| | | | |
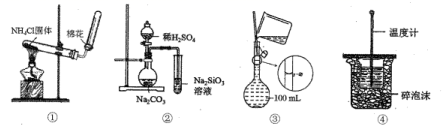
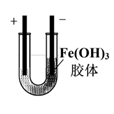
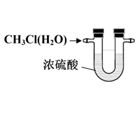
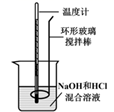
| 电泳实验证明Fe(OH)3胶体粒子带电 | 干燥一氯甲烷气体 | 排除盛有0.100 mol/L盐酸的滴定管中的气泡 | 测定酸碱中和反应的反应热 |
-
(1) 从如图实验装置可知,缺少的一种仪器名称是 。
-
(2) 在操作正确的前提下,提高中和热测定准确性的关键是。
-
(3) 若改用 60 mL 0.25 mol•L −1 H2SO4 和 50 mL 0.55 mol•L −1 NaOH 溶液进行反应,则比上述实验所放出的热量(填“多”或“少”),若实验操作均正确,最少需要测定 次温度。
-
(4) 写出用稀H2SO4 和稀氢氧化钠溶液的反应表示中和热的热化学方程式(中和热数值为 57.3kJ•mol −1): 。
-
(5) 某学生实验记录数据如下:
实验
起始温度 t1/℃
终止温度 t2/℃
序号
硫酸
氢氧化钠溶液
混合溶液
1
20.0
20.2
23.2
2
20.2
20.4
23.4
3
20.4
20.6
23.6
依据该学生的实验数据计算,该实验测得的中和热ΔH= (结果保留一位小数)
(已知稀溶液的比热容为 4.18J/(g•℃),稀溶液的密度 1g/cm3)。
-
(6) 上述实验数值结果与 57.3kJ•mol −1 有偏差,产生偏差的原因可能是 。
a.用温度计测定 NaOH 溶液起始温度后直接测定硫酸的温度
b.量取硫酸的体积时仰视读数
c.分多次把 NaOH 溶液倒入盛有硫酸的小烧杯中
d.实验装置保温、隔热效果差
-
(1) I.某实验小组在同样的实验条件下,用同样的实验仪器和方法步骤进行两组中和热测定的实验,实验试剂及其用量如表所示。
反应物
起始温度/℃
终了温度/℃
中和热/kJ•mol-1
酸溶液
NaOH溶液
①0.5mol•L-1HCl溶液50mL、0.55mol•L-1NaOH溶液50mL
25.1
25.1
ΔH1
②0.5mol•L-1CH3COOH溶液50mL、0.55mol•L-1NaOH溶液50mL
25.1
25.1
ΔH2
甲同学预计ΔH1≠ΔH2 , 其依据是。
-
(2) 若实验测得①中终了温度为28.4℃,则该反应的中和热ΔH1=(保留一位小数)(已知盐酸、NaOH溶液密度近似为1.0g·cm-3 , 比热容c=4.18×10-3kJ·g-1·℃-1)。
-
(3) 在中和热测定实验中,若测定酸的温度计未洗涤干燥就直接测量碱溶液的温度,则测得的中和热ΔH(填“偏大”“偏小”或“不变”)。
-
(4) Ⅱ.某化学小组为了研究外界条件对化学反应速率的影响,进行了KI溶液在酸性条件下与氧气反应的实验,记录实验数据如下:
实验编号
①
②
③
④
⑤
温度(℃)
30
40
50
60
70
显色时间(s)
160
80
40
20
10
该实验的原理:(用离子方程式表示)。
-
(5) 实验试剂除了1mol/LKI溶液、0.1mol/LH2SO4溶液外,还需要的试剂是,实验现象为。
-
(6) 上述实验操作中除了需要(2)的条件外,还必须控制不变的是___(填字母)。A . 温度 B . 试剂的浓度 C . 试剂的用量(体积) D . 试剂添加的顺序
-
(7) 由上述实验记录可得出的结论是。
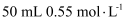 的NaOH溶液与
的NaOH溶液与 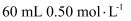 的盐酸反应,测得的中和热数值偏大
D . 在测定中和热实验中需要使用的仪器有:天平、量筒、烧杯、温度计、玻璃棒
的盐酸反应,测得的中和热数值偏大
D . 在测定中和热实验中需要使用的仪器有:天平、量筒、烧杯、温度计、玻璃棒
-
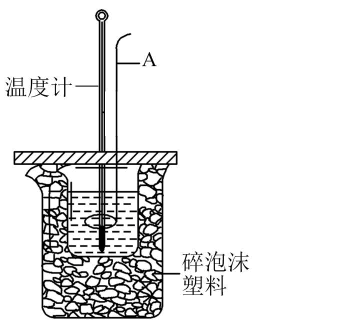
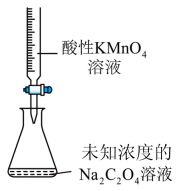
(1) 用50mL0.50
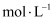 的盐酸与50mL0.55
的盐酸与50mL0.55 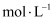 的NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中放出的热量可计算中和反应反应热。
的NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中放出的热量可计算中和反应反应热。 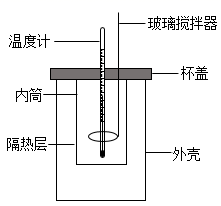
①若将杯盖改为薄铁板,求得的反应热
 将(填“偏大”、“偏小”或“无影响”)。
将(填“偏大”、“偏小”或“无影响”)。②实验时玻璃搅拌器的运动方向是。
a.上下运动b.左右运动c.顺时针运动d.逆时针运动
③若通过测定计算出产生的热量为1.42kJ,请写出该反应的热化学方程式:。
-
(2) 已知:
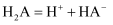 、
、  ,常温下,0.1
,常温下,0.1 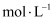 NaHA溶液的pH=2,则0.1
NaHA溶液的pH=2,则0.1 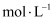
 溶液中
溶液中  的大小范围是;NaHA溶液中各离子浓度由大到小关系为。
的大小范围是;NaHA溶液中各离子浓度由大到小关系为。
-
(3) 一定条件下,在水溶液中所含离子
 、
、 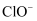 、
、  、
、  、
、 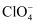 各1mol,其相对能量的大小如图所示(各离子在图中用氯元素的相应化合价表示),则反应
各1mol,其相对能量的大小如图所示(各离子在图中用氯元素的相应化合价表示),则反应  的
的 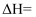
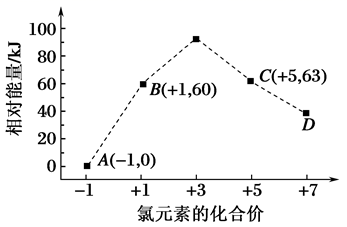
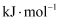 。
。 
A | B | C | D |
|
|
|
|
测定未知 | 探究铁的析氢腐蚀 | 配制0.10 mol/L NaOH溶液 | 中和热的测定 |
- 如图所示,工人师傅推动一台重300N的割草机,施加力F的大小为100N,方向斜向下与水平方向成α=370角(sin37°
- 丁二酮(C4H6O2)可用作糖果增香剂。下列关于丁二酮的说法中正确的是 A.丁二酮的相对分子质量86g B.丁二酮
- 下列各组离子在指定的溶液中,―定能大量共存的是 ①能使红色石蕊试纸变蓝的溶液中:K+、Na+、CO32-、NO3-、
- (9分)如图所示,已知电源电动势E=20V,内阻r=1Ω,当接入固定电阻R=4Ω时,电路中标有“3V,4.5W”的灯泡L
- 图甲中游标卡尺(游标尺上有20个等分刻度)读数为 cm。
- 2009年3月5日至13日,十一届全国人大二次会议在北京召开。回答下题。 今年“两会”期间,在网络媒体开展的“我有问题问
- 读90°E附近海平面气压图(单位:hPA.),回答以下气压最高值出现的纬度和气压值最低处的气压带名称分别是A.50°N、
- (1)25℃时,0.1 mol·L-1的HA溶液中c(H+)/c(OH-)=1010。请回答下列问题: ①HA是____
- 为了把陷在泥坑里的汽车拉出来,司机用一条结实的绳子把汽车拴在一棵大树上,开始时相距12 m,然后在绳的中点用400 N的
- 罗马法经历了一个复杂的发展历程,它从习惯法到成文法的转变从根本上说是适应了 A.维护平民利益的需要
- 按照所给文段的思路,仿照相应的句式,将文段补写完整。 曾几何时,在和暖的轻风中拥抱春天的温柔;曾几何时,________
- What the teachers really doubt is ______ this student will
- 对地球环境人口容量的叙述,正确的是 A、对地球环境人口容量的估计,共存在两种截然不同的观点 B、乐观者认为,未来人口不会
- 下列化学反应中属于有氧化物生成的化合反应的是 A.将二氧化锰加入过氧化氢溶液中 B.蜡烛
- A farmer once owned an oldmule(骡子). One day, the mule fellin
- 下列说法中正确的是()A.两个接触的物体之间一定有弹力作用B.一个物体静止在另一个物体上,他们之间可能有摩擦力作用 C.
- (四川省成都石室中学2010届高三10月月考) D George, when yourbig brother and y
- 下列实验事故处理的方法中,不正确的是( ) A.不慎把浓硫酸沾在手上,立即用干布拭去,再用水冲洗 B.不慎将浓碱沾
- 关于平型关战役属性的正确表述是 A.防御阶段配合正面战场的战役B.防御阶段敌后战场的战役 C.相持阶段配合正面战场的战役
- 下列句中加点的成语使用正确的一项是 A耸人听闻的药家鑫故意杀人案引起社会各界的广泛关注,它警示我们要切实加强对青少年的

 溶液的浓度
溶液的浓度


