含氮物质的综合应用 知识点题库
步 骤 | 现象 |
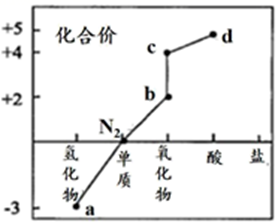
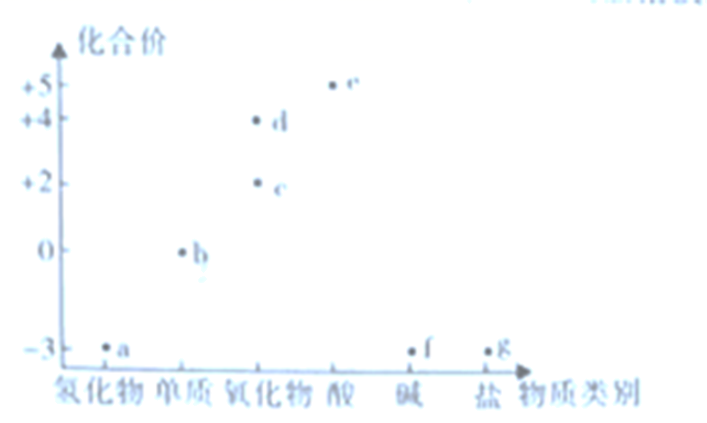
(1)其中e气体是有色的,其余气体均为无色,a、f是两种常见的大气污染物 | |
(2)a和b在常温下混合 | 气体变红棕色 |
(3)c和d混合 | 能产生白烟 |
(4)b、e、f分别通入氢硫酸中 | 都产生淡黄色浑浊 |
a、b、c、d、e、f依次可能是( )
-
(1) 以下操作可从智利硝石分离出NaNO3:溶解、
-
(2) 用NaNO3和浓硫酸反应可以制取硝酸,反应的化学方程式为 ;热的硝酸会腐蚀橡胶,制取装置中应该用
-
(3) )分离出的NaIO3可通过以下反应制得I2:4NaIO3+10NaHSO3→7Na2SO4+3H2SO4+2I2+2H2O.简述从反应后得到的混合物中分离出I2的操作 .NaHSO3过多或过少,I2的产率都会降低,当NaIO3与NaHSO3的物质的量之比为1:2.6时,I2的产率为
-
(4) 智利硝石资源有限(曾引起过南太平洋战争),现在工业上制NaNO3主要采用化学合成的方法,涉及的工业制备有(请结合课本知识回答) 、制硝酸、 等;写出工业制硝酸的化学方程式
-
(1) 已知:CH4(g)+2O2(g)═CO2(g)+2H2O(1)△H=﹣890.3kJ•mol﹣1
N2(g)+O2(g)═2NO(g)△H=+180kJ•mol﹣1
CH4可用于脱硝,其热化学方程式为:CH4(g)+4NO(g)=CO2(g)+2N2(g)+2H2O(1),△H=.
-
(2) C2H4也可用于烟气脱硝.为研究温度、催化剂中Cu2+负载量对NO去除率的影响,控制其它条件一定,实验结果如图1所示.为达到最高的NO去除率,应选择的反应温度和Cu2+负载量分别是.
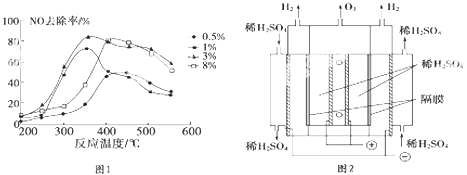
-
(3) 臭氧也可用于烟气脱硝.
①O3氧化NO 结合水洗可产生HNO3和O2 .
②一种臭氧发生装置原理如图2所示.阳极(惰性电极)的电极反应式为.
③将石墨电极设置成颗粒状的目的是.
-
(4) 如图3是一种用NH3脱除烟气中NO的原理.
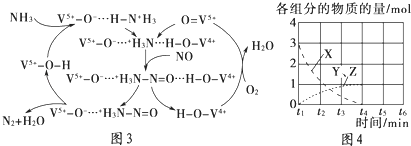
①该脱硝原理中,NO最终转化为(填化学式).
②当消耗2molNH3和0.5molO2时,除去的NO在标准状况下的体积为.
-
(5) NO直接催化分解(生成N2与O2)也是一种脱硝途径.在不同条件下,NO的分解产物不同.在高压下,NO在40℃下分解生成两种化合物,体系中各组分物质的量随时间变化曲线如图4所示.写出Y和Z的化学式:.
-
(6) NO2会污染环境,可用Na2CO3溶液吸收NO2并生成CO2 . 已知9.2g NO2和Na2CO3溶液完全反应时转移电子0.1mol,此反应的离子方程式是;恰好反应后,使溶液中的CO2完全逸出,所得溶液呈弱碱性,则溶液中存在的所有离子浓度大小关系是c(Na+)>.
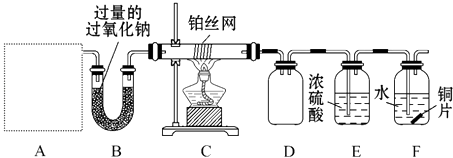
按上图连接好各仪器,检验装置气密性后,先将C处铂丝网加热至红热,再将A处产生的无色气体通入B装置,片刻后可观察到F中铜片表面有气泡产生.请回答下列问题:
-
(1) 若装置A中制取气体时限用一种试剂,则该试剂是(填字母).
a.NH4HCO3 b.NH4Cl c.Ca(OH)2 d.浓氨水
-
(2) C中发生反应的化学方程式为.
C处加热片刻后撤去酒精灯,铂丝仍保持红热,原因是.
-
(3) 若进入F装置的物质成分和质量一定,向F中加入下列物质中的(填字母)可使铜片溶解的质量增多.
a.Na2CO3 b.NaCl c.CuSO4 d.H2SO4
-
(4) 待实验结束后,将B中固体混合物溶于500mL 1.0mol•L﹣1的盐酸中,产生无色混合气体甲,溶液呈中性,则实验前B中原有Na2O2的物质的量是mol.
-
(5) 从安全与环保角度考虑,指出该装置中的两处明显缺陷,并提出修改建议:.
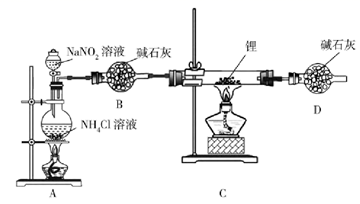
实验室用NH4Cl溶液和NaNO2溶液共热制备N2。
-
(1) 盛装NH4Cl溶液的仪器名称是。
-
(2) 安全漏斗中“安全”含义是。实验室将锂保存在(填“煤油”“石蜡油”或“水”)中。
-
(3) 写出制备N2的化学方程式。
-
(4) D装置的作用是。
-
(5) 测定Li3N产品纯度:取mg Li3N产品按如图所示装置实验。
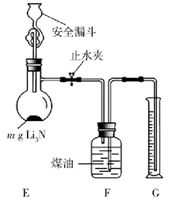
打开止水夹,向安全漏斗中加入足量水,当Li3N完全反应后,调平F和G中液面,测得NH3体积为VL(已折合成标准状况)。
①读数前调平F和G中液面的目的是使收集NH3的大气压(填“大于”“小于”或“等于”)外界大气压。
②该Li3N产品的纯度为%(只列出含m和V的计算式,不必计算化简)。若 Li3N产品混有Li,则测得纯度(选填“偏高”“偏低”或“无影响”)。
步骤1:在一支 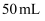 的注射器中充入
的注射器中充入 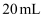 无色气体
无色气体  ,然后吸入
,然后吸入 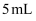 水,用乳胶管和弹簧夹封住管口,如题图所示。振荡注射器,无明显现象。
水,用乳胶管和弹簧夹封住管口,如题图所示。振荡注射器,无明显现象。
步骤2:打开弹簧夹,快速吸入少量  后夹上弹簧夹,气体变成红棕色。
后夹上弹簧夹,气体变成红棕色。
步骤3:振荡注射器,气体又变为无色,溶液仍无色。
下列说法不正确的是( )
![]()
 难溶于水
B . 步骤2中红棕色气体是
难溶于水
B . 步骤2中红棕色气体是  C . 步骤3中发生反应的氧化剂和还原剂的质量比为
C . 步骤3中发生反应的氧化剂和还原剂的质量比为 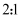 D . 重复步骤2、步骤3多次,可使
D . 重复步骤2、步骤3多次,可使  充分转化
充分转化
-
(1) 氮氧化物(以NO为主)直接排放到空气中会形成硝酸型酸雨,反应的化学方程式为。
-
(2) NH3催化还原NO的化学方程式为。
-
(3) 铁基催化剂在260~300℃范围内实现SCR技术的过程如下:
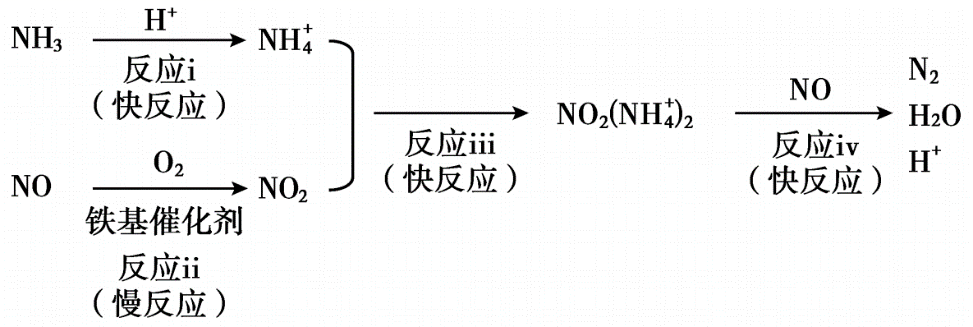
① 反应iv中消耗的NO2 (NH
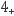 ) 2与NO的物质的量之比为。
) 2与NO的物质的量之比为。② 适当增大催化剂用量可以明显加快脱硝速率,结合上述过程解释原因:。
③ 向反应体系中添加NH4NO3可显著提高NO脱除率。原因如下:
NO
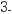 与NO发生反应NO
与NO发生反应NO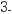 + NO = NO2 + NO
+ NO = NO2 + NO ;
;NO2与NH
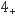 发生反应iii和反应iv转化为N2;
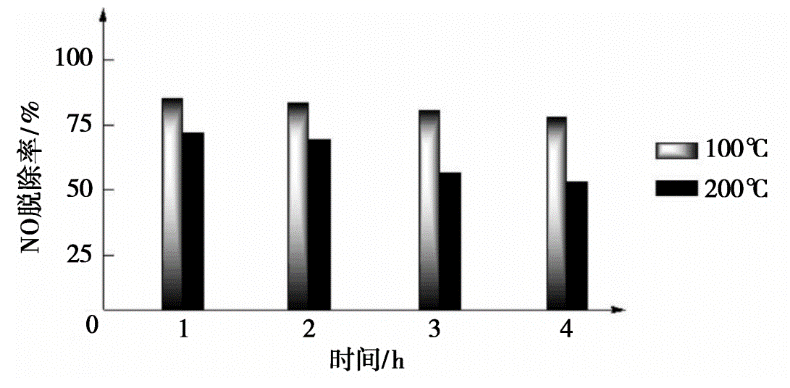
发生反应iii和反应iv转化为N2;NO
 与NH
与NH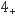 发生反应(填离子方程式)转化为N2。
发生反应(填离子方程式)转化为N2。 -
(4) 相比于铁基催化剂,使用锰基催化剂(活性物质为MnO2)时,烟气中含有的SO2会明显降低NO脱除率。
① 推测SO2与MnO2会发生反应使催化剂失效,其化学方程式是。
② 持续通入含SO2的烟气。不同温度下,每隔1 h测定NO脱除率,结果如下:
相同时间,200℃时NO脱除率低于100℃,原因是。
-
(1) I.研究氮的循环和转化对生产、生活有重要的价值。
写出实验室制备氨气的化学方程式:
-
(2) Ⅱ.氨是重要的化工原料。某工厂用氨制硝酸和铵盐的流程如下图所示,
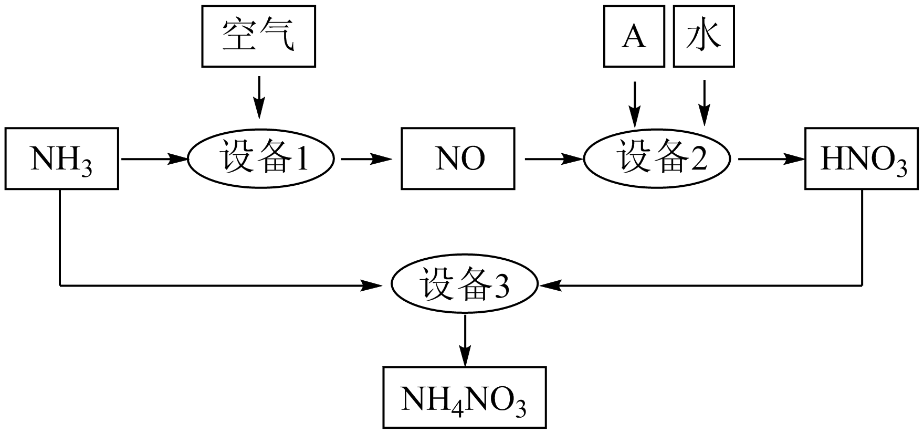
设备1中发生反应的化学方程式是;设备2中通入的物质A是。
-
(3) Ⅲ.氨氮废水的去除是当前科学研究的热点问题。氨氮废水中的氮元素多以和
 的形式存在。某工厂处理氨氮废水的流程如下:
的形式存在。某工厂处理氨氮废水的流程如下: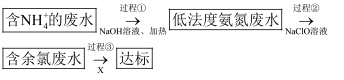
过程①的目的是将
 转化为
转化为 , 并通过鼓入大量空气将氨气吹出,写出
, 并通过鼓入大量空气将氨气吹出,写出 转化为
转化为 的离子方程式:
的离子方程式: -
(4) 过程②加入
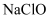 溶液可将氨氮物质转化为无毒物质,应后含氮元素,氯元素的物质化学式分别为、。
溶液可将氨氮物质转化为无毒物质,应后含氮元素,氯元素的物质化学式分别为、。
-
(5) 含余氯废水的主要成分是
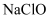 以及
以及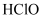 , X可选用以下哪种物质以达到去除余氯的目的(填字母),
, X可选用以下哪种物质以达到去除余氯的目的(填字母),a.
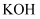 b.
b. c.
c.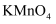 d.
d.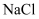
写出其中一个反应的离子方程式:
①农业生产中常使用的氮肥都是易溶于水的;②生产中使用的尿素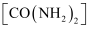 不属于有机物;③铵态氮肥可以与草木灰混合施用;④铵态氮肥在使用时宜深施盖土,避免受热;
不属于有机物;③铵态氮肥可以与草木灰混合施用;④铵态氮肥在使用时宜深施盖土,避免受热;
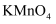 溶液中
溶液中
-
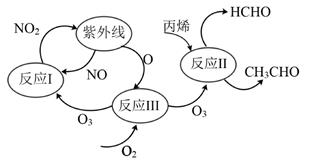
(1) 臭氧与空气中的氮氧化物和(填字母)在紫外线照射下产生光化学烟雾。
a.二氧化硫 b.碳氢化合物 c.二氧化碳
-
(2) 汽车排气管内的催化剂能将CO和
 转化为无害气体,发生的反应方程式为。
转化为无害气体,发生的反应方程式为。
-
(3) 工业上在催化剂作用下用
 还原废气中
还原废气中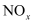 生成
生成 和
和 达到脱除目的,但当温度高于400℃时,
达到脱除目的,但当温度高于400℃时,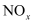 脱除率下降,原因可能是。
脱除率下降,原因可能是。
-
(4) 工业上氮的氧化物通常是用碱性溶液吸收。
①用
 溶液吸收硝酸工业尾气中的
溶液吸收硝酸工业尾气中的 , 生成等物质的量的两种钠盐(一种为
, 生成等物质的量的两种钠盐(一种为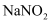 )及一种气体,反应的离子方程式为。
)及一种气体,反应的离子方程式为。②NaOH溶液浓度越大黏稠度越高,用不同浓度的NaOH溶液吸收
 (混有NO)含量不同的工业尾气,氮氧化物的吸收率随NaOH溶液浓度的变化如题图所示,曲线II表示NO的物质的量(填:“大于”、“小于”、“等于”)
(混有NO)含量不同的工业尾气,氮氧化物的吸收率随NaOH溶液浓度的变化如题图所示,曲线II表示NO的物质的量(填:“大于”、“小于”、“等于”) 物质的量:当NaOH溶液浓度高于
物质的量:当NaOH溶液浓度高于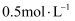 后,氮氧化物的吸收率随NaOH溶液浓度的升高而降低的原因是。
后,氮氧化物的吸收率随NaOH溶液浓度的升高而降低的原因是。
- 在―1叫做_________,运算的结果叫做__________.
- 可逆反应H2(g) + I2(g) 2HI(g)达到平衡的标志是( ) A. H2、I2、HI的浓度相等 B
- 已知热化学方程式:①CO(g)+ 1/2 O2(g)=CO2(g) ΔH=-283.0kJ·mol-1②H2(g)+1/
- 如图9四边形ABCD是菱形,且,是等边三角形,M为对角线BD(不含B点)上任意一点,将BM绕点B逆时针旋转得到BN,连接
- 关于历史上的“康乾盛世”,史学界对此基本上有两种评价:(一)从中国古代历史的纵向发展来看,值得颂扬。(二)从世界历史的横
- ;
- 已知满足约束条件当目标函数在该约束条件下取到最小值时,的最大值为 .
- 战国时期是我国封建社会的开端,其主要标志是( ) A、使用铁器和牛耕 B、封建土地私有制形成 C、
- 下列说法中正确的是 A. 电荷定向移动形成了电流B. 导体有电阻,绝缘体没有电阻C. 电动机把机械能转化为电能D.
- 分解因式: .
- 如图, 一固定斜面上两个质量相同的小物块A和B紧挨着匀速下滑, A与B的接触面光滑. 已知A与斜面之间的动摩擦因数是B与
- 有“高原之舟“之称的畜种是( ) A、蒙古马 B、骆驼 C、驴 D、牦牛
- 我国首部禁毒法于2008年6月1日起开始实施。历史上,国际联盟把虎门销烟开始的6月3日定为“国际禁烟日”。1987年联合
- 我国南海海底蕴藏着丰富的锰结核——含有锰、铁、铜等金属的矿物。已知锰原子的核内质子数为25,相对原子质量为55,则锰原子
- 通过核裂变产生核能可以用于发电,是一种常用的核燃料,下列说法错误的是( ) A.的中子数比质子数多51
- 某市某社区拟选拔一批综合素质较强的群众,参加社区的义务服务工作.假定符合参加选拔条件的每个选手还需要进行四轮考核,每轮设
- 1861年俄国改革之前,工业资本家30%是农奴身份,财产随时有可能被地主侵占。这一现象反映的本质问题是 A.俄国的资本主
- 表2为某省四类不同等级城市提供的货物和服务情况统计表(“∨”表示该城市具有该项职能)。读表完成10-11题。类 型
- 设,则
- 正比例函数的图像与反比例函数的图像交于点M(a,1),轴于点N(如图),若的面积等于2,求这两个函数的解析式。



