氯气的实验室制法 知识点题库
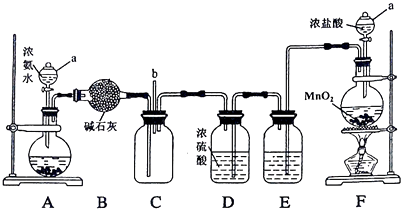
①用药匙向烧瓶中加入浓盐酸,再向分液漏斗中装入MnO2粉末;②用酒精灯直接加热烧瓶;
③需检查装置的气密性;④多余氯气用NaOH溶液吸收;⑤可用装有碱石灰的干燥管干燥氯气.
请回答下列问题:
-
(1) 仪器a的名称为;装置A的圆底烧瓶中盛放的固体物质可选用(填序号).
a.氯化钠 b.氢氧化钠 c.碳酸钙
-
(2) 装置F的圆底烧瓶中发生反应的离子方程式为;装置E的洗气瓶中盛放的试剂为,其作用是.装置D中浓硫酸的作用是.
-
(3) 反应过程中,装置C的集气瓶中有大量白烟产生,另一种产物为空气的主要成分之一,该反应的化学方程式为.
-
(4) 从装置C的b处逸出的尾气中含有少量Cl2 , 为防止其污染环境,可将尾气通过盛有溶液的洗气瓶.
-
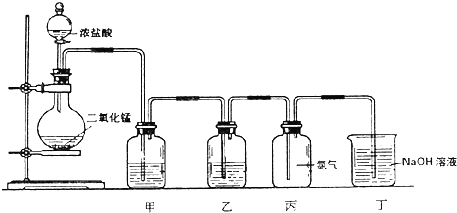
(1) 该实验装置中还缺少的仪器及用品是;.
-
(2) 为除去Cl2中混有的水蒸汽和氯化氢气体,洗气瓶甲和乙中分别盛放下列哪种溶液(填序号):甲,乙
A.浓H2SO4 B.饱和食盐水 C.澄清石灰水 D.淀粉KI溶液
-
(3) 丁装置的作用是,反应的离子方程式是.
-
(4) 烧瓶中发生反应的化学方程式是.
-
(5) 若要检验集气瓶丙的瓶塞处是否密封好,可用湿润的淀粉碘化钾试纸进行检测,若漏气,试纸变色,反应的离子方程式是.
 5Cl﹣+ClO3﹣+3H2O,请回答下列问题:
5Cl﹣+ClO3﹣+3H2O,请回答下列问题: 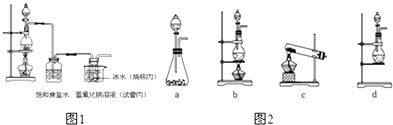
-
(1) 连接好装置,装药品之前,必须进行的一项操作步骤是.
-
(2) 圆底烧瓶内发生反应的化学方程式为;大试管内发生反应的离子方程式为.
-
(3) 饱和食盐水的作用是;冰水的作用是.
-
(4) 在制取Cl2时,实验室中若无MnO2 , 可用KMnO4粉末代替,发生下列反应:2KMnO4+16HCl(浓)═2MnCl2+2KCl+5Cl2↑+8H2O,则可选择的发生装置是(填序号).
-
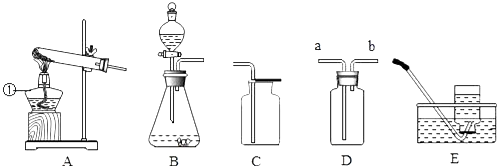
(1) 图中仪器①的名称是.
-
(2) 实验室用氯酸钾和二氧化锰的固体混合物制取氧气,反应的化学方程式为加热时试管口应略向下倾斜的原因是.请写出实验室制氧气的另外两个方程式
-
(3) 通常情况下,硫化氢气体是一种无色有臭鸡蛋气味的有毒气体,密度比空气大,能溶于水,其水溶
液叫氢硫酸(H2S).实验室用硫化亚铁固体与稀硫酸反应制取硫化氢气体时,应选择的发生装置为
(填字母),若用D装置收集该气体,气体应从(填“a”或“b”)端通入.为了防止中毒和污染空气,多余的硫化氢气体可用氢氧化钠溶液吸收,其反应的化学方程式为(氢硫酸跟稀盐酸一样,能与碱发生中和反应).
甲 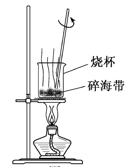 乙
乙 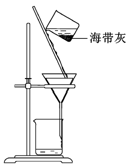
丙  丁
丁 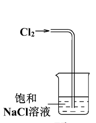
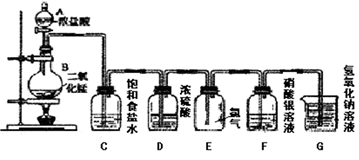
 用装置甲制取少量Cl2
B .
用装置甲制取少量Cl2
B . 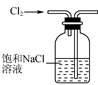 用装置乙除去Cl2中的HCl
C .
用装置乙除去Cl2中的HCl
C . 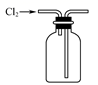 用装置丙收集Cl2
D .
用装置丙收集Cl2
D . 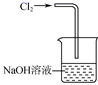 用装置丁吸收尾气
用装置丁吸收尾气
-
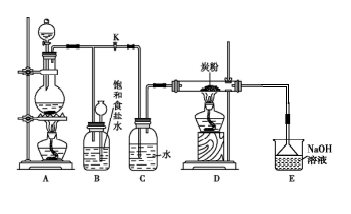
(1) A是氯气发生装置,其中发生反应的离子方程式为。
-
(2) 实验开始时,先点燃A处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃D处酒精灯,Cl2通过C瓶后再进入D。D装置的硬质玻璃管内盛有炭粉,发生氧化还原反应,其产物为CO2和HCl。则该反应的化学方程式为。
-
(3) E装置这样设计的目的是防倒吸,除了防倒吸之外还有的作用是。
-
(4) D处反应完毕后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有Cl2产生,则B的作用是。
-
(5) 若实验中使用12mol· L-1的浓盐酸10mL与足量的MnO2反应,则生成的Cl2的物质的量总是小于0.03mol,试分析可能存在的原因是。
-
(6) 某同学用如图的装置来验证氯气的有关性质:
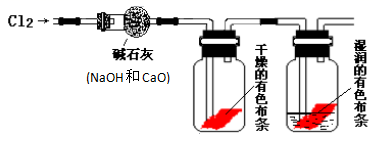
①该同学实验后并没有得到预期的实验现象,请你帮助他分析实验失败的原因。
②该同学在实验失败后对设计的实验装置进行了改进,并重新进行了实验,结果得到了预期的实验现象。你认为他预期的实验现象是,由此得出Cl2使有色物质褪色的机理是。
 与浓盐酸在常温下能反应产生
与浓盐酸在常温下能反应产生  。若用如图所示的实验装置来制备纯净、干燥的氯气,并与金属反应。每个虚线框表示一个单元装置,其中有错误的是( )
。若用如图所示的实验装置来制备纯净、干燥的氯气,并与金属反应。每个虚线框表示一个单元装置,其中有错误的是( ) 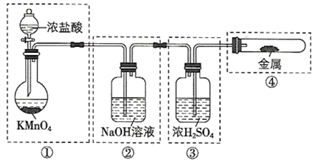



-
(1) ①储氯钢瓶中应贴的标签为(填字母代号)
A.易燃品 B.有毒品 C.爆炸品
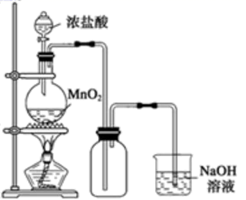
②实验室中常用MnO2氧化浓盐酸的方法制取氯气,实验装置如图a所示。
a:
 b:
b: 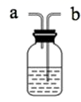
用此法值得的氯气中含有HCl和水蒸气,通常通过盛有、的洗气瓶,可以得到纯净、干燥的氯气。
③Cl2是有毒气体,为了防止多余Cl2污染空气,需要上图b装置进行尾气处理,用化学方程式表示该原理。气体应该由(填a或b)管通入。若要吸收标准状况下224mlCl2 , 至少需要1mol/L的上述溶液mL。
-
(2) ①工业上制取漂白粉的化学方程式是。
②瓶装漂白粉久置空气中会呈稀粥状而失去漂白作用。试用化学方程式表示漂白粉在空气中易失效的原因是。
③将Cl2制成漂白粉的主要目的是。
A.增强漂白能力和消毒作用
B.使它转化为较稳定物质,便于保存和运输
C.使它转化为较易溶于水的物质
D.提高氯的质量分数,有利于漂白消毒
-
(3) 同学们探究84消毒液在不同pH下使红纸褪色的情况,做了如下实验。
将5mL市售84消毒液稀释100倍,测得稀释后溶液的pH=12,将稀释后溶液各20mL分别加入a、b、c三个洁净的烧杯中:
烧杯
溶液的pH
现象
a
10
10min后,红纸基本不褪色;4h后红纸褪色
b
7
10min后,红纸颜色变浅;4h后红纸褪色
c
4
10min后,红纸颜色比b烧杯中10min后的浅;4h后红纸褪色
已知溶液中Cl2、HClO和ClO-的物质的量分数(a)随溶液pH变化的关系如图所示:
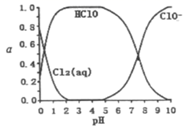
①由实验现象可获得结论:溶液的pH在4~10范围内,pH越大,红纸褪色(填“越快”或“越慢”)。
②结合图像进行分析,b、c两烧杯中实验现象出现差异的原因是。
 制取氯气并探究氯气性质,设计了如图所示的实验装置:
制取氯气并探究氯气性质,设计了如图所示的实验装置: 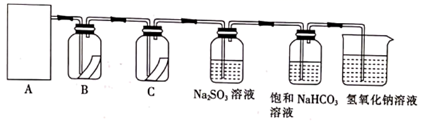
-
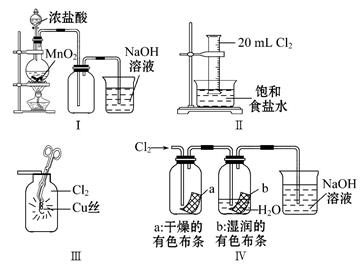
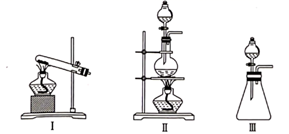
(1) 从装置I、Ⅱ、Ⅲ中选择合适的制氯气的装置( A处):( 填标号)。
-
(2) 装置B、C中依次放的是干燥的红色布条和湿润的红色布条实验过程中该同学发现装置B中的布条也褪色,其原因可能是;说明该装置存在明显的缺陷,请提出合理的改进方法。
-
(3) 验证氯气的氧化性:将氯气通入
 溶液中,氯气可将
溶液中,氯气可将  氧化成
氧化成  。写出该反应的化学方程式:。
。写出该反应的化学方程式:。
-
(4) 氯气通入饱和
 溶液中能产生无色气体已知酸性:盐酸>碳酸>次氯酸。( 强酸可以制弱酸)该实验证明氯气与水反应的生成物中含有( 填“盐酸”或“次氯酸”)。
溶液中能产生无色气体已知酸性:盐酸>碳酸>次氯酸。( 强酸可以制弱酸)该实验证明氯气与水反应的生成物中含有( 填“盐酸”或“次氯酸”)。
-
(5) 实验装置中烧杯内氢氧化钠溶液的作用是。
 的说法中,正确的是( )
的说法中,正确的是( )
 是一种无色、无味、无毒的气体
B .
是一种无色、无味、无毒的气体
B .  能使湿润的红色布条褪色
C .
能使湿润的红色布条褪色
C .  在
在  中燃烧,生成的产物为
中燃烧,生成的产物为  D . 实验室用加热分解
D . 实验室用加热分解 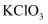 的方法制取
的方法制取
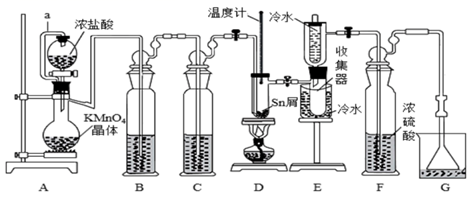
已知:①Sn、SnCl2、SnCl4有关的物理性质如下表:
| 物质 | 熔点/℃ | 沸点/℃ | 颜色、状态 |
| Sn | 232 | 2260 | 银白色固体 |
| SnCl2 | 246 | 623 | 无色晶体 |
| SnCl4 | -30 | 114 | 无色液体 |
②在空气中极易水解生成SnO2·xH2O。
请回答下列问题:
-
(1) 仪器a的名称为,其导管的作用是。
-
(2) 装置A中制备Cl2的离子方程式为。
-
(3) 装置B中的试剂为。
-
(4) 装置E的作用是。
-
(5) 下列关于实验装置的说法正确的是___________。A . 当观察到装置F上方出现黄绿色气体时才开始点燃酒精灯 B . 装置G的作用是吸收多余的氯气,故可选用Ca(OH)2 C . 整套实验装置先检漏,再连接,再添加药品,最后检查气密性 D . 锡熔化后可以适当增大氯气流量,继续加热
-
(6) 某同学想将装置F和G简化,可用(填仪器名称和药品)来替代。
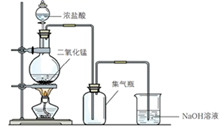
-
(1) 二氧化锰与浓盐酸反应制备氯气的化学方程式是。
-
(2) [提出猜想]ⅰ.随着反应进行,c(Cl-)降低,不能被二氧化锰氧化
ⅱ.随着反应进行,……
[进行实验]将反应后的固液混合物倒出,平均分在2个试管中,分别进行以下实验,证实了猜想ⅰ不成立。
序号
实验操作
实验现象
Ⅰ
将湿润的淀粉碘化钾试纸放置于试管口,加热试管;_,充分振荡,继续加热
试纸未变蓝
Ⅱ
将湿润的淀粉碘化钾试纸放置于试管口,加热试管;滴入2滴浓硫酸,充分振荡,继续加热
滴入浓硫酸前,试纸不变蓝;滴入浓硫酸后,试纸变蓝
将Ⅰ中操作补充完整:。
-
(3) II中试纸变蓝说明试管中的反应产生了(填化学式)。
-
(4) [进一步实验]设计如下实验进一步探究。
序号
实验装置
实验操作
现象
Ⅲ
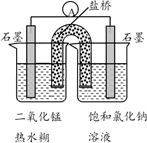
向左侧烧杯中滴加2滴浓硫酸
滴加浓硫酸前,电流表指针不偏转;滴加浓硫酸后,电流表指针偏转
Ⅳ
向右侧烧杯中滴加2滴浓硫酸
电流表指针始终不偏转
滴加浓硫酸后,左边烧杯中反应的电极反应式是。
-
(5) 依据实验Ⅰ-Ⅳ,解释“二氧化锰仍有剩余时就观察到反应停止”的原因是。
-
(6) [新的探究]小组同学又进行了实验Ⅴ、Ⅵ。
序号
实验操作
实验现象
Ⅴ
在0.5g二氧化锰中加入2毫升5%双氧水
产生气泡
Ⅵ
在0.5g二氧化锰中滴加2滴浓硫酸,再加入2毫升5%双氧水
产生气泡,黑色固体消失,生成无色溶液
Ⅵ中反应的离子方程式是。
-
(7) 结合依据实验Ⅰ-Ⅳ得出的结论,解释Ⅴ、Ⅵ中现象不同的原因。
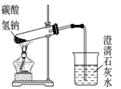 B . 检验过氧化钠与水反应的产物之一
B . 检验过氧化钠与水反应的产物之一 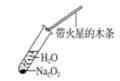 C . 除氯气中的氯化氢气体
C . 除氯气中的氯化氢气体 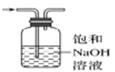 D . 测新制氯水的pH 值
D . 测新制氯水的pH 值 
FeCl3是棕红色固体,易潮解,在300℃以上可升华成含二聚三氯化铁( ![]() )分子的气体。可用于金属刻蚀,污水处理等。主要有以下制备方法:
)分子的气体。可用于金属刻蚀,污水处理等。主要有以下制备方法:
方法①:氯化法。以废铁屑和氯气为原料,在立式反应炉里反应,生成的氯化铁蒸气和尾气由炉的顶部排出,进入捕集器冷凝为固体结晶。
方法②:熔融法。将铁屑和干燥氯气在低共熔混合物(如30%KCl与70%FeCl3混合)内进行反应生成氯化铁,升华后收集在冷凝室中,该法制得的氯化铁纯度高。
方法③:复分解法。用氧化铁与盐酸反应后得到氯化铁溶液。
方法④:氯化亚铁合成法。将铁屑溶于盐酸中,然后向其中通入氯气得到氯化铁。
-
(1) 实验室模拟方法①制备FeCl3的装置如下图所示,下列说法不正确的是( )
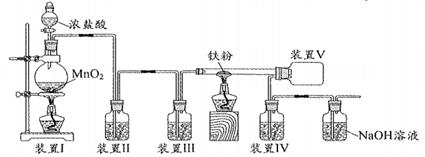 A . 装置Ⅰ反应的离子方程式为
A . 装置Ⅰ反应的离子方程式为 B . 装置Ⅱ洗气瓶中加入饱和氯化钠溶液除去Cl2中的少量HCl
C . 装置Ⅳ洗气瓶中盛放的液体为浓盐酸
D . 装置Ⅴ的作用是收集FeCl3
B . 装置Ⅱ洗气瓶中加入饱和氯化钠溶液除去Cl2中的少量HCl
C . 装置Ⅳ洗气瓶中盛放的液体为浓盐酸
D . 装置Ⅴ的作用是收集FeCl3
-
(2) 关于有关说法正确的是( )A . 二聚三氯化铁分子中含有配位键 B . 将FeCl3饱和溶液缓慢滴入氢氧化钠溶液中,可制取Fe(OH)3胶体 C . 直接加热蒸干方法③所得的氯化铁溶液制备无水氯化铁 D . 向方法④所得的溶液中加入KSCN溶液与氯气,检验该溶液中是否含有Fe2+
-
(3) 关于铁及其化合物的性质与用途具有对应关系的是( )A . Fe具有还原性,可用作抗氧化剂 B . Fe3O4具有磁性,可用于炼铁 C . Fe(OH)3胶体呈红褐色,可用于净水 D . FeCl3溶液呈酸性,可用于刻蚀铜板
回答下列问题:
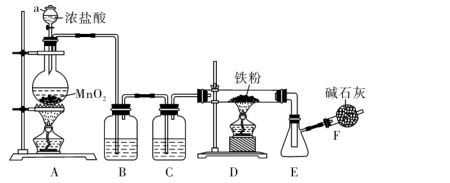
-
(1) 仪器a的名称是;装置B的作用是,C中盛装试剂是。
-
(2) 装置A中发生反应的离子方程式为。
-
(3) 装置D与E之间用较粗的导气管连接,原因是;点燃装置D处酒精灯时应先将空气排尽,原因是。
-
(4) 装置F的作用是。
-
(5) 与甲组设计对比,乙组同学去掉了装置C(其它操作不变)。实验时无论怎样改变铁粉的用量,装置D中都有少量的黑色固体残留。乙组同学猜测该黑色固体可能是,其依据是(用化学方程式表示)。
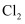 的实验,不能达到相应实验目的的是( )
的实验,不能达到相应实验目的的是( )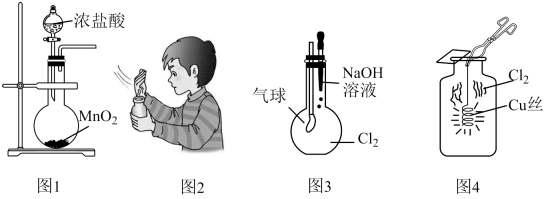
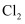 B . 用图2所示方法闻
B . 用图2所示方法闻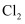 的气味
C . 用图3装置检验
的气味
C . 用图3装置检验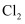 与
与 溶液是否反应
D . 用图4装置观察
溶液是否反应
D . 用图4装置观察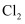 与
与 反应的现象
反应的现象
- Shannon will continue tobother you with phone calls _____ y
- 当物体克服重力做功时,物体的 ( ) A.重力势能一定减少,机械
- 椭圆中心在原点,焦点在x轴上,e=,它与直线x+y+1=0交于P、Q两点,以PQ为直径的圆过原点,求椭圆方程.
- 下列配搭错误的一项是 A、《论语》—孔子 B、大一统—汉景帝 C、地动仪—张衡 D、“医圣”—张仲景
- 在此次表彰大会上,在讲话中指出,我们一定要在全社会大力弘扬劳模精神,这是因为( ) ①优秀文化能丰富人的精神世界
- 鸦片战争改变了中国历史正常的发展历程,最主要体现在中国 A、革命任务发生变化 B、社会性质发生变
- (08年惠州一中二模理) 已知点,(1)求F的方程。(2)若A、B是F上的不同两点,O是坐标原点,求
- 小明在做种子的萌发实验时,在4个玻璃瓶中各放入2张餐巾纸,并在纸上均匀的放10粒完好的大豆种子.然后小明对4只瓶子做了不
- —I ‘m dying _________ a cup of hot tea, it’s so cold. —OK, c
- 2008年5月8日9点17分,奥运火炬传递队员成功登顶,奥运火炬首次到达世界最高峰珠穆朗玛峰。据此回答珠穆朗玛峰南坡的垂
- 下列图标中属于消防安全标志的是A.①②B.③④⑤C.①③⑤D.②④
- 读陆地海洋比例图,回答下题。下列有关陆地和海洋的叙述,正确的是 A.地球上最大的一块陆地是美洲大陆 B.此图说明地球上三
- 己知反应:①Cl2+2KBr=2KCl+Br2,②KClO3+6HCl=3Cl2↑+KCl+3H2O。据此判断下列说法正
- 从下面的描写段中找出两出表现香菱学诗如痴如醉的细节。(4分) 各自散后,香菱满心中还是想诗。至晚间对灯出了一回神,至三更
- X、Y、Z、E、F为五种短周期元素,原子序数依次递增。X+只含有一个质子;Y的正、负化合价绝对值相等,在同族元素中其氢化
- 数列{an}的前n项和为Sn=1-an(n∈N*).(1)判断数列{an}是否为等差或等比数列;(2)求数列{an}的前
- 下列生物除()外,都是由细胞构成的. A. 海带 B. 流感病毒 C. 向日葵 D. 蜜蜂
- 减数分裂四分体时期的细胞中,每个染色体与其DNA分子数之比是( ) A.l∶2 B.l∶4 C.l∶8
- 工业上常用铁质容器盛装冷浓酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:[探究一](1)将已去除表
- 小红家5月1日和6月1日电能表记数器上的示数分别如图8甲、乙所示,则小红家一个月用电 度。若每度电的费用0



