常用仪器及其使用 知识点题库
(1)做过碘升华实验的烧杯 .
(2)长期存放过三氯化铁溶液的试剂瓶 .
(3)盛过苯酚的容器
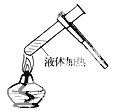 给液体加热
B .
给液体加热
B . 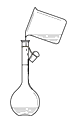 转移溶液
C .
转移溶液
C . 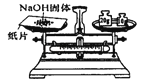 称取NaOH固体
D .
称取NaOH固体
D . 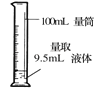 量取液体
量取液体
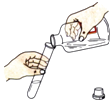 倾倒液体
B .
倾倒液体
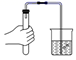
B . 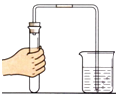 检查气密性
C .
检查气密性
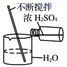
C . 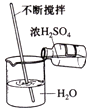 稀释浓硫酸
D .
稀释浓硫酸
D .  取用固体
取用固体
现实验室欲制取Na2S2O3·5H2O晶体(Na2S2O3·5H2O的相对分子质量为248)
步骤如下:
①称取12.6g Na2SO3于烧杯中,溶于80.0mL水。
②另取4.0g硫粉,用少许乙醇润湿后,加到上述溶液中。
③(如图所示,部分装置略去),水浴加热,微沸,反应约1小时后过滤。
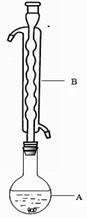
④滤液在经过..........、...........后析出Na2S2O3·5H2O晶体。
⑤进行减压过滤并干燥。
-
(1) 仪器B的名称是,其作用是,加入的硫粉用乙醇润湿的目的是。
-
(2) 步骤④应采取的操作是、。
-
(3) 滤液中除Na2S2O3和可能未反应完全的Na2SO3外,最可能存在的无机杂质是。如果滤液中该杂质的含量不很低,其检测的方法是: 。
-
(4) 为了测产品的纯度,称取7.40g 产品,配制成250mL溶液,用移液管移取25.00mL于锥形瓶中,滴加淀粉溶液作指示剂,再用浓度为0.0500mol/L的碘水,用(填“酸式”或“碱式”)滴定管来滴定(2S2O32- + I2 = S4O62- + 2I-),滴定结果如下:
滴定次数
滴定前读数(mL)
滴定后读数(mL)
第一次
0.30
30.52
第二次
0.36
31.06
第三次
1.10
31.28
则所得产品的纯度为,你认为影响纯度的主要原因是(不考虑操作引起误差)。
-
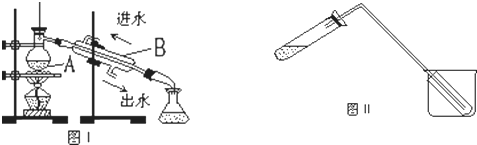
(1) 图Ⅰ是实验室制取蒸馏水的常用装置,仪器A、B的名称分别是:A、B;
-
(2) 温度计水银球应置于;
-
(3) 实验时A 中除加入一定量的自来水外,还需加入少量,其作用是;
-
(4) 图Ⅱ装置也可用于少量蒸馏水的制取(加热及固定仪器略),其原理与图I完全相同,该装置中使用的玻璃导管较长,其作用是。
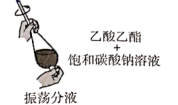
| 选项 | 实验目的 | 实验设计 |
| A | 除去乙酸乙酯中的乙酸 | |
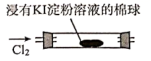
| B | 证明氧化性:Cl2>I2 | |
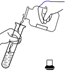
| C | 用NaOH标准溶液滴定某稀盐酸 | |
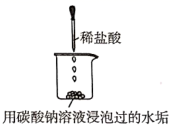
| D | 探究锅炉里的水垢样品在酸中的溶解 | |
回答下列问题:
-
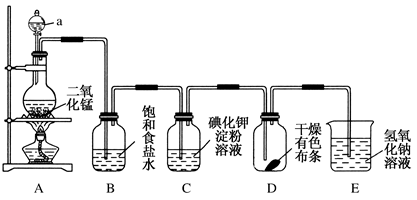
(1) 装置A中,仪器a的名称叫,该仪器中盛放的试剂为,写出A装置发生反应的离子方程式:。
-
(2) 装置B的作用是。
-
(3) 当有少量Cl2通过后,观察到装置C中溶液变成色。
-
(4) 当Cl2持续通过时,装置D中干燥的有色布条能否褪色?为什么?,。
-
(5) 若要证明Cl2无漂白性,则必须在装置D之前加一个。
-
(6) 装置E的作用是,该反应的离子方程式为。
-
(7) 家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。某品牌消毒液包装上说明如下。
注意事项:
1.本品对棉织品有漂白脱臼作用,对金属制品有腐蚀作用。
2.密封保存,请勿与洁厕灵同时使用。
3.保质期为一年。
消毒液与洁厕灵不能同时使用,原因是(用离子方程式表示)。
-
(1) I.研究小组用炼铁厂的铁矾渣制备FeCO3 , 铁矾渣主要含有K2Fe6(SO4)4(OH)12、ZnO、Fe2O3及少量的CaO、MgO、 SiO2 等。
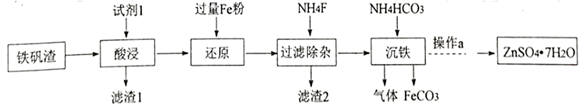
试剂1是过量的,滤渣 2的成分是 (写化学式);
-
(2) “沉铁”发生反应的离子方程式是;
-
(3) 沉铁后的滤液经“操作a”,再经过“过滤、 洗涤、干燥”得到皓矾(ZnSO4·7H2O),“操作a”是,取28.70g皓矾(ZnSO4·7H2O)加热,剩余固体的质量变化如图,100℃时所得固体的化学式。
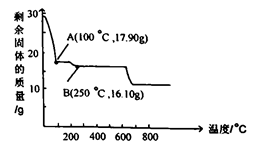
-
(4) II.研究小组又采用如下装置制取FeCO3 (C后及夹持装置略)。操作的关键是向Na2CO3溶液(pH=12.11)通入一段时间CO2至溶液pH为7,再滴加一定量FeSO4溶液,产生白色沉淀。
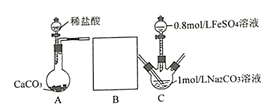
画出装置B,B中所用试剂为;
-
(5) 先向1mol/L Na2CO3溶液中通入CO2的目的是;
-
(6) FeCO3溶于乳酸[CH3CH(OH)COOH]能制得可溶性乳酸亚铁补血剂,该实验小组用KMnO4测定补血剂中亚铁含量进而计算乳酸亚铁的质量分数,发现乳酸亚铁的质量分数总是大于100%,其原因是(不考虑操作不当引起的误差)。
-
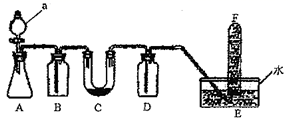
(1) a的名称。
-
(2) A是实验室中制取CO2的装置。写出A中发生反应的离子方程式:。
-
(3) 填写如表中的空白。
装置序号
加入的试剂
加入该试剂的目的
B
饱和NaHCO3溶液
D
-
(4) 写出C中发生反应的化学方程式:。
-
(5) F中得到气体的检验方法。
-
(6) 为了测定某碳酸钠样品的纯度,完成如下实验:在电子天平上准确称取三份灼烧至恒重的无水Na2CO3样品(杂质不与盐酸反应)0.4000g于250mL锥形瓶中,用50mL水溶解后,加2~3滴作指示剂,然后用0.2000mol•L-1HCl标准液滴定,滴定终点的实验现象为。已知:Na2CO3与HCl的滴定反应为Na2CO3+2HCl═2NaCl+H2O+CO2↑,滴定时实验数据列表如表:
实验次数编号
0.2000mol•L-1HCl溶液的体积(mL)
滴定前刻度
滴定后刻度
1
1.00
31.50
2
5.00
34.50
3
7.00
42.50
选取上述合理数据,计算出碳酸钠样品的纯度为。

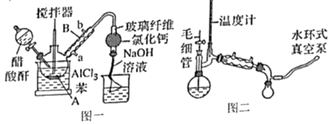
(实验步骤)
步骤一:向装有10mL分液漏斗、机械搅拌装置和回流装置(上端通过氯化钙干燥管与氯化氢气体吸收装置相连)的100mL仪器A中迅速加入13g(0.097mol)粉状无水三氯化铝和16mL(约14g,0.18mol)无水苯。在搅拌下将4mL(约4.3g,0.04mol)醋酸肝自分液漏斗慢慢滴加到A(先加几滴,待反应发生后再继续滴加),控制醋酸的滴加速度以使A稍热为宜。加完后(约10min),待反应稍和缓后在沸水浴中搅拌回流,直到不再有氯化氢气体逸出为止。
步骤二:反应结束,将A中的液体倒入冷水中,经处理得到较纯净的苯乙酮。
步骤三:经称重苯乙酮产量约为4.1g,计算产率。
已知在常压下:
| 名称 | 分子质量 | 颜色晶型 | 熔点 | 沸点 | 密度 | 溶解度 |
| 醋酸酐 | 102 | 无色液体 | -73 | 140 | 1.082 | 与水反应 |
| 苯 | 78 | 无色液体 | 5.5 | 80.5 | 0.879 | 不溶 |
| 苯乙酮 | 120 | 无色液体 | 20.5 | 202 | 1.0281 | 微溶 |
-
(1) 图一装置中仪器A名称是。
-
(2) 图一装置中漏斗一半扣在水面下、一半露在水面上的原因是。
-
(3) 制备过程中为什么要逐渐地滴加醋酸酐?。
-
(4) 图一装置中CaCl2的作用是。
-
(5) 步骤二为得到较纯净的苯乙酮,需要经过下列的操作:①蒸馏收集某温度下的馏分;②依次用10%的NaOH溶液、水洗分液;③用无水MgSO4干燥并过滤;④水层用苯萃取合并有机层;⑤分液。正确的顺序是___(填字母代号)。A . ⑤④②③① B . ⑤②③④① C . ②④⑤①③ D . ②④⑤③①
-
(6) 本实验为收集产品用了减压蒸馏装置,如图二所示。装置中温度计水银球的位置是否正确?(“是”或“否”)。收集产品,需要控制一定温度,可能是(填字母代号)。
A.202℃B.220℃C.175℃
-
(7) 经计算,该反应的产率为(保留两位有效数)。
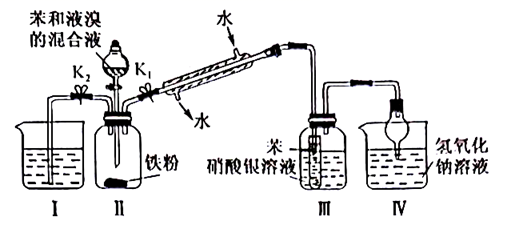
回答下列问题:
-
(1) 图中有存在 1处不正确,请指出:。
-
(2) 装置IV中使用倒立干燥管的作用是。
-
(3) 反应结束后,打开K2 , 关闭K1和分液漏斗活塞使装置I中的水倒吸人装置Ⅱ中,这样做的目的是。
-
(4) 写出装置Ⅱ中发生的有机反应的化学方程式: ,反应类型为,通过该实验能证明此反应类型的实验现象为。
| 编号 | ① | ② | ③ | ④ |
| 操作示 意图 | | | | |
| 操作名称 | 倾倒液体 | 取用块状固体 | 稀释浓硫酸 | 检查气密性 |
 和
和 的形式存在,其总铬含量的测定方法如下。
的形式存在,其总铬含量的测定方法如下。步骤一:取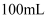 废水,加热浓缩成
废水,加热浓缩成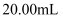 溶液,然后加入
溶液,然后加入 溶液将
溶液将 转化为
转化为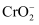 ;
;
步骤二:加入稍过量的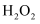 , 使
, 使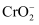 在碱性条件下转化成
在碱性条件下转化成 ;
;
步骤三:加入硫酸酸化并煮沸后,加入足量的碘化钾将六价铬还原为 , 同时生成单质
, 同时生成单质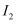 ;
;
步骤四:加入指示剂用 溶液滴定,滴定过程中消耗
溶液滴定,滴定过程中消耗 溶液
溶液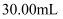 。
。
已知: , 请回答下列问题:
, 请回答下列问题:
-
(1) “步骤三”中加硫酸酸化时存在反应
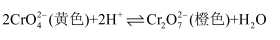 , 则该反应平衡常数的表达式为
, 则该反应平衡常数的表达式为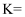 。升高溶液的温度会导致溶液黄色加深,则该反应的
。升高溶液的温度会导致溶液黄色加深,则该反应的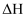 0(填“>”或“<”)。
0(填“>”或“<”)。
-
(2) 若“步骤三”省略加热煮沸操作会导致废水中铬元素含量的测量结果(填“偏高”、“偏低”或“无影响”)。
-
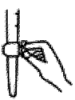
(3) “步骤四”中加入的指示剂为,盛装
 溶液的滴定管,滴定前排气泡时,应选择如图中的(填选项字母);滴定终点时的现象为。
溶液的滴定管,滴定前排气泡时,应选择如图中的(填选项字母);滴定终点时的现象为。a.
 b.
b. c.
c.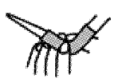 d.
d.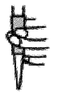
-
(4) 硫代硫酸钠晶体(
 )不溶于乙醇,可用作纸浆漂白时的脱氯剂等。用工业硫化钠(主要成分
)不溶于乙醇,可用作纸浆漂白时的脱氯剂等。用工业硫化钠(主要成分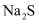 , 含少量
, 含少量 )及纯碱等为原料制备
)及纯碱等为原料制备 的流程如下:
的流程如下:
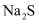 溶液中
溶液中
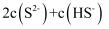 (填“>”、“<”或“=”),“反应”过程中体系
(填“>”、“<”或“=”),“反应”过程中体系 过小产品产率降低的原因是(用离子方程式表示),提纯
过小产品产率降低的原因是(用离子方程式表示),提纯 时,应用洗涤。
时,应用洗涤。
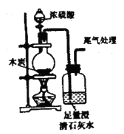 验证木炭和浓硫酸反应生成
验证木炭和浓硫酸反应生成 B .
B . 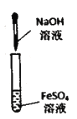 实验室制备
实验室制备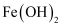 并能较长时间观察到白色固体
C .
并能较长时间观察到白色固体
C . 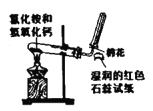 实验室制备和收集氨气并验满
D .
实验室制备和收集氨气并验满
D . 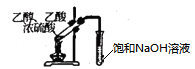 制备乙酸乙酯
制备乙酸乙酯
请回答下列问题:
-
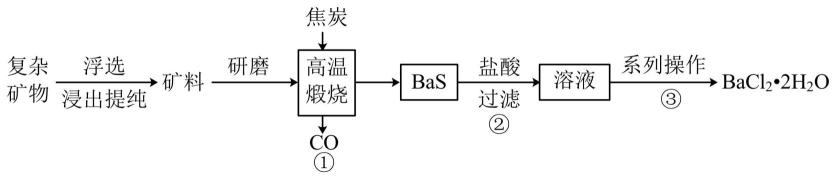
(1) 复杂矿物的主要成分为
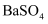 , 还含有少量
, 还含有少量 、
、 , 若采用稀硫酸进行浸出提纯,其中发生反应的离子方程式是,提纯后的矿料进一步研磨的目的是。
, 若采用稀硫酸进行浸出提纯,其中发生反应的离子方程式是,提纯后的矿料进一步研磨的目的是。
-
(2) 步骤①中
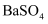 与焦炭反应的化学方程式为;实际生产中必须加入过量的焦炭,其主要目的是。
与焦炭反应的化学方程式为;实际生产中必须加入过量的焦炭,其主要目的是。
-
(3) “系列操作”是指蒸发浓缩、、、洗涤、干燥;其中在实验室中进行蒸发浓缩,除用到酒精灯、三脚架外,还需用到的仪器有。
- 右图为“地球圈层构成示意图”,图中所示的圈层A、B、C分别为 A.大气圈、水圈、生物圈 B.生物圈、大气圈、水圈
- 一位同学这样描述自己的考前情况:“每次考试前几周,我就开始担心自己考不好,总是睡不好觉。尤其是考试前几天,除了不能入睡以
- 如图3-11,金属杆ab的质量为m,长为L,通过的电流为I,处在磁感应强度为B的匀强磁场中,结果ab静止且紧压于水平导轨
- 我国所处的温度带有( ) A .北温带 北寒带 B.北温带 热带 C.南温带 热带
- 下列各句中,加点的成语使用恰当的一句是 () A.今年春节期
- 已知铜和浓硫酸可以在加热条件下发生如下反应(反应方程式已配平): Cu+2H2SO4(浓)CuSO4+A↑+2H2O 试
- 某学生做浓硫酸性质的实验:在一支试管中放入一块很小的铜片,再加入2mL浓硫酸,然后把试管固定在铁架台上。把一小条蘸有品红
- 函数 的自变量x的取值范围是 。
- 中东位于“五海三洲”之地,其中三洲是( ) A、亚洲、北美洲、欧洲 B、亚洲、非洲、欧洲 C、亚洲、非
- 朝核问题引发了国际关注,核问题的关键是核能的如何利用。已知某种核原料的原子核中含有1个质子和2个中子,那么( ) A
- 如图1-3-6所示,两根长度均为L的细线下端拴一质量为m的小球,两线间夹角为α,今使摆球在垂直线面的平面内做小幅度振动,
- 氧化汞受热分解生成汞和氧气的反应前后,发生改变的是()A. 元素种类 B. 原子种类 C. 分子种类 D. 原子数目
- 有关南极洲的叙述,不正确的是 A.极端恶劣的气候条件,使南极洲生物资源相当贫乏 B.11月至次年3月,是到南极洲考察的最
- 分析有关基因工程的资料,回答问题。 下表中列出了几种限制酶识别序列及其切割位点,圈l、圈2中箭头表示相关限制酶的酶切位点
- 在兴奋的产生和传导过程中,发生了机械刺激(或其他刺激)转变为电信号、电信号转变成化学信号,以及化学信号转变为电信号等变化
- 《苏州风俗考》记载明代苏州纺织业情况是“郡城之东,皆习机业,工匠各有专能,匠有常主,计日受值。……若机户工作减,此辈衣食
- “黄金有价、玉无价”,某一种玉石的主要成份是NaAlSi2O6 , 下列说法正确的是( ) A. 其
- In the USA, _______ Thanksgiving Day is a harvest festival.T
- 如图,在▱ABCD中,∠ABC的平分线交AD于点E,延长BE交CD的延长线于F. (1)若∠F=40°,求∠A的度数;
- 根据下面的新闻材料,拟一条一句话新闻。(不超过25个字)(杭州网2012-03-12)昨天,杭州市环保局、共青团杭州市委