制取氧气的原理 知识点题库
根据图回答问题.

-
(1) 实验室用A制取氧气,反应的化学方程式是 ,还需补充的仪器是 .
-
(2) 实验室用Β制取二氧化碳,反应的化学方程式是 ,装置中要改正的是 , 将燃着的木条放在集气瓶口,若观察到 , 说明集气瓶中已充满二氧化碳.
-
(3) 将上述实验收集的一瓶气体倒扣在燃着的蜡烛上(如图C)所示,观察到蜡烛烛焰更加明亮,一段时间后逐渐熄灭,则集气瓶中原有的气体是 .
-
(4) D为探究燃烧条件的实验,其中热水作用是 , 反应的化学方程式是 .
请结合图示实验装置,回答下列问题.

-
(1) 写出有标号的仪器名称:① , ② .
-
(2) 用高锰酸钾制氧气选用的发生装置是 (选填序号),反应的化学方程式为 .
-
(3) 若B装置中固体为锌粒,试剂可制H2 . 要获得干燥的H2 , 应先将气体通过盛有的D装置,再用E装置收集,气体应从 端通入(选填“a”或“b”).
-
(4) 实验室可用B或C装置制CO2 , 反应的化学方程式为 ,C相对于B装置的优点有 .
-
(5) 若用F装置收集NH3 , 油层的作用是 .
实验室现有氯酸钾、二氧化锰和稀盐酸,以及下列仪器.

(1)若利用上述仪器和药品制取氧气,反应的化学方程式为 ,应补充的一种仪器是(填仪器名称).
(2)若补充一种药品(填名称),并利用上述仪器和药品制取二氧化碳,你选择的仪器是 (填字母),添加药品前应进行的操作是 .
如图是初中化学实验室常见气体的制取装置:

-
(1) 实验室制取氧气的原理之一是 (用化学方程式表示),此原理对应的发生装置是 (填序号〕.用D装置收集氧气,验满的方法是;
-
(2) 收集二氧化碳应选择的装置为 (填序号).理由是 , 欲收集一瓶干燥的二氧化碳,还需选用E装置,则E中应装入的药品是 .

-
(1) 实验开始前必须进行的操作是.
-
(2) 反应开始后,若G中出现红色,H中有白色沉淀生成,判断E、F中的物质可能是;.(填名称)
-
(3) 按基本反应类型写出该实验中有关反应的化学方程式:(装置用字母表示)
化合反应,发生在装置中;
分解反应,发生在装置中;
置换反应,发生在装置中.
归纳与演绎是重要的科学方法,也是常用的科学学习方法。下面是实验室制取气体的发生装置和收集装置:

-
(1) 我们已经学过实验室制取O2、H2、CO2三种气体的反应原理、制取与收集方法,请你归纳出实验室制取这三种气体反应的共同点 (填字母,可以多选)。
A . 需要加热 B . 需用催化剂 C . 没有气体参加反应 D . 生成的气体只有一种 -
(2) 某同学选用氯酸钾晶体和二氧化锰混合制氧气,请写出发生反应的化学方程式
该同学选择上述A装置作为制氧气的发生装置,他选择的理由是
-
(3)
该同学对“氧气的性质实验”进行了微型化改进。打开A止水夹,关闭B止水夹,给氧储气罐充满氧气。实验开始时,关闭A止水夹,打开B止水夹,氧储气罐由于自身重力缓慢下降而排出氧气,在M中完成氧气性质的各个实验。实验现象明显且可以持续较长时间,是由于。

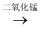 水+氧气
B . 氯酸钾
水+氧气
B . 氯酸钾  氯化钾+氧气
C . 水
氯化钾+氧气
C . 水 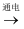 氧气+氢气
D . 氧化汞
氧气+氢气
D . 氧化汞  汞+氧 气
汞+氧 气
 B .
B .  C .
C .  D .
D . 

| 实验1 | 实验2 | |
| MnO2的质量/g | 0.5 | 0.5 |
| 5%H2O2溶液的体积/mL | 40 | 待填 |
| 水浴温度/℃ | 20 | 80 |
下列有关实验中的说法错误的是( )
-
(1) 过氧化钙晶体可用下列方法制备:CaCl2+H2O2+NH3+H2O→CaO2·xH2O↓+NH4Cl。
用如图1制取装置制备过氧化钙晶体。

①装置A中生成的气体为;仪器X的名称为。
②装置C采用冰水浴控制温度在0℃左右,可能的原因主要有:
Ⅰ.该反应是放热反应,温度低有利于 ,有利于提高CaO2·xH2O产率;
Ⅱ.该反应是放热反应,温度低可避免过氧化氢受热分解变质而影响晶体的生成。
-
(2) 为确定过氧化钙晶体的组成,某化学兴趣小组查资料发现:过氧化钙晶体受热时会先失去结晶水,然后再分解成氧化钙和氧气,于是他们称取21.6克晶体用热分析仪对其进行热分解实验,并绘制成固体质量与温度关系图2,由此计算x=

-
(1) 用双氧水和二氧化锰代替原集气瓶里的水, 其优点除了使实验更简便外, 还有。
-
(2) 实验中可观察到到铁丝燃烧的现象是,并放出大量热,生成一种黑色固体,请写出该反应的化学方程式。

①用电子秤称量出整套装置的总质量为498.6g;
②在A、B、C三个仪器中装入药品(加入双氧水溶液质量为50g);
③关闭a处止水夹,打开A仪器的阀门,向锥形瓶中加入全部的双氧水溶液,随即关闭A仪器的阀门;
④第二次称量整套装置的总质量为497g;
⑤组装仪器,并检查装置的气密性;
⑥充分反应后,打开a处止水夹,向装置中持续缓慢地鼓入X气体;
-
(1) 在本实验采用的装置中,仪器A的名称是。
-
(2) 正确的实验步骤为。
-
(3) 为尽可能减小测量误差,请结合测量原理判断,操作⑤中鼓入的X气体是 。A . CO2 B . 除去氧气后的空气 C . 氢气 D . 经干燥处理的空气
-
(4) 根据题意,计算双氧水溶液中溶质的质量分数,写出计算过程。
①将注射器活塞推至零刻度,按图连接装置,并检査装置的气密性。
②将质量分数为30%过氧化氢溶液调节成不同的pH值,待用。
③取pH=2质量分数为30%过氧化氢溶液6毫升加入分液漏斗中,.调节水浴的温度为60℃打开
分液漏斗的阀门,使过氧化氢溶液在恒温环境中分解:.
④30分钟后观察并记录注射器的刻度,即测出生成的氧气体积.
⑤分别取不同pH值不同 , 重复以上实验,各组数据绘制成图乙。

-
(1) 本试题中涉及过氧化氢(H2O2)分解的化学方程式;
-
(2) 补充完成操作步骤⑤;
-
(3) 实验中测定的氧气的体积比理论值要偏大些,其可能的原因是;
-
(4) 査阅资料,过氧化氢的分解还与容器的材料有关,请结合本实验数据和下列资料,说明实验室如何保存过氧化氢溶液。
材料
不锈钢
PP塑料
铁
铜
氧气体积/ml
282.2
0
69.4
520.6
(60℃时,6ml浓度为60%的过氧化氢分解30分钟所得的氧气)

请回答下列问题:
-
(1) 实验室用过氧化氢溶液和二氧化锰制取氧气,化学方程式为
-
(2) 实验室用过氧化氢溶液和二氧化锰制取氧气,若选用 C 做发生装置,你认为选用 C 的优点是;
-
(3) 欲使用装置 E 用排空气法收集氢气,则气体应从 (填“a”或“b”)端通入;
-
(4) 甲烷是最简单的有机物类的气体,实验室常用加热醋酸钠与氢氧化钠固体混合物来制得.实验室制取甲烷应选用的发生装置是(填序号)
【问题】为什么橡皮塞会突然弹飞呢?
【查阅资料】
①容器内瞬间产生气体过多,压强过大,可能导致橡皮塞弹飞。
②化学反应速率与反应物的溶质质量分数、接触面积、温度、催化剂等因素有关。
【猜想】
甲同学:导气管堵塞或弯折造成。
乙同学:过氧化氢溶液用量过多造成。
丙同学:过氧化氢溶液的溶质质量分数过大造成。
【分析验证】通过检查实验装置发现导气管没有堵塞、弯折的情况;与实验成功的小组交流,得知各小组所用过氧化氢溶液的溶质质量分数均相同。于是他们否定了(1)同学的猜想。请你设计实验,验证另一名同学的猜想是导致本次实验橡皮塞弹飞的主要原因。
|
实验步骤 |
实验现象 |
结论 |
|
取两支试管分别加入等质量的二氧化锰,再加入(2). |
的反应较剧烈 |
该同学的猜想正确 |
【交流反思】老师建议他们可以通过改进发生装置的方法,避免橡皮塞弹飞。请选择你觉得最合适的发生装置 。


求:
-
(1) 反应前溶液中的过氧化氢质量;
-
(2) 反应后溶液中的溶质质量分数。

如图1:铁丝能在氧气中燃烧,火星四射,剧烈燃烧,但没有火焰,因为是固体物质燃烧。
如图2:蜡烛在氧气中燃烧且有明亮的火焰。
针对这些问题,同学们进行实验,请你参与他们的实验探究。
-
(1) 写出实验室用过氧化氢溶液和二氧化锰制取氧气的化学方程式:。
-
(2) 点燃蜡烛,用坩埚钳夹持一根尖嘴玻璃管,将其末端插入燃着的蜡烛烛心附近,一段时间后用火柴在玻璃管尖嘴处点燃,有火焰产生(如图2所示)。由此可知,蜡烛燃烧产生的火焰是由(填“固态”或者“气态”)石蜡燃烧形成的。要使该实验成功,同学们认为尖嘴玻璃管不宜过长,原因是如果导气管过长石蜡蒸气会在导管中。
 B . 实验室加热高锰酸钾制取氧气
B . 实验室加热高锰酸钾制取氧气  C . 将水通电分解一段时间
C . 将水通电分解一段时间  D . 用等质量、等浓度的双氧水分别制取氧气
D . 用等质量、等浓度的双氧水分别制取氧气 
- The typewriter _______ all week. A. laying on the table, wer
- 统计表明,2010年二季度中国GDP超过日本,成为全球第二大经济体,但“第二大”并不等于“第二强”。从人均GDP看,中国
- 已知关于x的方程2x2-(+1)x+m=0的两根为sinθ和cosθ,θ∈(0,2π).(文)求m的值.(理)求方程的两
- —It’s very kind of you to have carried the luggage for me.
- 很多同学都尝试设计并制作生态瓶,但是有相当一部分同学的设计并不成功。下面罗列了设计生态瓶应遵循的原理,其中不合理的是 A
- 【甲】臣本布衣,躬耕于南阳,苟全性命于乱世,不求闻达于诸侯。先帝不以臣卑鄙,猥自枉屈,三顾臣于草庐之中,咨臣以当世之事,
- 下列句子中没有错别字且加点字的读音正确的一项是 A.尽管整个世界还是处于深刻的危机之中,但很多人已经在开始争论世界各国经
- 国务院决定自2009年1月1日起,增值税小规模纳税人的征收率统一由原来的6﹪的征收率降至3%。这说明 A.税收具有随意性
- 从圆外一点向这个圆作两条切线,则两切线夹角的余弦值为 A. B. C.
- 利用太阳光分解水制氢是未来解决能源危机的理想方法之一。某研究小组设计了如图1-2-21图所示的循环系统,实现光分解水制氢
- 某课外小组分别用下图所示装置对原电池和电解原理进行实验探究. 请回答:I.用图1所示装置进行第一组实验. (1)在保证电
- 增大压强,对已达平衡的下列反应产生的影响是 3Ag+Qg 2Rg+2Sg A
- Hedidn’t make _____ clear when and where the meeting would
- 已知函数上两点和,其中.过的直线与轴交于,那么( ) A.成等差数列 B.成等比数列 C.成等差数列
- 猪的卵原细胞中含有20对同源染色体,它产生的卵细胞中染色体有 A.10条 B.20条 C.40条 D.60条
- 如图,AB是圆O的直径,点C在圆O上,延长BC到D使BC=CD,过C作圆O的切线交AD于E.若AB=6,ED=2,求BC
- 有两种饱和一元醇的混合物18.8g,与13.8g Na充分反应,生成的H2在标准状况下的体积为5.6L,这两种醇分子中相
- 依次填入下列各句括号内的词语,最恰当的一项是①新规定将于明年一月一日开始 ,届时原规定将停止使用。②卫生部
- “张-烯炔环异构反应”被《Name Reactions》收录。该反应可高效构筑五元环化合物: (R、R‘、R“表示
- 下列物态变化过程中,属于液化现象的是( ) A.湿衣服变干了 B.夏天的早晨,草地上出现



