定量实验与探究实验 知识点题库
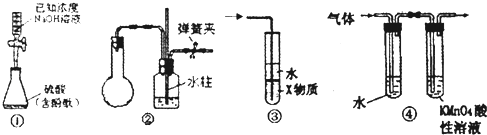
序号 | 硫酸的体积/mL | 锌的质量/g | 锌的性状 | 温度/ | 完全溶于酸的时间/s | 生成硫酸锌的质量/g |
1 | 50.0 | 2.0 | 薄片 | 25 | 100 | m1 |
2 | 50.0 | 2.0 | 颗粒 | 25 | 70 | m2 |
3 | 50.0 | 2.0 | 颗粒 | 35 | 35 | m3 |
4 | 50.0 | 2.0 | 粉末 | 25 | 45 | 5.0 |
5 | 50.0 | 6.0 | 粉末 | 35 | 30 | m4 |
6 | 50.0 | 8.0 | 粉末 | 25 | t6 | 16.1 |
7 | 50.0 | 10.0 | 粉末 | 25 | t7 | 16.1 |
-
(1) 化学反应速率本质上是由决定的,但外界条件也会影响反应速率的大小.本实验中实验2和实验3表明对反应速率有影响.
-
(2) 我们最好选取实验(填3个实验序号)研究锌的形状对反应速率的影响.我们发现在其它条件相同时,反应物间的反应速率越快.
-
(3) 若采用与实验1完全相同的条件,但向反应容器中滴加少量硫酸铜溶液,发现反应速率明显加快.原因是.
-
(4) 利用表中数据,可以求得:硫酸的物质的量浓度是 mol/L.
-
(1) 实验需用1.00mol•L﹣1 CuSO4溶液480mL,配制以上溶液需用的玻璃仪器除了烧杯、玻璃棒、量筒外还需;所称取的胆矾固体是;配制溶液浓度会导致所配溶液浓度偏高的是
A.称量质量正确,但胆矾晶体部分失结晶水
B.配制溶液时,定容时仰视容量瓶刻度线
C.定容摇匀后发现液面低于刻度线,再往容量瓶里加水定容至刻度
D.称量胆矾时把胆矾放在右盘称
-
(2) B与稀硫酸反应的化学方程式为.
-
(3) 甲同学认为A中可能含有杂质Na+ , 验证此判断正确的方法是.
-
(4) 气体C的成分:(SO3和SO2不需填).
-
(5) 通过计算确定A的组成为.
-
(1) 甲灼烧至恒重的化学方程式(M、Z用元素符号表示)
-
(2) 甲能用作塑料阻燃剂的原因.
-
(3) 工业上利用CO2和H2在一定条件下反应合成甲醇.已知下列反应:
①CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)△H1
CH3OH(g)+H2O(g)△H1②2H2(g)+O2(g)═2H2O(l)△H2
③H2O(g)═H2O(l)△H3
写出气态甲醇完全燃烧生成CO2(g)和气态水的热化学方程式: (用△H1、△H2、△H3表示△H)
-
(4) 反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),它的有关数据如图1所示,反应物起始的物质的量之比
CH3OH(g)+H2O(g),它的有关数据如图1所示,反应物起始的物质的量之比  =1.5或
=1.5或  =2
=2 下列说法正确的是 .
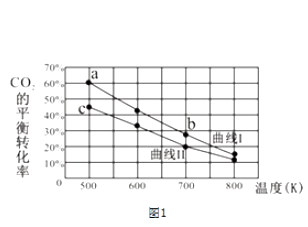 A . 曲线Ⅰ对应的反应物起始物质的量之比为1.5 B . 单位时间内消耗H2的物质的量与消耗H2O的物质的量之比为3:1时,反应达到平衡状态 C . a点对应的H2的平衡转化率为90% D . b点对应的平衡常数K值大于c点
A . 曲线Ⅰ对应的反应物起始物质的量之比为1.5 B . 单位时间内消耗H2的物质的量与消耗H2O的物质的量之比为3:1时,反应达到平衡状态 C . a点对应的H2的平衡转化率为90% D . b点对应的平衡常数K值大于c点 -
(5) CO2(g)+3H2(g)
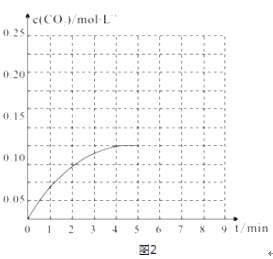
 CH3OH(g)+H2O(g)在体积为2L的固定绝热的密闭容器中加入1 molCH3OH和1 molH2O,第4 min达到平衡,反应中c(CO2)的变化情况如图2所示.
CH3OH(g)+H2O(g)在体积为2L的固定绝热的密闭容器中加入1 molCH3OH和1 molH2O,第4 min达到平衡,反应中c(CO2)的变化情况如图2所示. 在第5 min时向体系中再充入0.2molCO2和0.4molH2(其它条件不变),
第8 min达到平衡,此时c(H2)=c(CH3OH).
请在图2中画出5到9 min的c(CO2)浓度示意曲线.
-
(1) 机智如化学老师的你用固体烧碱配制500mL0.20molL﹣1的NaOH溶液,需要称取g固体,定容时除了胶头滴管和玻璃棒,还需要的仪器为.
-
(2) 语文老师要用36.5%(ρ=1.18gcm﹣3 )的浓盐酸配制0.4molL﹣1的盐酸240mL,需准确量取36.5%的浓盐酸mL.
-
(3) 若配制0.5molL﹣1的硫酸溶液的其他操作均正确,但出现下列错误操作,下列所配制的硫酸溶液浓度偏低的是 (填序号).A . 将稀释的硫酸溶液转移至容量瓶后,未洗涤烧杯和玻璃棒. B . 移液时容量瓶中有少量蒸馏水. C . 用胶头滴管向容量瓶中加水时溶液凹面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切. D . 用胶头滴管加水时,俯视观察溶液凹液面与容量瓶刻度相切. E . 稀释后没冷却到室温就将溶液转移至容量瓶.
①用天平称取28.6g Na2CO3•10H2O,放在烧杯中用适量的蒸馏水将其完全溶解;
②把制得的溶液小心地注入………….中;
③继续向容量瓶中加蒸馏水至液面距刻度线1cm~2cm处,改用………….小心滴加蒸馏水至溶液凹液面最低处与刻度线相切;
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转移入容量瓶,并轻轻摇匀;
⑤将容量瓶塞塞紧,充分摇匀.
请填写下列空白:
-
(1) 操作步骤的正确顺序为(填序号);
-
(2) 写出②③步骤中,所缺的仪器、;
-
(3) 若实验过程中加蒸馏水时不慎超过了刻度,应如何处理?.
-
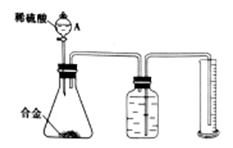
(1) 仪器A的名称是。
-
(2) 检查装置气密性的方法是。
-
(3) 检查装置气密性好后开始实验,滴加稀硫酸时开始没有气泡产生,你认为可能的原因是。
-
(4) 若测得气体的体积是4.48L(转化为标准状况下),则合金中镁的质量分数是,若读数时没有冷却到室温读数,测得合金中镁的质量分数(填写“偏大”或“偏小”)。
-
(5) 下列实验方案中能测定镁的质量分数的是。
A.W1gMg、Al合金量
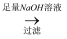 固体→洗涤、干燥称量质量为W2g
固体→洗涤、干燥称量质量为W2gB.W1gMg、Al合金
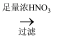 固体→洗涤、干燥称量质量为W2g
固体→洗涤、干燥称量质量为W2gC.W1gMg、Al合金
 排水量气测得气体体积为V2L(转化为标况)
排水量气测得气体体积为V2L(转化为标况)D.W1gMg、Al合金
 溶液
溶液 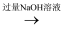 沉淀→洗涤、干燥称量质量为W2g
沉淀→洗涤、干燥称量质量为W2g
①用量筒量取50 mL 0.50 mol·L-1盐酸倒入小烧杯中,测出盐酸温度;②用另一量筒量取50 mL 0.55 mol·L-1NaOH溶液,并用另一温度计测出其温度;③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液温度。
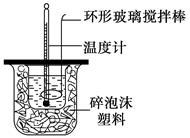
回答下列问题:
-
(1) 倒入NaOH溶液的正确操作是________(填序号)。A . 沿玻璃棒缓慢倒入 B . 分三次少量倒入 C . 一次迅速倒入
-
(2) 使盐酸与NaOH溶液混合均匀的正确操作是________(填序号)。A . 用温度计小心搅拌 B . 揭开泡沫塑料板用玻璃棒搅拌 C . 轻轻地振荡烧杯 D . 用套在温度计上的环形玻璃搅拌棒轻轻地上下搅动
-
(3) 现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1 L 1 mol·L-1的稀盐酸恰好完全反应,其反应热分别为ΔH1、ΔH2、ΔH3 , 则ΔH1、ΔH2、ΔH3的大小关系为。
-
(4) 假设盐酸和氢氧化钠溶液的密度都是1 g·cm-3 , 又知中和反应后生成溶液的比热容c=4.18 J·g-1·℃-1。为了计算中和热,某学生记录数据如下:
实验序号
起始温度t1/ ℃
终止温度t2/ ℃
盐酸
氢氧化钠溶液
混合溶液
①
20.0
20.1
23.2
②
20.2
20.4
23.4
③
20.5
20.6
23.6
依据该学生的实验数据计算,该实验测得的中和热ΔH=(结果保留一位小数)。
-
(5) (填“能”或“不能”)用Ba(OH)2溶液和硫酸代替氢氧化钠溶液和盐酸,理由是。
-
(1) 该同学用托盘天平应称量g Na2CO3粉末,使用容量瓶前必须进行的一步操作是。
-
(2) 下图是该同学配制的一些关键步骤和操作图。
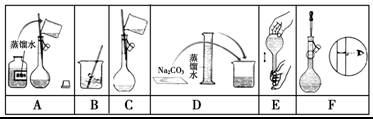
配制过程的先后顺序为(用字母A~F填写)。
-
(3) 步骤A通常称为洗涤,如果没有步骤A,则配得溶液的浓度将(填“偏高”、“偏低”、“不变”);步骤F如果俯视刻度线,配得溶液的浓度将(填“偏高”、“偏低”、“不变”)。
|
NaOH溶液起始读数 |
NaOH终点读数 |
|
|
第一次 |
0.10 mL |
18.60 mL |
|
第二次 |
0.30 mL |
19.00 mL |
-
(1) 准确移取25.00 mL某未知浓度的盐酸溶液的仪器名称是。
-
(2) 根据以上数据可以计算出盐酸的物质的量浓度为 mol/L。 (保留4位有效数字)
-
(3) 用0.2000 mol/L标准氢氧化钠溶液滴定待测盐酸溶液,滴定时左手控制碱式滴定管的玻璃球,右手不停摇动锥形瓶,眼睛注视, 直到滴定终点。
-
(4) 达到滴定终点的标志是。
-
(5) 以下操作造成测定结果偏高的原因可能是________(填字母代号)。A . 未用标准液润洗碱式滴定管 B . 滴定终点读数时,俯视滴定管的刻度,其他操作均正确 C . 盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗 D . 滴定到终点读数时发现滴定管尖嘴处悬挂一滴
-
(1) Ⅰ.实验步骤:
配制100mL待测白醋溶液:量取10.00mL食用白醋,注入烧杯中用水稀释后转移到100mL(填仪器名称)中定容,摇匀即得。
-
(2) 用酸式滴定管取待测白醋溶液20.00mL于锥形瓶中,向其中滴加2滴作指示剂。
-
(3) 读取盛装0.1000mol/LNaOH溶液的(填仪器名称)的初始读数。如果液面位置如图所示,则此时的读数为mL。

-
(4) 滴定。当看到现象时,停止滴定,并记录NaOH溶液的最终读数。再重复滴定3次。
-
(5) Ⅱ.实验记录
滴定次数
实验数据(mL)
1
2
3
4
V(样品)
20.00
20.00
20.00
20.00
V(NaOH)(消耗)
15.95
15.00
15.05
14.95
Ⅲ.数据处理与讨论:
甲同学在处理数据时计算得:平均消耗的NaOH溶液的体积V=
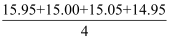 mL=15.24mL。指出他的计算的不合理之处:。按正确数据处理,可得市售白醋总酸量=g/100mL(结果保留四位有效数字)
mL=15.24mL。指出他的计算的不合理之处:。按正确数据处理,可得市售白醋总酸量=g/100mL(结果保留四位有效数字) -
(6) 乙同学仔细研究了该品牌白醋的标签,发现其中还含有苯甲酸钠作为食品添加剂,他想用资料法验证醋酸与苯甲酸钠不会发生离子互换反应,需查找在一定温度下的醋酸与苯甲酸的(填写序号)。
a.pH b.沸点 c.电离常数 d.溶解度
-
(7) 在本实验的滴定过程中,下列操作会使实验结果偏大的是(填写序号)
a.未用标准NaOH溶液润洗滴定管
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
c.锥形瓶中加入待测白醋溶液后,再加入少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出
回答下列问题:
-
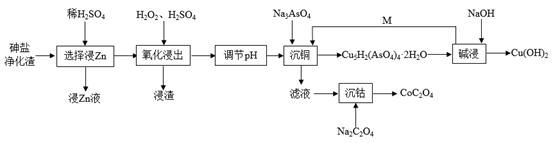
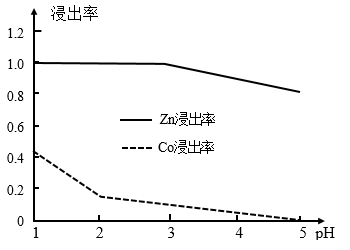
(1) 在“选择浸Zn”之前,将砷盐净化渣进行研磨的目的是。其他条件不变时,Zn和Co的浸出率随pH变化如图所示,则“选择浸Zn”过程中,最好控制溶液的pH=。
-
(2) 从“浸Zn液”中制备ZnSO4·7H2O时需要结晶、过滤、洗涤、烘干。烘干操作需在减压低温条件下进行,原因是。
-
(3) “氧化浸出”时,As被氧化为H3AsO4的化学方程式为。“浸渣”的主要成分为(填化学式)。
-
(4) 用NaOH溶液调节氧化浸出液至弱酸性,再加入Na3AsO4进行“沉铜”,得到难溶性的Cu5H2(AsO4)4·2H2O,则“沉铜”的离子方程式为。
-
(5) 为测定草酸钴产品的纯度,现称取m g样品,先用适当试剂将其转化,得到纯净的草酸钴溶液,再用过量的稀硫酸酸化,用c mol·L-1高锰酸钾标准液滴定,达到滴定终点时的现象为,共用去V mL高锰酸钾标准液,则该草酸钴产品的纯度为。若酸化时用盐酸代替硫酸,测得的纯度将。(填“偏高”“偏低”或“无影响”)。
 )是工业制硫酸的主要原料,在空气中煅烧黄铁矿,生成
)是工业制硫酸的主要原料,在空气中煅烧黄铁矿,生成  和
和  气体。某化学学习小组设计了如下实验,通过测量生成
气体。某化学学习小组设计了如下实验,通过测量生成  的质量来测定黄铁矿的纯度,根据要求回答下列问题。
的质量来测定黄铁矿的纯度,根据要求回答下列问题。 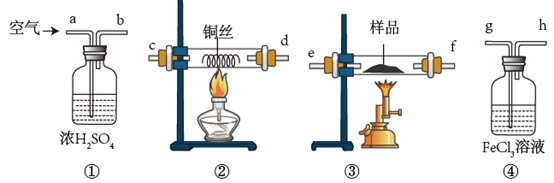
-
(1) 用各装置接口字母表示气流从左到右的顺序。
-
(2) 将样品研磨成粉末状再反应的目的是。
-
(3) 装置③中煅烧时发生反应的化学方程式为。
-
(4) 装置②中铜网的作用是。
-
(5) 反应结束后,关闭③处酒精喷灯仍需通一段时间的空气,其目的是。
-
(6) 写出装置④中发生反应的离子方程式。
-
(7) 该小组取8.0g样品进行实验,实验后装置④增重6.4g,则该样品纯度为。
 与
与  反应会因温度不同而可能生成
反应会因温度不同而可能生成  。某兴趣小组在用
。某兴趣小组在用  还原
还原  的实验中,用磁铁吸出生成的黑色粉末X。为确定X的组成,他们进行了相关实验探究。
的实验中,用磁铁吸出生成的黑色粉末X。为确定X的组成,他们进行了相关实验探究。
-
(1) 甲同学认为黑色粉末X能被磁铁吸附,因此Ⅹ是铁单质。但乙同学不同意他的观点,原因是。
-
(2) 乙同学:先将少量黑色粉末K放入盛有足量硫酸铜溶液的烧杯中,搅拌,固体部分溶解,有红色物质析出,过滤;利用磁铁分离除去滤渣中的红色物质,然后向剩余滤渣中加入盐酸,滴加几滴
 溶液,溶液出现红色。通过分析现象,乙同学得出X的组成是
溶液,溶液出现红色。通过分析现象,乙同学得出X的组成是  和
和  。
。 ①写出剩余滤渣与盐酸反应的离子方程式:;滴加
 溶液的目的是。
溶液的目的是。②若在粉末X中直接加入盐酸、
 溶液,溶液不出现红色。则不出现红色的原因是(用离子方程式表示)。
溶液,溶液不出现红色。则不出现红色的原因是(用离子方程式表示)。 -
(3) 丙同学的实验方案如下:
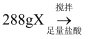 溶液
溶液 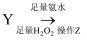 沉淀
沉淀 
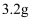 红棕色固体
红棕色固体①加入
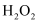 时,发生反应的离子方程式为,操作Z是。
时,发生反应的离子方程式为,操作Z是。②通过以上数据,可得出
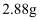 黑色粉末X中各成分的物质的量为。
黑色粉末X中各成分的物质的量为。
实验序号 | 实验温度/K | 有关物质 | 溶液颜色褪至无色所用时间/s | ||||
酸性KMnO4溶液 | H2C2O4溶液 | H2O | |||||
V/mL | C/mol·L-1 | V/mL | C/mol·L-1 | V/mL | |||
① | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
② | 293 | 2 | 0.02 | 3 | 0.1 | 1 | 8 |
③ | 313 | 2 | 0.02 | 3 | 0.1 | 1 | t2 |
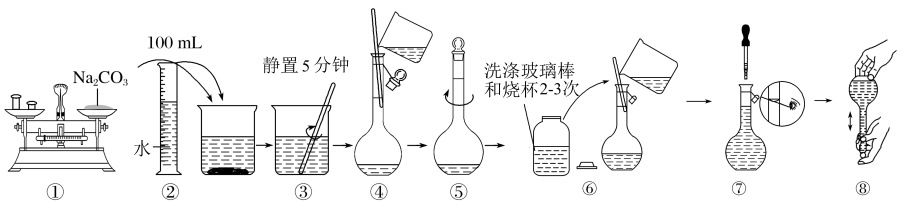
-
(1) 此配制过程中,溶解纯碱首次向烧杯中加入蒸馏水的体积约为mL。
-
(2) 使用托盘天平的第一步操作是,需要称量纯碱的质量为。
-
(3) 本次配制应选择的最主要仪器为(只写1个)。
-
(4) 指出所给流程图中的操作有两个明显的不正确,请简要描述出不正确点:、。
-
(5) 指出操作对所配制溶液浓度的影响(填写“偏大”“偏小”或“无影响”)。
①溶解、转移溶液后,没有洗涤玻璃棒及烧杯:。
②定容时仰视刻度线:。
③容量瓶未干燥,有少量蒸馏水:。
- 今有H2、Cl2混合气100mL(标况),其中一种气体体积为45mL。光照使两种气体发生反应后恢复到标况,气体体积为__
- (08江苏无锡)手电筒中使用的锌―锰干电池,在工作时反应的化学方程式为:Zn+2NH4Cl+2MnO2 ZnCl2
- 假如你有幸成为一位2010年广州亚运会的志愿者,你认为在服务过程中应当 ①维护国家安全、荣誉和利益 ②遵守
- 图甲表示某动物精巢内细胞分裂不同时期与核内DNA数量变化的关系,图乙为处于细胞分裂不同时期的细胞图像(只表示出部分染色体
- 下列物质的名称与化学式相符的是A.硫酸铁(FeSO4) B.碳酸钠(Na2CO3) C.氯酸钾(KCl) D.
- 2008年11月22日,APEC第十六次领导人非正式会议上指出,为遏制不断恶化的金融危机,各国应迅速采取一切必要的财政、
- 关于下列a、b、c、d四种生物的叙述,不正确的是() A. a和d不具有核膜包被细胞核 B.
- 质量为m的木块在质量为M的长木板上滑行(如图),长木板与水平地面间的动摩擦因数为μ1,木块与木板间的动摩擦因数为μ2,若
- 葛朗台是如何诱骗继承权的?
- 阅读下面的文章,完成小题。 不平凡的求学生涯 钱伟长的传奇人生,是一代中国学人希冀和奋斗的缩影。 1931年9月,清华大
- (二)古代诗歌阅读(11分) 螺川[注]早发 王猷定 月落秋山晓,城头鼓角停。 长江流远梦,短棹拨残星。 露湿鸥衣白,天
- 梭伦改革为雅典民主政治的形成打下牢固阶级基础的措施是 A.使公民大会成为国家最高权力机关 B.鼓励发展工商业 C.以财产
- 2013年5月27日,一场名为“追寻时光印记”的老物件展览在重庆大剧院拉开序幕,3000多件老物件让我们感受到半个世纪以
- 在一条倾斜的、静止不动的传送带上,有一铁块正在匀速向下滑动,如果传送带向上加速运动,同一铁块由上端滑到底端所用时间()
- 辽宁“丹东一号”清代沉船(致远舰)水下考古调查历时三年取得重大成果,确认在当年大东沟海战战场发现的沉船为清北洋水师致远舰
- There is always a parking lot _____theshopping centre. A. in
- Astronomers estimate called the Pleiades in the const
- 要除去下列各组物质中的少量杂质,所选试剂和方法不可行的是( ) 选项 物质 杂质 试剂、方法 A N2 O2 通过足量的
- 组成DNA的结构的基本成分是( ) ①核糖 ②脱氧核糖 ③磷酸 ④腺嘌呤、鸟嘌呤、胞嘧啶 ⑤胸腺嘧啶
- 如图是某种蜡烛在燃烧过程中高度与时间之间关系的图象,由图象解答下列问题:(1)此蜡烛燃烧1小时后,高度为 cm;经



