复杂化学式的确定 知识点题库
-
(1) 碳酸根的物质的量为 ;镁离子的物质的量为
-
(2) 铝离子的物质的量为
-
(3) 写出该碱式碳酸盐的化学式
-
(1) 要确定铁的某氯化物FeClx的化学式,可用离子交换和滴定的方法.实验中称取0.54g的FeClx样品,溶解后先进行阳离子交换预处理,再通过含有饱和OH﹣的阴离子交换柱,使Cl﹣和OH﹣发生交换.交换完成后,流出溶液的OH﹣用0.40mol/L的盐酸滴定,滴至终点时消耗盐酸25.0mL.计算该样品中氯的物质的量,并求出FeClx中,x值为;
-
(2) 现有一含有FeCl2和FeCl3的混合物样品,采用上述方法测得n(Fe):n(Cl)=1:2.1,则该样品中FeCl3的物质的量分数为;
-
(3) FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为;
-
(4) 高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料.FeCl3与KClO在强碱性条件下反应可制取K2FeO4 , 其反应的离子方程式为.
-
(1) X元素符号是;
-
(2) Z、W形成的气态氢化物的稳定性>(写化学式)。
-
(3) 由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液能与铜反应,离子方程式为。
-
(4) 由X、Y、Z、W和Fe五种元素组成的相对分子质量为392的化合物B,1molB中含有6mol结晶水。对化合物B进行如下实验:
a.取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体;过一段时间白色沉淀变为灰绿色,最终变为红褐色。
b.另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解。
①由实验a、b推知B溶液中含有的离子为;
②B的化学式为。
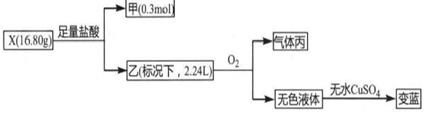
已知:气体乙在标况下的密度为1.52g·L-1 , 气体丙无色、有刺激性气味,能使品红溶液褪色。
-
(1) X的化学式为,乙的电子式为。
-
(2) X与足量盐酸反应的化学方程式为 。
-
(3) 在澄清石灰水中通入过量气体丙反应的离子方程式为。
请回答:
-
(1) 甲的化学式是。
-
(2) 实验室可通过石墨棒为电极电解NH4Cl和盐酸的混合溶液来制备甲,电解时发生反应的化学方程式为 。
-
(3) ①甲遇水蒸气可形成一种常见的漂白性物质C 同时放出气体D ,该反应为非氧化还原反应,写出甲与水反应的化学方程式为。
②D在高温条件下能还原Fe2O3 , 生成两种单质,写出该反应的化学方程式。
-
(1) 2 mol O3和3 mol O2的质量之比为,同温同压下的密度之比为,含氧原子数之比为。
-
(2) 在标准状况下,由CO和CO2组成的混合气体6.72 L,质量为12 g。此混合物中CO和CO2分子数目之比是,混合气体的平均摩尔质量是。
-
(3) 气体化合物A的化学式可表示为OxFy,已知同温同压下10 mL A受热分解生成15 mL O2和10 mL F2,则A的化学式为,推断的依据是。
-
(4) 在标准状况下,15.6 g Na2O2投入足量水中,可产生O2的体积为。
-
(5) 标准状况下有①0.112 L水、②3.01×1023个HCl分子、③13.6 g H2S气体、④0.2 mol氨气、⑤2 mol氦气、⑥6.02×1023个白磷(P4)分子,所含原子个数从大到小的顺序为。
 CoxOy+CO2来生产相应的钴的氧化物。实验室中可以用下列装置来制取钴的氧化物并测定其分子组成。
CoxOy+CO2来生产相应的钴的氧化物。实验室中可以用下列装置来制取钴的氧化物并测定其分子组成。 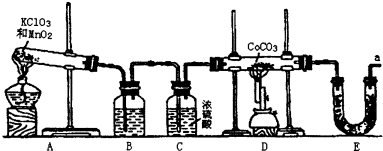
请填写下列空白:
-
(1) 写出A装置的大试管里发生反应的化学方程式;
-
(2) E装置的U形管里盛放的物质是___;A . P2O5 B . 无水CaCl2 C . 碱石灰 D . 无水CuSO4
-
(3) O3的氧化性比O2强。已知制得的O2中含有少量的Cl2和O3 , 则B装置中所盛放的物质是___;A . NaOH溶液 B . 饱和NaHCO3溶液 C . 饱和NaCl溶液 D . KI溶液
-
(4) 实验结束时,若先撤去A装置中的酒精灯,会引起;
-
(5) 在CoCO3完全转化为CoxOy后,若称得E管增重4.40g,D管内残留物质的质量是8.30g,则生成CoxOy的化学式为;请写出详细的计算过程。
-
(6) 此实验装置存在一个比较大的缺陷,如何完善。
-
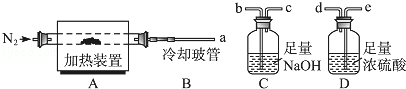
(1) Mg2Al(OH)6Cl•xH2O热分解的化学方程式为.
-
(2) 若只通过测定装置C、D的增重来确定x,则装置的连接顺序为(按气流方向,用接口字母表示),其中C的作用是.装置连接后,首先要进行的操作的名称是.
-
(3) 加热前先通N2排尽装置中的空气,称取C、D的初始质量后,再持续通入N2的作用是、等.
-
(4) 完全分解后测得C增重3.65g、D增重9.90g,则x=.若取消冷却玻管B后进行实验,测定的x值将(填“偏高”或“偏低”).
-
(5) 上述水滑石在空气中放置时易发生反应生成[Mg2Al(OH)6Cl1﹣2x(CO3)y•zH2O],该生成物能发生类似的热分解反应.现以此物质为样品,用(2)中连接的装置和试剂进行实验测定z,除测定D的增重外,至少还需测定.
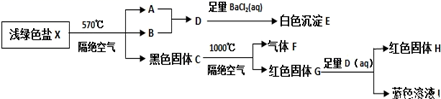
上述实验中,得到23.3g白色沉淀 E、28.8g红色固体G和12.8g红色固体H。
已知:①X分解成A、B、C的反应为非氧化还原反应;
②常温下B呈液态且1个B分子含有10个电子。
请回答如下问题:
-
(1) 写出B分子的电子式;X的化学式是。
-
(2) 在隔绝空气、570℃温度下加热X至完全分解的化学反应方程式为:。
-
(3) 请写出G溶于D溶液的离子方程式:。
-
(4) 请设计实验检验固体C中是否仍含有X:。
Cu(Inl-xGaxSe2)(简称CIGS)可作多晶膜太阳能电池材料,具有非常好的发展前景。
回答下列问题:
-
(1) 已知铟的原子序数为49,基态铟原子的电子排布式为[Kr];Ga、In、Se,第一电离能从大到小顺序为。
-
(2) 硅与碳位于同主族,碳的化合物中往往有碳碳双键、碳碳三键,但是硅的化合物中只存在硅硅单键,其主要原因是。常温常压下,SiF4呈气态,而SiCl4呈液态,其主要原因是。
-
(3) 31Ga可以形成GaCl3·xNH3 (x=3、4、5、6)等一系列配位数为6的配合物,向上述某物质的溶液中加入足量AgNO3溶液,有沉淀生成:过滤后,充分加热滤液有氨气逸出,且又有沉淀生成,两次沉淀的物质的量之比为1:2。则该溶液中溶质的化学式为。
-
(4) Seo32-的立体构型为;SeO2中硒原子采取杂化类型是。
-
(5) 常见的铜的硫化物有CuS和Cu2S两种。已知:晶胞中S2-的位置如图l所示,铜离子位于硫离子所构成的四面体中心,它们晶胞具有相同的侧视图如图2所示。已知CuS和Cu2S的晶胞参数分别为a pm和b pm,阿伏加德罗常数的值为NA。
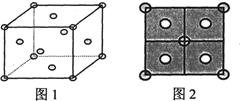
①CuS晶体中,相邻的两个铜离子间的距离为pm。
②Cu2S晶体中,S2-的配位数为。
⑨Cu2S晶体的密度为p=g·cm-3(列出计算式即可)。
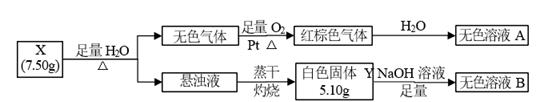
请回答:
-
(1) 白色固体 Y 的名称是;X 的化学式是。
-
(2) 红棕色气体转化为无色溶液A 的化学方程式是
-
(3) 将少量无色溶液B 滴入无色溶液 A 时发生反应的离子方程式是
-
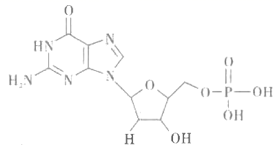
(1) 构成DNA片段的元素中,N、O、P电负性由大到小的顺序是。
-
(2) 已知N2O为直线形结构,结构式为N=N=O。则N2O是(填“极性”或“非极性”)分子,中间氮原子的杂化轨道类型为杂化。
-
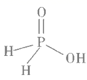
(3) 磷能形成多种含氧酸,某资料认为次磷酸的结构如图所示,则次磷酸分子中σ键与π键数目之比为,1mol次磷酸最多能与 molNaOH发生中和反应。
-
(4) 已知下列数据:
物质
熔点/K
沸点/K
分解温度/K
NH3
195.3
239.7
1073
PH3
139.2
185.4
713.2
NH3的熔、沸点均高于PH3的原因是;PH3的分解温度高于其沸点,其原因是。
-
(5) 某磷青铜晶胞结构如图所示。
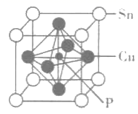
①其化学式为。
②基态锡原子的价电子排布式为。
该晶体中距离Sn原子最近的Cu原子有个。
③若晶体密度为8.82g·cm-3 , 距离最近的Cu原子核间距为pm(用含NA的代数式表示,设NA表示阿伏加德罗常数的值)。
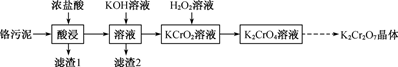
已知:①Cr(OH)3不溶于水,与Al(OH)3类似,具有两性;
②酸性条件下,H2O2可将+6价的Cr还原为+3价的Cr;
③+6价的Cr在溶液pH<5时,主要以  的形式存在;在pH>7时,主要以
的形式存在;在pH>7时,主要以  的形式存在;
的形式存在;
④部分物质溶解度曲线如图所示:
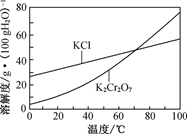
-
(1) 用KOH调节pH至11-12的目的是。
-
(2) 写出加入30%H2O2过程中发生的离子反应方程式:。
-
(3) 流程中K2CrO4溶液含有少量过氧化氢,经过多步处理制得K2Cr2O7晶体。请补充完整由K2CrO4溶液为原料制备K2Cr2O7晶体的实验方案:取一定量流程中的K2CrO4溶液于烧杯中,,,,过滤、冰水洗涤及干燥。(实验中必须使用的试剂:稀盐酸)
-
(4) 铁明矾[Al2Fe(SO4)4∙24H2O]在空气中能被氧气氧化,久置后生成盐A,盐A的化学式为Al2Fe(OH)x(SO4)4∙24H2O。为确定盐A的化学式,学习小组进行如下实验:
①取一定质量的盐A样品溶于足量的稀硫酸中,将溶液分为两等份。
②其中一份与酸性K2Cr2O7溶液充分反应(反应后
 被还原成Cr3+),消耗浓度为0.3000mol∙L-1的K2Cr2O7溶液25.00mL;
被还原成Cr3+),消耗浓度为0.3000mol∙L-1的K2Cr2O7溶液25.00mL;③往另一份溶液中加入足量稀氨水,在空气中微热并搅拌使之充分反应,待沉淀不再变化后过滤,将沉淀洗涤并充分灼烧后称量,得9.10g干燥固体粉末。
通过计算确定x的值(写出计算过程)。
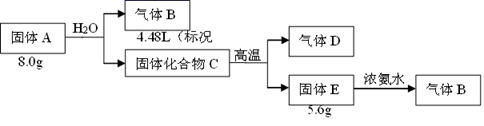
-
(1) 组成A的元素是(填元素符号),A的化学式是。
-
(2) 固体A与足量稀盐酸反应的化学方程式。
-
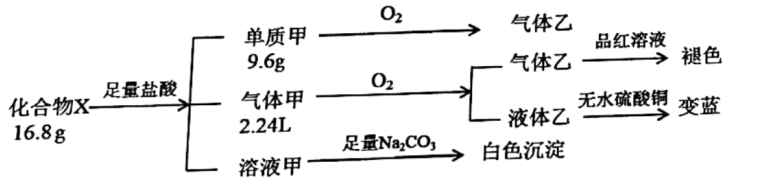
(1) 气体甲的电子式为,X的化学式为。
-
(2) 写出化合物X与足量盐酸反应的化学方程式:。
-
(3) 向澄清的石灰水中通入过量的气体乙,离子方程式为。
- X、Y两元素可形成X2Y3型化合物,则X、Y原子基态时外围电子的电子排布不可能是 ( )A.X:
- 下图中阴影部分表示黑夜,图示日期过后地球公转速度减慢。据此回答下面试题。1. 关于图示时刻的叙述,正确的是( ) A.
- 在高速公路的拐弯处,通常路面都是外高内低,如图所示。汽车的运动可看作是做半径为R的圆周运动。设内外路面高度差为,路基的水
- 下列各句中,没有语病的一句是 A.为充分体现志愿者的工作价值,亚运会前夕,广州亚组委志愿者部创造性地推出了“志愿时”,即
- 新时期,如何弘扬爱国主义? 爱国主义是动员和鼓舞中国人民团结奋斗的一面旗帜,是各族人民风雨同舟、自强不息的精神支
- In the United States there was an unusual tale telling of th
- 下图1是生长素作用特点曲线,图2是不同浓度生长素影响某植物乙烯生成和成熟叶片脱落的实验结果示意图.下列叙述,错误的是()
- 阅读下面的文字,完成1~3题。 “中庸”辨义 “中庸”是儒家伦理学说的一个核心思想,但在现实生活中却常常被误解、误用,颇
- 中国的英文名字是China,是瓷器的意思。下列关于中国古代制瓷业发展的表述,不正确的是:( )A.商周时期已经开始
- The policeman asked ________ with the old women. A. what the
- 含硫化合物的种类很多,现有SO2、Na2SO3、H2SO4、 CuSO4 四种常见的含硫化合物。回答下列问题: (1)将
- 施用农药DDT的地区虽然占陆地面积的一部分,可是在远离施药地区的南极,动物体内也发现了DDT,这种现象说明了 A
- 如图所示,L标有“12V 6W”的字样(灯泡的电阻不变),R1是定值电阻,R2上标有“24 1A”,电源电压为12V。则
- 白藜芦醇结构如右式, 它广泛存在于食物(例如桑椹、花生、尤其是葡萄)中,它可能具有抗癌性。能够与1mol该化合物起反应的
- 在华盛顿会议上《五国海军条约》的签订: A.成功地解决了列强对中国的争夺 B.成功地解决了对太平洋地区势力范围的制海权
- 既不能构成人体细胞,也不为人体提供能量但作用却很大的营养物质是 ( ) A.水
- 有人为探究植物根愈伤组织分化因素而设计了如图所示的实验,下列有关该实验的操作或结论的叙述中正确的是()A.生长素是诱导根
- 如图所示,一束红光从水中的A点沿AO方向以入射角i射向空气,反射后通过水中的B点,折射后通过空气中的C点(B、C在图中均
- 下面一段文字如果加上一些虚词,表达效果会更好。为此,请将下面的虚词插入文中适当的地方。插入后,将紧接虚词后的词语填在横线
- ......



