复杂化学式的确定 知识点题库
-
(1) 将1.5mol SO2用氢氧化钠溶液、石灰及氧气处理后,假设硫元素不损失,理论上可得到 g石膏(CaSO4•2H2O)
-
(2) 用CH4消除NOx污染的化学方程式为:
CH4+4NO=2N2+CO2+2H2O; CH4+2NO2=N2+CO2+2H2O
现有11.2L NO2、NO的混合气体NOx , 将其还原为N2 , 需要4.48L 的CH4 , 则混合气体中NO2、NO的物质的量之比为 .(体积都已换算为标准状况)
-
(3) (a)常温下用氧缺位铁酸锌ZnFe2Oy可以消除NOx污染,使NOx转变为N2 , 同时ZnFe2Oy转变为ZnFe2O4 . 若2mol ZnFe2Oy与足量NO2可生成0.5mol N2 , 则y= .
(b)氧缺位铁酸锌ZnFe2Oz化学式的氧化物形式为aZnO•bFeO•cFe2O3 . 已知1mol ZnFe2Oz最多能使4.0L(标况)NO1.4转化为N2 . 则上述氧化物形式的化学式可具体表示为 .
-
(1) 该复杂盐的化学式为.
-
(2) 该复杂盐中两种阳离子的质量比为.
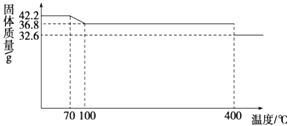
试回答下列问题:
-
(1) 试确定150℃时固体物质的化学式为.
-
(2) 查阅资料知:虽然亚铁氰化钾自身毒性很低,但其水溶液与酸反应放出极毒的氰化氢(HCN)气体;亚铁氰化钾加热至一定温度时能分解产生氰化钾(KCN).据此判断,烹饪食品时应注意的问题为.
-
(3) 在Fe2+、Fe3+的催化作用下,可实现2SO2+O2+2H2O═2H2SO4的转化.已知,含SO2的废气通入
Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2++O2+4H+═4Fe3++2H2O,则另一反应的离子方程式为.则上述转化的重要意义在于.
-
(1) 要确定铁的某氯化物FeClx的化学式。可用离子交换和滴定的方法。实验中称取0.54g的FeClx样品,溶解后先进行阳离子交换预防处理,再通过含有饱和OH-的阴离子交换柱,使Cl-和OH-发生交换。交换完成后,流出溶液的OH-用0.40mol·L-1的盐酸滴定,滴至终点时消耗盐酸25.0mL。计算该样品中氯的物质的量,并求出FeClx中x值。
-
(2) 现有一含有FeCl2和FeCl3的混合样品,采用上述方法测得n(Fe): n(Cl)=1:2.1,则该样品中FeCl3的物质的量分数为。在实验室中,FeCl2可用铁粉和反应制备,FeCl3可用铁粉和反应制备。
-
(3) FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为。
-
(4) 高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4 , 其反应的离子方程式为。
-
(1) 通常制造的农药含元素F、P、S、Cl。四种元素的电负性从大到小的顺序为;第一电离能从大到小的顺序为。
-
(2) 科学家曾利用元素周期表寻找F、Cl的含碳化合物作为制冷剂。已知CCl4的沸点为76.8℃,CF4的沸点为-128℃,若要求制冷剂沸点介于两者之间,则含一个碳原子的该制冷剂可以是(写出其中一种的化学式)。
-
(3) 1963年以来科学家借助射电望远镜,在星际空间已发现NH3、HC≡C-C≡N等近两百种星际分子。与NH3互为等电子体的阳离子为;HC≡C-C≡N分子中
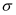 键与
键与 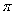 键的数目比n(
键的数目比n( 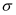 )∶n(
)∶n( 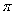 )=。
)=。
-
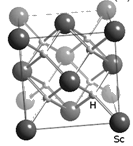
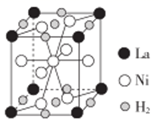
(4) 过渡元素(包括稀土元素)中可寻找各种优良催化剂。Sc的一种氢化物的晶胞结构如图所示,该氢化物的化学式为。
试回答如下问题:
-
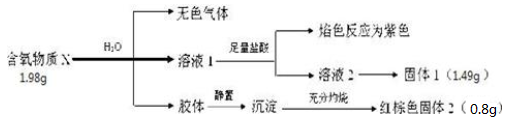
(1) X的化学式为,写出X与H2O反应的离子方程式
-
(2) 工业上由红棕色固体2可以制备其单质,写出化学方程式.
-
(3) 保存X时应注意.

已知:i)反应①为非氧化还原反应,反应③为氧化还原反应;ii)A、B混合气体遇无水硫酸铜呈蓝色,溶于水后溶液呈酸性。请回答:
-
(1) X 所含元素除 Cu、Cl 外,还有、。(写元素符号)
-
(2) 写出 X 灼烧的化学反应方程式:。
-
(3) 步骤③发生的离子反应方程式是:。
-
(1) 过氧化钠可在呼吸面具或潜水艇中作为氧气的来源,请写出Na2O2的电子式,(填“是”或“不是”)碱性氧化物。
-
(2) 工业上,粗盐需精制,为除去Ca2+需要加入的试剂名称为。食盐中含有KIO3 , 可加入稀硫酸酸化的淀粉碘化钾溶液检测,若变蓝,则说明含有KIO3 , 写出相应反应的离子方程式。等物质的量Cl2、H2O2、ClO2(还原产物为Cl-)消毒效率最高的是。
-
(3) 已知硼酸可治疗湿疹,是一元弱酸,存在电离方程式H3BO3+H2O
 B(OH)
B(OH)  +H+ , 其与过量NaOH反应得到的盐的化学式为。
+H+ , 其与过量NaOH反应得到的盐的化学式为。
-
(4) 含重金属离子Cu2+的废水中,可加入Na2S溶液除去,写出Na2S溶液与Cu2+发生反应的离子方程式;某温度条件下,CuSO4·xH2O失掉0.5个结晶水,失重3.88%,则x=。
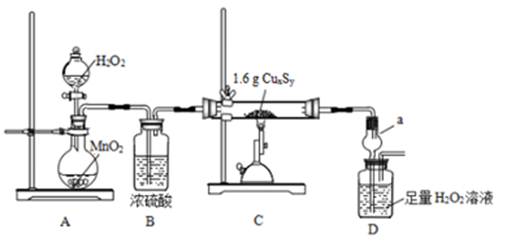
步骤一:打开A装置分液漏斗的活塞,高温灼烧1.6 g CuxSy至固体质量不再变化,得到红色固体单质和一种能使品红溶液褪色的气体。
步骤二:将D中所得溶液按下述流程进行处理:煮沸D中溶液并冷却→配制250 mL溶液→取25.00 mL溶液,滴入2-3滴酚酞溶液→滴定,消耗0.1 mol/L NaOH溶液20.00 mL。
回答下列问题:
-
(1) 仪器a的名称是,其作用为。
-
(2) 装置D中反应的化学方程式为。
-
(3) 步骤二中配制溶液时所需的玻璃仪器除玻璃棒和烧杯外,还有。
-
(4) 利用题中提供的数据可计算得出该铜硫化物的化学式为。
-
(5) 有同学认为可将装置D改为一个装有足量碱石灰的干燥管,通过测定反应前后干燥管的增重来计算硫元素的含量。该方案测定硫元素的含量的结果(填“偏大”、“偏小”或“无影响”)。
-
(1) I.由三种短周期元素组成的化合物A,按如下流程进行实验。已知相同条件下气态A物质的密度为氢气密度的49.5倍。
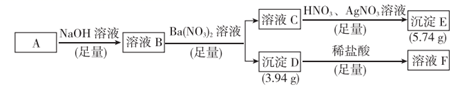
请回答:
组成A的三种元素为,A的化学式为。
-
(2) A与足量NaOH溶液反应的化学方程式为。
-
(3) A与足量氨气在一定条件下可以反应生成2种常见的氮肥,该反应的化学方程式为。
-
(4) II.某兴趣小组利用废铜屑制备硫酸铜晶体,装置如图所示(夹持装置和加热装置已略去),在实验中将适量硝酸逐滴加入到废铜屑与稀硫酸的混合物中,加热使之反应完全,通过蒸发浓缩、冷却结晶,制得硫酸铜晶体。
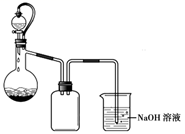
将硝酸逐滴加入到废铜屑与稀硫酸的混合物中的目的是。
-
(5) 实验过程中盛有NaOH溶液的烧杯上方仍然出现了红棕色气体,请对该实验装置提出改进意见:。
-
(1) Ⅰ.已知化合物X、A均为红色固体,X含有四种元素,气体单质H密度为
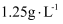 (标准状况下)。流程中每一步反应试剂均过量且完全反应。
(标准状况下)。流程中每一步反应试剂均过量且完全反应。 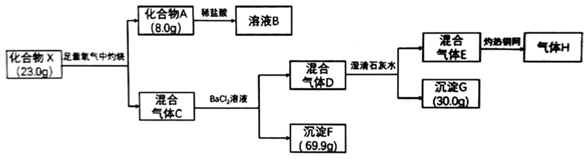
气体H的化学式,X的化学式。
-
(2) 混合气体C通入氯化钡溶液生成沉淀F,请写出反应的离子方程式。
-
(3) 固体X与足量氧气反应的化学方程式。
-
(4) Ⅱ.碱式氯化铜为绿色或墨绿色粉末,难溶于水,溶于稀酸和氨水,在空气中十分稳定。模拟制备碱式氯化铜的实验如下:向
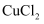 溶液中通入
溶液中通入  和
和  ,调节pH至5.0~5.5,控制反应温度于70~80℃,实验装置如图所示(部分夹持装置已省略)。
,调节pH至5.0~5.5,控制反应温度于70~80℃,实验装置如图所示(部分夹持装置已省略)。 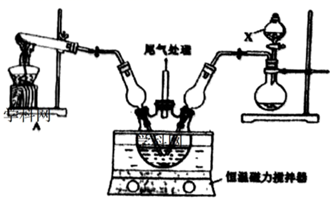
仪器X的名称是。
-
(5) 反应过程中,在三颈烧瓶内除观察到有白烟生成,还可能观察到的现象是。
-
(6) 若体系
 过高会导致碱式氯化铜的产量(填“偏高”、“偏低”或“无影响”)。
过高会导致碱式氯化铜的产量(填“偏高”、“偏低”或“无影响”)。
-
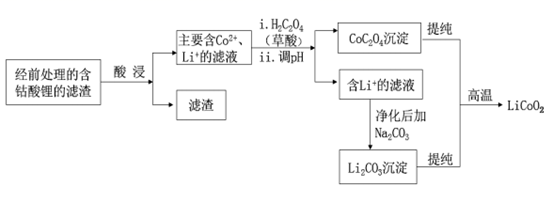
(1) 用H2SO4酸浸时,通常需添加30%的H2O2以提高浸出效率,写出相应反应的化学方程式:。
-
(2) 用盐酸代替H2SO4和H2O2 , 浸出效率也很高。但工业上不使用盐酸,主要原因是会产生有毒、有污染的气体(填化学式)。
-
(3) 其他条件不变时,相同反应时间,随着温度升高,含钴酸锂的固体滤渣在H2SO4和30%的H2O2混合液中的浸出率如下表所示,请分析80℃时钴的浸出率最大的原因:。
反应温度/℃
60
70
80
90
钴的浸出率/%
88
90.5
93
91
-
(4) 已知常温下草酸Ka1=5.6×10-2 , Ka2=1.5×10-4 , Ksp(CoC2O4)=4.0×10-6 , 求常温下Co2+与草酸反应生成CoC2O4沉淀的平衡常数K=。
-
(5) 高温下,在O2存在时,纯净的CoC2O4与Li2CO3再生为LiCoO2的化学方程式为。
-
(6) 在空气中煅烧CoC2O4生成钴的氧化物和CO2 , 若测得充分煅烧后固体的质量为3.615g,CO2的体积为2.016L(标准状况),则钴的氧化物的化学式为。
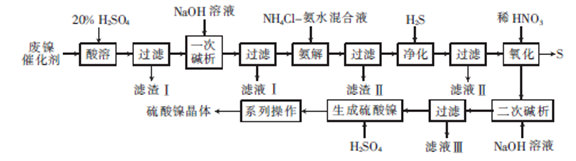
已知:Ni3+的氧化性比稀HNO3强。
回答下列问题:
-
(1) 已知:Cr3++4OH-= CrO2-+2H2O。“一次碱析”时,需加入过量的NaOH溶液的目的是。
-
(2) “氨解”的目的为。
-
(3) “净化”“过滤”后得到含有两种元素的不溶性化合物,该化合物的化学式为,写出“氧化”中发生反应的离子方程式:。
-
(4) 从NiSO4溶液中得到硫酸镍晶体需经过“系列操作”为,,过滤,洗涤,干燥(填操作名称)。
-
(5) 1844年,科学家发现金属镍可以用NaH2PO2将水溶液中的Ni2+还原出来,NaH2PO2将转化为H3PO3 , 这一原理现用于化学镀镍。写出化学镀镍原理的离子方程式。
-
(6) 为测定硫酸镍晶体(NiSO4·n H2O)的组成,进行如下实验:称取2.63g样品,配成250.00mL溶液,准确量取配制的溶液25.00mL,用0.0400mol/L EDTA(Na2H2Y)标准溶液滴定Ni2+(离子方程式为Ni2++H2Y2-=NiY2-+2H+),消耗EDTA标准溶液25.00mL。则硫酸镍晶体的化学式为。
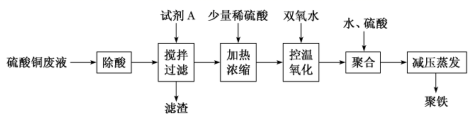
回答下列问题:
-
(1) 试剂A为。
-
(2) 本实验中两次加入硫酸,其中“加热浓缩“时加入稀硫酸,除了抑制离子水解,还为了,“聚合”时加硫酸是为了控制溶液的pH在一定范围内,若pH偏大,则。
-
(3) “控温氧化”时选用绿色氧化剂双氧水,该过程需要控温的原因是。
-
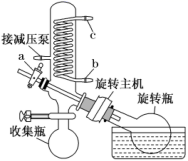
(4) 减压蒸发装置如图所示。实验开始时,应先打开减压泵,从(填字母)口通入冷水,再打开旋转主机;实验结束时应先关闭旋转主机,再,打开阀门a通大气后,最后取下(填仪器名称),从中获得聚铁。本实验采取减压蒸发的理由是。
-
(5) 测定聚合硫酸铁样品主要成分的化学式。准确称取所得聚铁样品5.520g,溶于适量稀盐酸中,然后分成两等份:
a.一份加入过量的BaCl2溶液,然后过滤、洗涤、干燥,称重,得固体质量1.165g;
b.另一份置于250mL锥形瓶中,加入过量KI,充分反应后再用0.5000 mol•L-1Na2S2O3溶液滴定至终点,消耗标准溶液20.00mL。
已知:I2+2S2O32–=2I–+S4O62–(无色)
①计算所得产品化学式中n=。
②若m=4,写出“聚合”过程的化学方程式:。
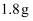 , 在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重
, 在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重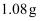 和
和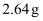 。试求该有机物的实验式和分子式。
。试求该有机物的实验式和分子式。
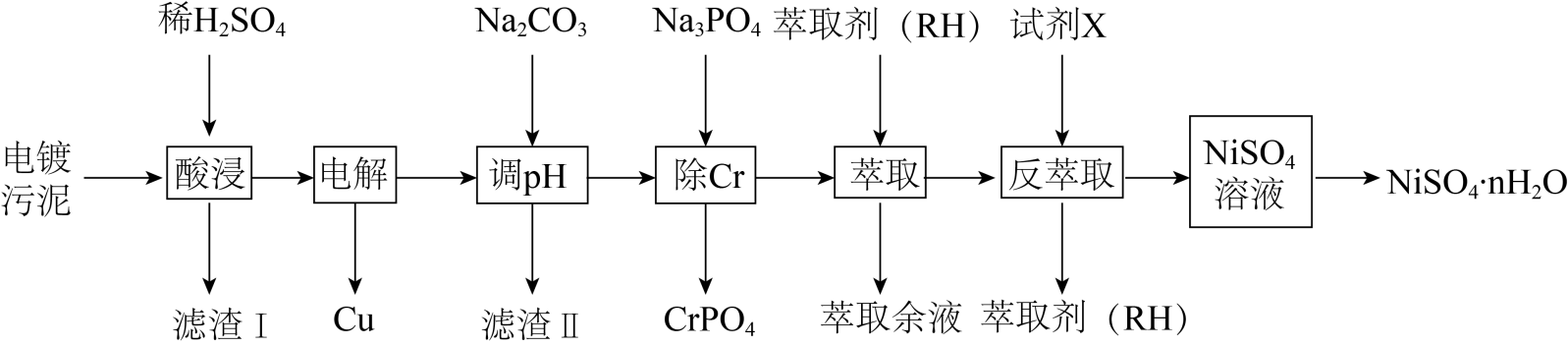
已知:Ⅰ.电镀污泥含有Cu(OH)2、Ni(OH)2、Fe(OH)3、Cr(OH)3和SiO2等。
Ⅱ.萃取剂(RH)萃取Ni2+的原理为Ni2++2RH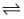 NiR2+2H+。
NiR2+2H+。
回答下列问题:
-
(1) “酸浸”时,为加快浸出速率,提高生产效益,降低生产成本,下列措施不合理的有____ (填标号)。A . 搅拌 B . 适当增大硫酸的浓度 C . 对污泥进一步球磨粉碎
-
(2) “电解”时,铜的电解电压(U)较低,且电解速率很快,铁和铬存在形式随电解电压的变化如下表。为得到纯的NiSO4·nH2O,电解电压(U)的范围是(单位:V)。
电解电压/V
1.0
1.2
1.5
2.0
2.5
3.0
3.5
Fe2+
有
有
有
无
无
无
无
Cr4+
无
无
无
无
无
有
有
-
(3) 萃取余液可在操作单元中循环利用(填选项),
A.酸浸 B.调pH C.除Cr
反萃取剂X为 (填化学式)。
-
(4) “反萃取”得到的NiSO4溶液,可在强碱溶液中被NaClO氧化,得到用作镍镉电池正极材料的NiOOH。该反应的离子方程式为。
-
(5) 第三代混合动力车,可以用电动机,内燃机或二者结合推动车轮。汽车上坡或加速时,电动机提供推动力,降低汽油的消耗;在下坡时,电池处于充电状态。混合动力车目前一般使用镍氢电池。镍氢电池充放电原理如图1所示,根据所给信息判断,混合动力车上坡或加速时,乙电极的电极反应式为。
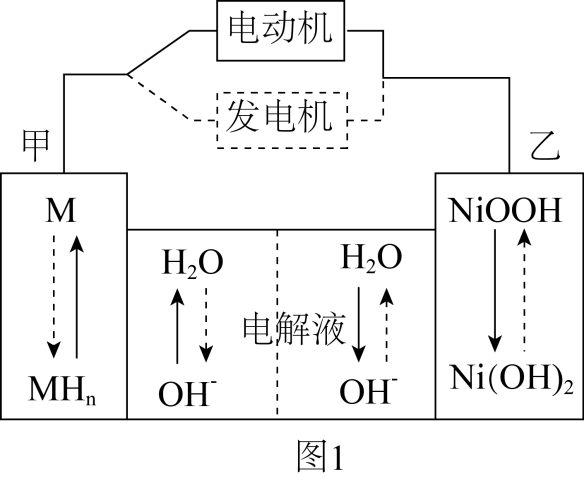
-
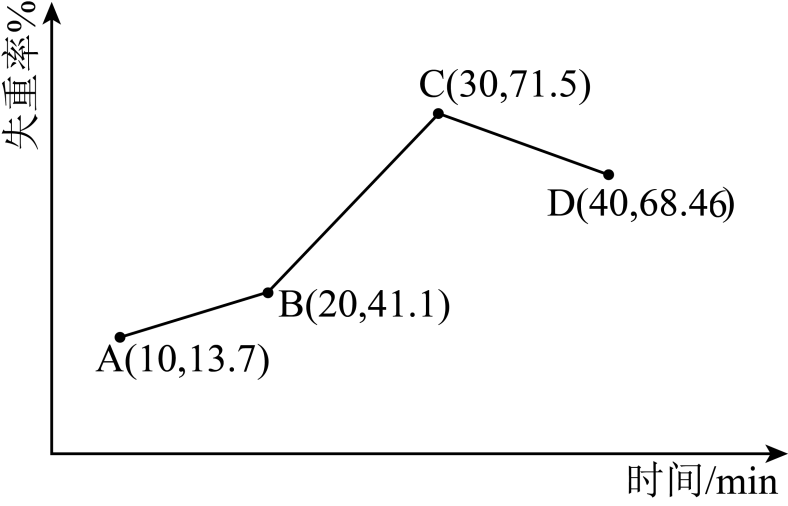
(6) 采用热重分析法测定NiSO4·nH2O样品所含结晶水数。将样品在900℃下进行煅烧,失重率随时间变化如下图,A点时失掉2个结晶水,n的值为。
- 下列依据热化学方程式得出的结论正确的是 A.已知2SO2(g)+O2 2SO3(g)
- 给出下列互不相同的直线l,m,n和平面α,β,γ的三个命题: ①若l与m为异面直线,l⊂α,m⊂β,则α∥β;②若α∥β
- 下列生物的细胞中,有成形细胞核的是( ) A.大肠杆菌 B.葡萄球菌 C.酵母菌 D.肺炎双球
- 农业税收在国家收入中的比重具有明显的时代特征,我国农业正逐步向现代过渡,减免农业税有利于农业的发展。 阅读下列图文材料。
- _____ do you think is tallest in our class? A. Of whom B.
- 下图为“我国某山1月和7月的平均气温垂直分布图”。读图回答。 根据图示信息判断,该山最可能位于我国的
- 观察下列各式: 1×3+1=4=22, 2×4+1=9=32, 3×5+1=16=42,4×6+1=25=52,…….请
- 一个样本有100个数据,最大的351,最小的是75,组距为25,可分为___ ____组.
- 下列叙述对应有误的是 A.细胞质基质:也是人体细胞内产生ATP的场所 B.脂双层:构成膜
- 下表反映1500-1800年间欧洲主要国家商船抵达亚洲的数量。结合所学知识和表格信息可以得出的结论是
- 下列没有发生化学变化的是 A.雕像受腐蚀 B.铜插入硝酸银溶液后 C.镁条燃烧 D.水流过沙砾池
- 方程(r为参数,θ为常数,|θ|<)所表示的曲线是( )A.以点(0,-1)为圆心,半径为|r|的圆的一部分B.以
- 下列地理现象和形成原因,组合正确的是( ) A.夏天多云时,白天不会太热——大气的散射作用 B.日落后的黄昏天空
- 已知向量,若//.则锐角.
- 解不等式组:
- 如图,在△AOB中,=a,=b,M、N分别在OA、OB上且有=λa(0<λ<1),=μb(0<μ<1).设AN与BM交于
- 根据右图的溶解度曲线,判断下列说法不正确的是( ) A.图中a点表示,t2℃时100g水中最多溶解甲物质25g B.甲
- 氧化性随原子序数的增加而增强的是( ) A.F-、Cl-、Br-
- 做简谐运动的物体向平衡位置运动时,速度越来越大的原因是( ) A.回复力对物体做正功,动能增加
- 补写出下列名篇名句中的空缺部分。(两题任选一题) (1)西望夏口, ______ ,山川相缪,郁



