物质的结构与性质之间的关系 知识点题库
(1)A、B、C三种元素分别是 、 、 .
(2)A、B、C之间可形成多种化合物,其中属于离子化合物的化学式分别为 、 、 (任举三种).
(3)用电子式表示B和C形成化合物的过程
-
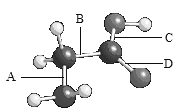
(1) 在如图的模型中, 处表示的是双键(填A、B、C、D);Z的核外共有 种不同能量的电子,有 个未成对电子.X形成的单质晶体可能为 .
a.离子晶体b.分子晶体c.原子晶体d.金属晶体
-
(2) Y与W可形成YW5的化合物,有关该物质的叙述不正确的是 .
A、离子化合物,固态时是离子晶体
B、溶于水所形成的溶液显碱性
C、投入少量水中,有两种气体产生
D、YW5中Y的化合价为﹣5价
-
(3) 下列可以验证Y与Z两元素原子得电子能力强弱的实验事实是 .
A、比较这两种元素的气态氢化物的沸点
B、比较这两种元素最高价氧化物对应水化物的酸性
C、比较这两种元素的气态氢化物的稳定性
D、比较这两种元素的单质与氢气化合的难易
-
(4) X、Y、Z、W四种元素组成的某无机盐,既可与盐酸反应,又可以与NaOH溶液反应,其化学式为 ,在这四种元素中,一种元素的单质在加热时能够与另外三种元素组成的具有强氧化性的化合物反应,写出该反应的化学方程式:
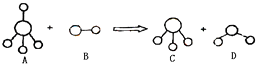
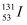 是常规核裂变产物之一,可以通过测定大气或水中
是常规核裂变产物之一,可以通过测定大气或水中 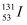 的含量变化来检测核电站是否发生放射性物质泄漏.下列有关
的含量变化来检测核电站是否发生放射性物质泄漏.下列有关 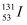 的叙述中正确的是( )
的叙述中正确的是( )
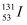 的原子核内中子数多于质子数
B .
的原子核内中子数多于质子数
B . 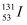 的原子序数为131
C .
的原子序数为131
C . 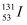 的原子核外电子数为78
D .
的原子核外电子数为78
D . 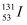 的化学性质与
的化学性质与 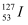 不同
不同

-
(1) X元素组成的单质的分子式是,若X元素的原子核内中子数和质子数相等,则X元素组成的单质的摩尔质量为,是晶体。
-
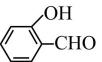
(2) Y元素的名称是,其氢化物的沸点(填“高于”“低于”或“无法确定”)氯化氢。
-
(3) Z元素组成的单质的晶体类型属于,Z的氢化物和氧化物反应的化学方程式为。
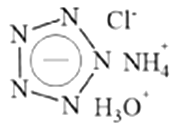
 B . 该盐中氮元素的化合价均为-3价
C . 该盐遇强碱能释放出NH3
D . 该盐中五氮阴离子具有还原性
B . 该盐中氮元素的化合价均为-3价
C . 该盐遇强碱能释放出NH3
D . 该盐中五氮阴离子具有还原性
钴及其化合物有着广泛的应用前景。回答下列问题:
-
(1) 基态Co原子的核外电子排布式为.
-
(2) 以无水乙醇作溶剂,Co(NO3)2可与某多齿配体结合形成具有催化活性的配合物,其结构简式如下图所示。
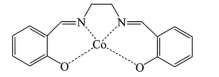
①配合物中提供孤对电子的原子是(填元素符号);
②该多齿配体中所含元素电负性由大到小的顺序为(填元素符号):
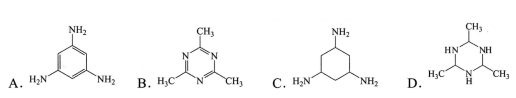
③下列化合物与上述配合物中C和N原子的杂化类型均相同的是(填标号)。
-
(3) 亚硝酸钴钠可与K+结合形成
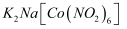 ,从而实现对K+的定量测定。
,从而实现对K+的定量测定。 ①
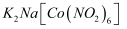 中存在的化学键类型有(填标号);
中存在的化学键类型有(填标号);A.金属键 B.离子键 C.极性共价键 D.配位键
②与亚硝酸根互为等电子体的化合物有(写一种)。
-
(4) Co与Ca属于同一周期,且最外层电子数相同,但金属Co的熔点、沸点均比金属Ca的高,原因是。
-
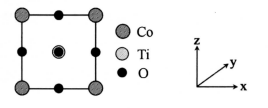
(5) 某种铁酸钴(CoTiO3)晶胞沿x、y或z轴任意一个方向的投影如下图所示。晶胞中Co处于各顶角位置,则O处于 位置,与Co紧邻的O的个数为。若晶胞中Co与O的距离为a nm,阿伏加德罗常数的值为NA,该晶体的密度为g.cm-3(列出计算式)。
-
(1) 基态P原子的价电子排布式为。
-
(2) 磷的一种同素异形体——白磷(P4)的空间构型为,其键角为,推测其在CS2中的溶解度 (填“大于”或“小于”)在水中的溶解度。
-
(3) 膦(PH3)和氨(NH3)的键角分别为93.6°和107°,试用价层电子对互斥理论分析PH3的键角小于NH3的原因:。
-
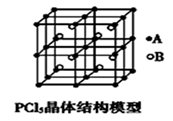
(4) 常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如图所示,由A、B两种微粒构成。将其加热至148℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CCl4、SF6互为等电子体,则A、B的化学式分别为、,A的中心原子杂化轨道类型为。
-
(5) 第三周期主族元素中,按第一电离能大小排序,第一电离能在磷和铝之间的元素是(填元素符号)。
-
(6) 氮化硼、氮化铝、氮化镓的结构类似于金刚石,熔点如下表所示。试从结构的角度分析它们熔点不同的原因:。
物质
BN
AlN
GaN
熔点/℃
3000
2200
1700
①苯 ②四氯化碳 ③溴苯 ④植物油 ⑤乙酸乙酯 ⑥硝基苯
| 选项 | 目的 | 分离方法 | 原理 |
| A. | 分离苯和苯酚 | 加浓溴水过滤 | 苯酚与浓溴水反应生成白色沉淀 |
| B. | 分离乙酸乙酯和乙醇 | 分液 | 乙酸乙酯和乙醇的密度不同 |
| C. | 除去乙烯中混有的SO2 | 酸性KMnO4溶液洗气 | SO2能被酸性KMnO4溶液氧化生成SO42— |
| D. | 除去丁醇中的乙醚 | 蒸馏 | 丁醇与乙醚的沸点相差较大 |
 B . 熔点:金刚石>硅单质
C . 沸点:水晶>氯化锂
D . 热分解所需温度:
B . 熔点:金刚石>硅单质
C . 沸点:水晶>氯化锂
D . 热分解所需温度: 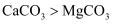
 、
、 、
、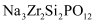 是常用的固体电解质。回答下列问题:
是常用的固体电解质。回答下列问题:
-
(1) 基态Si的电子排布式为。
-
(2) Zr的原子序数为40,位于周期表的第周期ⅣB族。
-
(3)
 、
、 、
、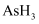 的沸点由高到低的顺序是。
的沸点由高到低的顺序是。
-
(4) 亚磷酸
 是磷元素的一种含氧酸,与NaOH反应只生成
是磷元素的一种含氧酸,与NaOH反应只生成 和
和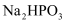 两种盐,则
两种盐,则 分子的结构式为,其中P原子的杂化方式为。
分子的结构式为,其中P原子的杂化方式为。
-
(5) Ti能形成化合物
 , 该化合物中
, 该化合物中 的配位数为,在该化合物中不含(填标号)。
的配位数为,在该化合物中不含(填标号)。A.
 键 B.
键 B. 键 C.配位键 D.离子键 E.极性键 F.非极性键
键 C.配位键 D.离子键 E.极性键 F.非极性键 -
(6) 我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为
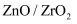 固溶体。四方
固溶体。四方 晶胞如图所示。A原子的坐标为
晶胞如图所示。A原子的坐标为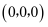 , B原子的坐标为
, B原子的坐标为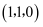 , 则C原子的坐标为。该晶体密度为
, 则C原子的坐标为。该晶体密度为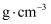 (写出表达式)。在
(写出表达式)。在 中掺杂少量ZnO后形成的催化剂,化学式可表示为
中掺杂少量ZnO后形成的催化剂,化学式可表示为 , 则
, 则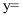 (用x表达)。
(用x表达)。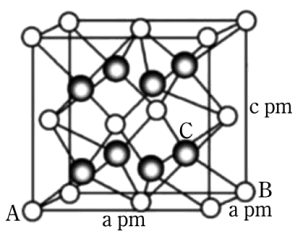
 具有易液化、含氢密度高、应用广泛等优点,
具有易液化、含氢密度高、应用广泛等优点, 的合成及应用一直是科学研究的重要课题。
的合成及应用一直是科学研究的重要课题。
-
(1) 以
 合成
合成 , Fe是常用的催化剂。
, Fe是常用的催化剂。①基态Fe原子的电子排布式为。
②实际生产中采用铁的氧化物
 , 使用前用
, 使用前用 和
和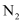 的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:
的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下: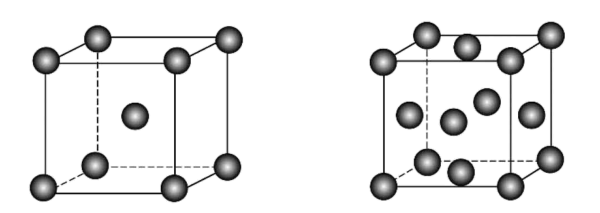
两种晶胞所含铁原子个数比为。
③我国科学家开发出
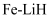 等双中心催化剂,在合成
等双中心催化剂,在合成 中显示出高催化活性。第一电离能(I1):
中显示出高催化活性。第一电离能(I1):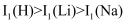 , 从原子结构角度解释原因是。
, 从原子结构角度解释原因是。 -
(2) 化学工业科学家侯德榜利用下列反应最终制得了高质量的纯碱。

①1体积水可溶解1体积
 , 1体积水可溶解约700体积
, 1体积水可溶解约700体积 。
。 极易溶于水的原因是。
极易溶于水的原因是。②
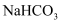 分解
分解 。
。 空间结构为。
空间结构为。
 , 是因为其范德华力更大
B .
, 是因为其范德华力更大
B .  的热稳定性大于
的热稳定性大于 , 是因为键能O-H比S-H大
C . NaCl熔点大于KCl,是因为晶格能NaCl比KCl大
D .
, 是因为键能O-H比S-H大
C . NaCl熔点大于KCl,是因为晶格能NaCl比KCl大
D . 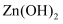 溶于氨水,是因为Zn2+能和
溶于氨水,是因为Zn2+能和 形成稳定的
形成稳定的
-
(1) X、Y、W的第一电离能由大到小的顺序是 (填字母对应的元素符号)。
-
(2) 已知元素Z的某钾盐(KH2ZO4)是其酸(H3ZO2)的正盐,则酸H3ZO2的结构式为 (元素Z用对应的元素符号书写)。
-
(3) 已知元素X、Z相关键的键能(kJ•mol-1)如表:从能量角度看,X元素形成的单质以X2、而Z元素形成的单质Z4(结构式可表示为
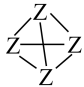 )形式存在的原因是。
)形式存在的原因是。X—X
X≡X
Z—Z
Z≡Z
193
946
197
489
-
(4) 元素W的含氧酸根离子(WO
 )的空间构型为,与之互为等电子体的阴离子有 (写出一种离子符号;等电子体指化学通式相同且价电子总数相等的分子或离子)。
)的空间构型为,与之互为等电子体的阴离子有 (写出一种离子符号;等电子体指化学通式相同且价电子总数相等的分子或离子)。
-
(5) 对于基态Q原子,下列叙述正确的是____ (填标号)。A . 遵循能量最低原理,核外电子排布应为[Ar]3d94s2 B . 排布在外层的电子总是比排布在内层的电子离核更远 C . 电负性比钾高,原子对键合电子的吸引力比钾大 D . 电子先排入4s轨道,再排进3d轨道,故3d轨道的电子能量比4s高
-
(6) 向盛有QSO4水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液。分离出所得溶质化合物[Q(NH3)4(H2O)2]SO4 , 然后加热该化合物固体,首先失去的组分是,理由是。
- 在这些书法作品中,黄庭坚的作品是( )
- 如图4-5-2所示,一根金属棒绕其中心顺时针转动,并与一通电直导线同面,则( )图4-5-2A.棒与导线平行时,棒
- 如图,在平面直角坐标系中,正方形的两直角边分别在坐标轴的正半轴上,分别过,的中点,作,的平行线,相交于点,已知. (1)
- 民族区域自治制度是我国的基本政治制度。实行民族区域自治制度,意味着() ①自治机关享有经济、文化和立法自治权 ②自治地方
- 阅读下面的文章,回答问题。 一张安稳的睡床 ①他们或许是这个城市最先感到天气转冷的一群人。霜降过后的某个中午,在北京城铁
- 希腊历史学家希罗多德说,克利斯提尼“领着人民参与政治”。克利斯提尼改革中符合这一评述的是( )
- 地球表面海陆面积之比是( ) A.5:5 B.3:7 C.7:3
- 读气候资料图,回答下列小题图中①气候类型为 A.温带季风气候 B.地中海气候 C.亚热带季风气候 D.温带
- (10福建南安6.)初三(1)班的小朱人称“小马虎”,下面是从他的笔记中摘录的部分化学用语,你认为正确的是A.碳酸钾:K
- “天宫一号”使用镍氢电池供电。镍氢电池的负极材料为储氢合金(用—表示,氢以单原子填入合金晶格),总反应为,下列说法正确的
- 2008奥运吉祥物福娃,其外材为纯羊毛线,内充物为无毒的聚酯纤维(如图)。下列说法正确的是A.羊毛与聚酯纤维的化学成分相
- 社科院12月15日发布2011年《社会蓝皮书》指出,预计2010年国内生产总值总额将突破37万亿元;12月27日,全国财
- What will people die of 100 years from now? If you think tha
- 阅读下面的文言文,完成下题。 王羲之起家秘书郎。复授护军将军。羲之既拜护军,又苦求宣城郡,不许。 乃以为右军将军、会稽内
- 武汉某经贸团代表赴东南亚采购货物,下列产品最有可能出现在订货合同中的是( ) A、棉花、小麦 B、蔬菜
- 在平面直角坐标系中,从六个点:A(0,0)、B(2,0)、C(1,1)、D(0,2)、E(2,2)、F(3,3)中任取三
- 2012年,19个省市对口援疆资金总规模超过100亿元。同时,通过转移支付、专项资金等渠道,中央投入资金规模将数倍于对口
- Salem, the “City of Peace”, is a small city with a big histo
- Riding a London subway, a person fromother countries will no
- 下列关于细胞内ATP的叙述中,正确的是 A.每个ATP分子含有3个高能磷酸键 B.每个ATP分子含有2个磷



