物质的结构与性质之间的关系 知识点题库
下列有关物质结构和性质的说法中,正确的是( )
A . 元素非金属性Cl>S的实验依据是酸性HCl>H2S
B . 碳元素的电负性小于氧元素,每个CO2分子中有4个σ键
C . 同周期主族元素的原子形成的简单离子的电子层结构一定相同
D . C、N、O三种元素,其第一电离能由大到小的顺序为N>O>C
下列说法正确的是( )
A . C和Si属于第ⅣA族元素,C非金属性比Si强,CO2、SiO2均是酸性氧化物
B . Na2O2与水反应,红热的Fe与水蒸气反应均能生成碱
C . NaHCO3、Na2CO3两种固体分别加热后均有气体生成
D . 氮、硫的单质及其氢化物在一定条件下均可与氧气反应,都直接生成NO2、SO2
已知磷酸分子中的三个氢原子都可以跟重水分子(D2O)中的D原子发生氢交换.又知次磷酸(H3PO2)也可跟D2O进行氢交换,但次磷酸钠(NaH2PO2)却不能跟D2O发生氢交换.由此可推断出H3PO2的分子结构是( )
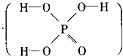
A . 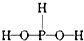 B .
B . 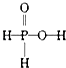 C .
C . 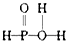 D .
D . 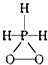
 C .
C .
下列说法正确的是( )
A . 胶体区别于其他分散系的本质特征是胶体可发生丁达尔效应
B . 在一定温度和压强下,气体体积主要取决于气体分子之间的平均间距
C . 摩尔质量与物质的量的多少有关,它等于物质的质量除以物质的量
D . 确定物质中是否含有C、H、O、N、Cl、Br、S等元素可用元素分析仪,确定物质中是否含有哪些金属元素可用原子吸收光谱
下列关于甲烷的叙述中不正确的是( )
A . 甲烷是烃类物质中相对分子质量最小的物质
B . 1 mol CH4在光照条件下最多能与4 mol Cl2反应
C . 甲烷的二氯代物只有一种结构可以证明甲烷为正四面体结构
D . 甲烷与空气的体积比为1∶2时,混合气体点燃爆炸最剧烈
元素周期表中,除了22种非金属元素外,其余的都是金属,请根据元素周期表回答下列问题:
-
(1) I.基态氮原子核外共有种运动状态不相同的电子,该原子核外电子排布中电子在能量最低的轨道呈形,用n表示能层,氟元素所在族的外围电子排布式为。
-
(2) 在元素周期表中,某些主族元素与下方的主族元素的性质有些相似,被称为“对角线规则”,如下表:
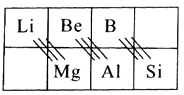
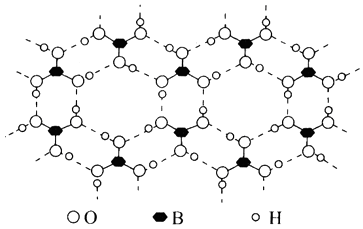
根据“对角线规则”写出Be(OH)2与NaOH反应的离子方程式,硼酸(H3BO3)是一种具有片层结构的白色晶体,层内的H3BO3分子间通过氢键相连(如图)。含1mol H3BO3的晶体中有mol氢键,H3BO3中B原子的杂化类型为。
-
(3) 以第二周期为例,除Be、N外,其它元素的第一电离能从左到右逐渐增大的原因是。
-
(4) II.近年来铁及其化合物在工农业中有广阔的应用前景。
铁的一种络离子[Fe(CN)6]4-中Fe2+的配位数为6,该络离子中不存在______(填序号)。
A . 共价键 B . 非极性键 C . 配位键 D . δ键 E . π键 -
(5) AlCl3的熔点比NaCl熔点低的原因是。
-
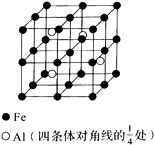
(6) 一种Al-Fe合金的立体晶胞如图所示。若晶体的密度为ρ g∙cm-3 , 则此合金中最近的两个Fe原子之间的距离为cm(用含ρ的代数式表示)。
化学与生活、生产和社会可持续发展密切相关。下列说法正确的是()
A . 高纯二氧化硅可用作计算机芯片的材料
B . 硅胶、铁粉均可作为食品包装中的抗氧化剂
C . 氯化铝是工业上电解法冶炼金属铝的原料
D . “地沟油”可用来制肥皂和生物柴油
化学与环境密切相关,下列有关说法正确的是( )
A . 酸雨是pH小于7的雨水
B . CO2、SO2、NO2都会导致酸雨的形成
C . 目前工业废气脱硫应用最广泛的方法是石灰法
D . 我国重点城市近年发布“空气质量日报”列入的首要污染物包括SO2、NO2、可吸入颗粒物和CO2
下列溶液分别与碳酸钠溶液混合后不能产生沉淀的是( )
A . 氢氧化钙溶液
B . 氢氧化钡溶液
C . 氢氧化钠溶液
D . 氯化钙溶液
化学与生活、社会发展息息相关。下列有关说法错误的是( )
A . “霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应
B . “曾青(硫酸铜)涂铁,铁赤色如铜”,过程中发生了置换反应
C . “外观如雪,强烧之,紫青烟起”,该过程中利用了焰色反应
D . 医用酒精体积分数是75%,用医用酒精灭菌消毒是利用强氧化性使细菌、病毒死亡
下列关于化学的文献,理解正确的是( )
A . 《咏石灰》中“…烈火焚烧若等闲,…要留清白在人间”,其中“清白”指的是氢氧化钙
B . 《肘后备急方》中“青蒿一握,以水二升渍,绞取汁”,该提取过程属于化学变化
C . 《抱朴子》中“丹砂(HgS)烧之成水银,积变又还成丹砂”,描述的是升华和凝华过程
D . 《本草纲目》中“用浓酒和糟入甑,蒸令气上,用器承滴露”,涉及的实验操作是蒸馏
我国科学家首次抓住“兔耳朵”解密催化反应“黑匣子”。图a是TiO2结构图,图b是TiO2吸附H2O后形成“兔耳朵”的结构图,图c是图b的俯视图。下列叙述错误的是( )
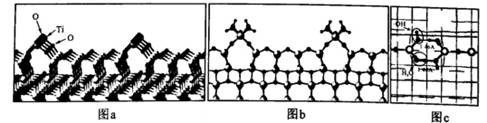
A . 由图a可知,每隔4个Ti原子会有一列凸起
B . 由图b可知,凸起位置上的Ti原子是反应的活性位点
C . 由图c可知,水分子和羟基之间靠共价键结合
D . 将CO引人体系,通过观察凸起结构变化,证实水煤气变换催化反应的发生
填写下列空白:
-
(1) 写出表示含有8个质子、10个中子的原子的化学符号:。
-
(2) 周期表中位于第8纵行的铁元素属于第族。
-
(3) 下列几种物质:①Ca(OH)2②H2O2③He④H2S ⑤MgCl2 ,只含有离子键的是(选填序号,下同);只含有极性共价键的化合物是;
-
(4) HClO的结构式,I2的电子式。
-
(5) 下列变化中:①干冰气化;②硝酸钾熔化;③KHSO4熔融;④蔗糖溶液水⑤硫酸溶于水;未破坏化学键的是 ;
-
(6) 下列不能说明氯元素原子得电子能力比硫元素原子得电子能力强的是
①HCl的溶解度比H2S的大 ②HCl的酸性比H2S的强 ③HCl的稳定性比H2S的强④Cl2与铁反应生成FeCl3 , 而S与铁反应生成FeS ⑤HClO4的酸性比H2SO4的强 ⑥Cl2能与H2S反应生成S
-
(1) 比较酸性条件下得电子能力的相对强弱:HClOCl2(填“>”、“<”或“=”),用一个离子方程式表示:。
-
(2) NaCNO是离子化合物,各原子均满足8电子稳定结构,NaCNO的电子式是。
-
(3) 相同温度下,冰的密度比水小的主要原因是。
1875年科学家布瓦博德朗发现了一种新元素,命名为“镓”,它是门捷列夫预言的元素类铝。Ga(镓)和As(砷)在周期表的位置如图,下列说法错误的是( )
| Al | P | |
| Ga | As |
A . Ga的原子序数为31
B . 碱性:Al(OH)3 <Ga(OH)3
C . 简单离子半径r(Ga3+)>r(As3-)>r(P3-)
D . GaAs可制作半导体材料,用于电子工业和通讯领域
化学与生产、生活密切相关。下列说法不正确的是( )
A . 我国“蛟龙”号载人潜水器供人活动的耐压球壳是用钛合金制造的,钛合金球壳直径2米,壁厚105毫米,可承受万米深海压强
B . 合理利用太阳能、风能和氢能等能源有利于实现“低碳经济”
C . 蒸馒头时,在发酵的面团里加入一些小苏打可使馒头松软
D . “天问一号”火星探测器装有太阳能电池板,其主要材料是二氧化硅
下列有关叙述不正确的是( )
A . 分子、原子和离子是构成物质的基本微粒
B . 带有单电子的原子或原子团是自由基
C . 一个非可逆化学反应是一个基元反应
D . 处于最低能量状态的原子是基态原子
人类对第二周期的元素及化合物认识最早。
-
(1) 第二周期的元素中,I1(第一电离能)从大到小排前三位的是。
-
(2) 人类合成的第一个稀有气体化合物是XeF+PtF
 , PtF
, PtF 中的键角有90°和180°两种。下列关于该化合物的说法中正确的是____。
A . 熔化状态下不能导电 B . XeF+中所有原子都满足8电子稳定结构 C . 用两个Cl替换F后,所得PtF4Cl2有两种结构 D . 含有离子键、极性键、非极性键和配位键
中的键角有90°和180°两种。下列关于该化合物的说法中正确的是____。
A . 熔化状态下不能导电 B . XeF+中所有原子都满足8电子稳定结构 C . 用两个Cl替换F后,所得PtF4Cl2有两种结构 D . 含有离子键、极性键、非极性键和配位键 -
(3) XeF+PtF
 溶于水可生成Xe和HPtF6 , 写出反应的化学方程式。。
溶于水可生成Xe和HPtF6 , 写出反应的化学方程式。。
-
(4) 解释HNO3和HNO2酸性强弱不同的原因。
-
(5) SCN—中C原子的杂化类型为, 其中含有两个相同的大π键,其形式为。(用π
 表示,n为原子数,m为电子数),检验Fe3+时,SCN—以 S原子配位不以N原子配位的原因是。
表示,n为原子数,m为电子数),检验Fe3+时,SCN—以 S原子配位不以N原子配位的原因是。
-
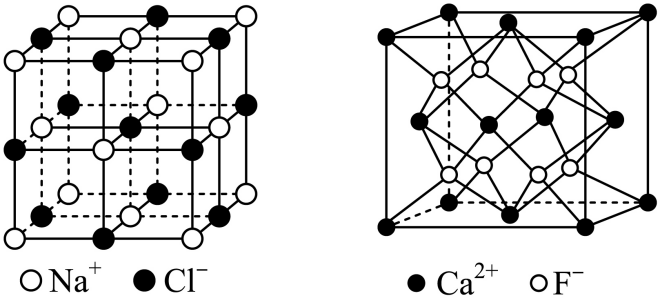
(6) 如图,在NaCl的晶体中,Na+和Cl—互相占据对方的正八面体空隙,CaF2晶体中,F—占据由Ca2+构成的所有正四面体空隙。钛镍合金具有形状记忆功能。某钛、镍原子个数比为2:1的合金的晶体结构为:镍原子呈面心立方排列,钛原子填充在由镍原子围成的所有八面体空隙和一半的四面体空隙中,若最近的钛原子和镍原子紧密接触,镍原子周围距离最近的钛原子数为; 钛原子和镍原子的半径分别为r1和r2 , 该晶体的空间利用率为(用含r的代数式表示,不必化简,空间利用率=晶胞中原子的总体积/晶胞的体积)。
下列关于物质结构及元素周期表的说法错误的是( )
A . IIA族基态原子最外层电子排布均为ns2
B . 第三、四周期同主族元素的原子序数均相差8
C . 2p轨道上有三个未成对电子的X原子与3p轨道上有三个未成对电子的Y原子化学性质相似
D . C、H、O三种元素的电负性由小到大的顺序为H<C<O
X、Y为第三周期元素,Y最高正价与最低负价的代数和为6,二者形成的一种化合物在固态时以[XY4]+[XY6]-的形式存在。下列说法正确的是( )
A . 该化合物中含有离子键和共价键,为共价化合物
B . 简单氢化物的稳定性:X>Y
C . 同周期元素氧化物对应的水化物中,Y元素氧化物对应水化物的酸性最强
D . 阴离子[XY6]-和阳离子[XY4]+中,X原子杂化方式和离子空间构型均不相同
最近更新
- (13分)请认真阅读下列三个反应:利用这些反应,按以下步骤可从某烃A合成一种染料中间体DSD酸:请写出A、B、C、D的结
- 美国国务卿马歇尔曾提出的“欧洲复兴计划”宣称:“我们的政策的目的是恢复世界上行 之有效的经济制度,从而使自由制度赖以存在
- 在△ABC中,已知AB=,AC边上的中线BD=,求sinA的值.
- 氢化钙(CaH2)固体可用于登山队员的能源提供剂,与氢气做能源相比它的优点是
- Daredevil climber Alain Robert, known as the French Spiderma
- 读表,回答8-9题。 8. 表中①②③④所对应的地区分别是( ) A. 东南、西南、华北、西北
- 10.对下面的这首唐诗理解不正确的一项是( )(2分) 凉州词 王之涣 黄河远上白云间,一片
- 若=1,则cos2θ的值为………………………………( )(A)
- 已知口袋中有大小相同的m个红球和n个白球,m≥n≥2,从袋中任意取出两个球.(1)若m=4,n=3,求取出的两个球中至少
- 运用溶解度表与溶解度曲线回答下列问题:(1)氯化钠的溶解度曲线是 (填“A”或“B”)。 (2)60
- 假设2050年1月1日,人类在距离地球50亿光年的地方,发现一颗与地球一样存在生命的行星。关于该行星的叙述,可能性较小的
- The suggestion ________ by the teacher is available. A. putf
- 京剧的主要唱腔是“西皮”和“二黄”,这说明京剧最早是受什么地方的戏剧影响而形成的() A.北京 B.河北、河南 C.江
- (16届安徽省舒城晓天中学九年级上学期第一次月考)综合性学习。 随着手机的逐渐普及,越来越多的中学生开始使用手机,有些同
- 若航空母舰上的直升机垂直于甲板匀加速飞行到高度为H的天空,如果加速度a和每秒钟的耗油量Q之间的关系是Q=a·α+β(α、
- 下列情况中,不属于染色体变异的是( ) A.用花药培养出了单倍体植株 B.第5号染色体短臂缺失引起
- We all write ______, even when there’s not much to say. A. n
- 如图所示电路中,R为电阻箱,电源的电动势为E,内阻为r。当调节电阻箱使外电阻分别为R1、R2时,其功率相等。此时对应的电
- 下列含氯元素的物质中,氯元素的化合价由低到高的一组是( ) A、Cl2、CaCl2、NaClO B、Ca
- 下列加线字的读音全部相同的一组是( ) A.脊jǐ 山脊 脊髓 脊梁



