物质的结构与性质之间的关系 知识点题库
下图是已经合成的最著名硫-氮化合物分子结构。下列说法正确是( )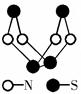
(1)写出元素符号:W为 ,X为 ,Y为 ,Z为 .
(2)W2Z是由 键组成的分子,其电子式为 .
(3)由Y、X、W组成的物质是 键和 键组成的 化合物.
-
(1) 镓元素位于元素周期表的周期族,砷原子核外的电子有种运动状态。
-
(2) Si、P、S 的第一电离能由大到小的顺序是 , 二氧化硅和干冰晶体的熔点差别很大,其原因是。
-
(3) 与AsF3互为等电子体的分子为(只写一中),其空间构型为。
-
(4) 硼酸(H3BO3)本身不能电离出H+ , 在水溶液中易结合一个OH-生成[B(OH)4]- , 而体现弱酸性。
①[B(OH)4]-中B原子的杂化类型为。
②[B(OH)4]-的结构式为。
-
(5) 金刚石的晶胞如图所示,
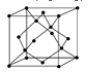
若以硅原子代替金刚石晶体中的碳原子,便得到晶体硅;若将金刚石晶体中一半的碳原子换成硅原子,且碳、硅原子交替,即得到碳化硅晶体(金刚砂)。①金刚石、晶体硅、碳化硅的熔点由高到低的排列顺序是(用化学式表示);
②金刚石的晶胞参数为a pm(1 pm=10-12 m)。 金刚石晶胞的密度为g/cm3(只要求列算式,阿伏加德罗常数为NA)。
-
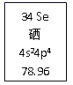
(1) Se元素在周期表中的位置为。表中78.96的意义为。Se原子最外层电子排布的轨道表示式为。
-
(2) 从原子结构角度解释硫的非金属性大于硒。
-
(3) 硒化氢(H2Se)是一种有恶臭味的有毒气体,是一种(选填“极性、或非极性”)分子,其空间结构为型。
-
(4) 工业上常用浓H2SO4焙烧CuSe的方法提取硒,反应产生SO2、SeO2的混合气体,写出反应的化学方程式。理论上该反应每转移1mol电子,可得到SeO2的质量为g,得到SO2在标准状况下的体积为 L。
| 选项 | 规律 | 结论 |
| A | 较强酸可以制取较弱酸 | 次氯酸溶液无法制取盐酸 |
| B | 反应物浓度越大,反应速率越快 | 常温下,相同的铝片中分别加入足量的浓、稀硝酸,浓硝酸中铝片先溶解完 |
| C | 结构和组成相似的物质,沸点随相对分子质量增大而升高 | CH4沸点低于C2H6 |
| D | 活泼金属做原电池的负极 | Mg-Al—NaOH构成原电池,Mg做负极 |
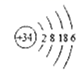
① 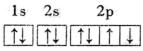 该原子的电子排布图,最外层违背了洪特规则
该原子的电子排布图,最外层违背了洪特规则
②处于最低能量状态原子叫基态原子,1s22s22px1→1s22s22py1过程中形成的是发射光谱
③运用价层电子对互斥理论,CO32-离子的空间构型为三角锥型
④具有相同核外电子排布的粒子,化学性质相同
⑤NCl3中N-Cl键的键长比CCl4中C-Cl键的键长短
-
(1) Sn为ⅣA族元素,单质Sn与干燥Cl2反应生成SnCl4。常温常压下SnCl4为无色液体,SnCl4空间构型为,其固体的晶体类型为。
-
(2) NH3、PH3、AsH3的沸点由高到低的顺序为(填化学式,下同),还原性由强到弱的顺序为,键角由大到小的顺序为。
-
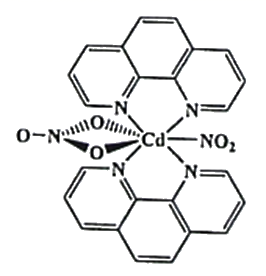
(3) 含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种Cd2+配合物的结构如图所示,1mol该配合物中通过螯合作用形成的配位键有mol,该螯合物中N的杂化方式有种。
-
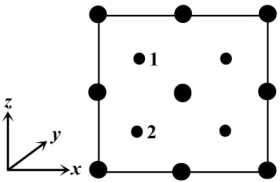
(4) 以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系CdSnAs2的晶胞结构如图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如下表所示。
坐标
原子
x
y
z
Cd
0
0
0
Sn
0
0
0.5
As
0.25
0.25
0.125
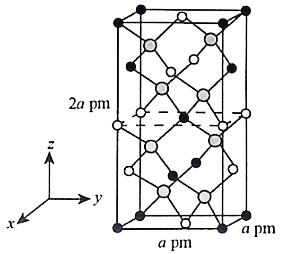
一个晶胞中有个Sn,找出距离Cd(0,0,0)最近的Sn(用分数坐标表示)。CdSnAs2
晶体中与单个Sn键合的As有个。
-
(1) 基态P原子中,电子占据的最高能级符号为,基态N原子核外有种运动状态不同的电子。
-
(2) C、N、O三种元素电负性从大到小的顺序为;第一电离能χ(P)χ(Cl)(填“>”或“<”)。
-
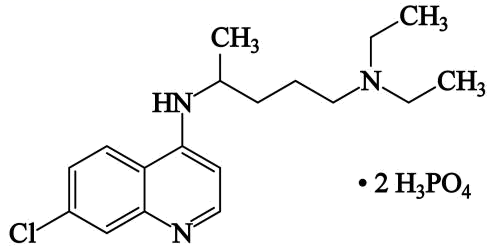
(3) 磷酸氯喹中N原子的杂化方式为,NH3是一种极易溶于水的气体,其沸点比AsH3的沸点高,其原因是。
-
(4) GaN、GaP、GaAs都是很好的半导体材料,晶体类型与晶体碳化硅类似,熔点如表所示,
GaN
GaP
GaAs
熔点/℃
1700
1480
1238
①GaN、GaP、GaAs的熔点变化原因是。
②砷化镓晶体中含有的化学键类型为(填选项字母)。
A.离子键 B.配位键 C.σ键 D.π键 E.极性键 F.非极性键
③以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置。称作原子分数坐标。如图为沿y轴投影的磷化镓晶胞中所有原子的分布图。若原子1的原子分数坐标为(0.25,0.25,0.75),则原子2的原子分数坐标为;若磷化镓的晶体密度为ρg·cm-3 , 阿伏加德罗常数的值为NA , 则晶胞中Ga和P原子的最近距离为pm(用代数式表示)。
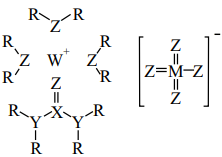
 呈四面体
D . 最高价氧化物对应水化物的酸性:Y<X
呈四面体
D . 最高价氧化物对应水化物的酸性:Y<X
- 如图所示是一个测量仪表的示意图,根据图中所示的信息,此时读数为_________kW·h.小云利用该电表 测定家中电热取
- 阅读下面的文字,完成后面题目。 生命的节奏与教育的节奏 ①学校生活是一段生命的旅程,教育则是一场深入生命的探险。那些
- (09年长沙一中一模文)刘、李两家夫妇各带1个小孩一起到公园游玩,购票后排队依次入园.为安全起见,首尾一定要排两位爸爸,
- 下图是“有关工业与其污染”示意图,正确的排序是 A.①电镀厂②冶炼厂③飞机场④水泥厂B.①冶炼厂②电镀厂③水泥厂④飞机场
- 下列物质不易被氧化、不易分解,且能存放在玻璃试剂瓶中的是( ) A.氯水 B.KI溶液
- 下列疾病由病毒引起的是( ) A.肺炎 B.菌痢 C.艾滋病 D.
- The practice of magic includes special words,actions, and ob
- 选修4-5:不等式选讲 已知函数 (1)若不等式的解集为,求实数a,m的值。 (2)当a=2时,解关于
- 美国的全球卫星定位系统(简称GPS)由24颗卫星组成,卫星分布在等分地球的6个轨道平面上,每个轨道上又分布有4颗卫星,这
- 地面的观察者看雨滴是竖直下落的,坐在匀速行驶的列车车厢中的乘客看雨滴是() A.水平向前运动 B.水平向后运动 C.倾斜
- 小明以“繁荣与开放的唐朝”为主题进行探究,下列他整理的内容中不符合史实的是( ) A.已普遍使用最先进的活字印
- While I was waiting outside my wife’s office building for he
- 三个体积相同的实心木球,铁球和铜球(ρ木<ρ铁<ρ铜),放入装有水银的容器中后,都漂浮在水银面上,则下列说法
- 依据下列的句式,试各举一例,完成整个语段。 古往今来,大凡有所建树者,无不是临渊之后而退而结网者。如果哥伦布只是“临渊羡
- Thinking that the students were having an evening class, the
- 该气象观测点观测到下表所列的一次天气变化过程: 1月1日1月2日1月3日气温(℃)最高气温251513最低气温1020平
- 如果ax2+2x+=(3x+)2+m,则a,m的值分别是( ) A.6,0 B.9,0
- 300 mL某浓度的NaOH溶液中含有60 g 溶质,现欲配制1 mol・L-1 的NaOH 溶液,应取原溶液与蒸馏水的
- 下列关于CO2 与CO 的不同点比较错误的是 ( ) A. 组成:一个二氧化碳分子比一个一氧化碳
- N2(g)+3H2(g) 2NH3(g)在体积不变的密闭容器中反应,下列叙述表示处于化学平衡状态的是() A.N2、H



