原子核外电子的运动状态 知识点题库
①电子层 ②电子亚层 ③电子云的伸展方向 ④电子的自旋状态.
-
(1) 镝(Dy)的基态原子电子排布式为[Xe]4f106s2 , 画出镝(Dy)原子外围电子排布图:。
-
(2) 高温超导材料镧钡铜氧化物中含有Cu3+ , 基态时Cu3+ 的电子排布式为。
-
(3) 观察下面四种镧系元素的电离能数据,判断最有可能显示+3 价的元素是(填元素名称)。几种镧系元素的电离能(单位:kJ • mol-1)
元素
I1
I2
I3
I4
Yb(镱)
604
1217
4494
5014
Lu(镥)
532
1390
4111
4987
La(镧)
538
1067
1850
5419
Ce(铈)
527
1047
1949
3547
-
(4) 元素铈(Ce)可以形成配合物(NH4)2[Ce(NO3)6]。
①组成配合物的四种元素,电负性由大到小的顺序为(用元素符号表示)。
②写出氮的最简单气态氢化物水溶液中存在的氢键:(任写一种)。
③元素Al 也有类似成键情况,气态氯化铝分子表示为(AlCl3)2 , 分子中Al 原子杂化方式为,分子中所含化学键类型有(填字母)。
a.离子键 b.极性键 C.非极性键 d.配位键
-
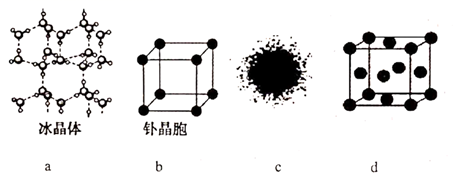
(5) PrO2(二氧化镨)的晶体结构与CaF2相似,晶胞中镨原子位于面心和顶点,则PrO2(二氧化镨)的晶胞中有个氧原子;已知晶胞参数为a pm,密度为ρ g· cm-3 , NA= (用含a、ρ的代数式表示)。
-
(1) Ga基态原子核外电子排布式为,As基态原子核外有个未成对电子。
-
(2) Ga、As、Se的第一电离能由大到小的顺序是,Ga、As、Se 的电负性由大到小的顺序是。
-
(3) 比较下列镓的卤化物的熔点和佛点,分析其变化规律及原因:。
镓的卤化物
GaI3
GaBr3
GaCl3
熔点/℃
77.75
122.3
211.5
沸点/℃
201.2
279
346
GaF3的熔点超过1000 ℃,可能的原因是。
-
(4) 二水合草酸镓的结构如图1所示,其中镓原子的配位数为,草酸根中碳原子的杂化轨道类型为。
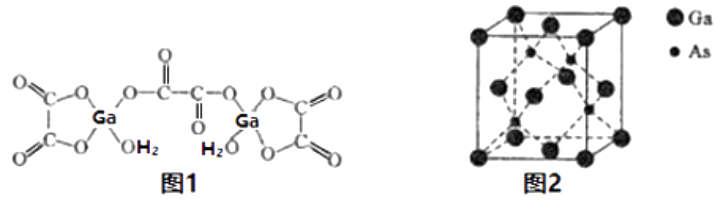
-
(5) 砷化镓的立方晶胞结构如图2所示,晶胞参数为a=0.565nm,砷化镓晶体的密度为g/ cm3(设NA为阿伏加德罗常数的值,列出计算式即可)。
-
(1) 铁在元素周期表中的位置。
-
(2) 配合物Fe(CO)n常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)n晶体属于(填晶体类型)。Fe(CO)n的中心原子价电子数与配体提供电子数之和为18,则n= 。Fe(CO)n在一定条件下发生反应:Fe(CO)n(s)
 Fe(s)+ n CO(g)。已知反应过程中只断裂配位键,则该反应生成物中新形成的化学键类型为。
Fe(s)+ n CO(g)。已知反应过程中只断裂配位键,则该反应生成物中新形成的化学键类型为。
-
(3) K3[Fe(CN)6]溶液可用于检验(填离子符号)。CN-中碳原子杂化轨道类型为,C、N、O三元素的第一电离能由大到小的顺序为(用元素符号表示)。
-
(4) 铜晶体的晶胞如图所示。
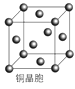
①基态铜原子的核外电子排布式为。
②每个铜原子周围距离最近的铜原子数目。
-
(5) 某M原子的外围电子排布式为3s23p5 , 铜与M形成化合物的晶胞如附图所示(黑点代表铜原子)。
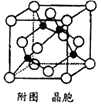
①该晶体的化学式为。
②已知该晶体的密度为g.cm-3 , 阿伏加德罗常数为NA , 则该晶体中铜原子和M原子之间的最短距离为pm(只写计算式)。
-
(1) F基态原子的核外电子排布式为。
-
(2) 在A、B、C三种元素中,第一电离能由小到大的顺序是(用元素符号回答)。
-
(3) 元素B的简单气态氢化物的沸点(填“高于”或“低于”)元素A的简单气态氢化物的沸点,其主要原因是。
-
(4) 由A、B、C形成的离子CAB−与AC2互为等电子体,则CAB−的结构式为。
-
(5) 由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为。
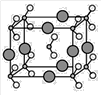
-
(6) FC在加热条件下容易转化为F2C,从原子结构的角度解释原因。
-
(1) N原子核外有 种不同运动状态的电子。基态N原子中,能量最高的电子所占据的原子轨道的形状为。
-
(2) 经测定发现,N2O5固体由NO2+ 和NO3-两种离子组成,该固体中N原子杂化类型为;与NO2+互为等电子体的微粒有(写出一种)。
-
(3) HF和HI电离出H+较难的是(填化学式,下同)。铵盐大多不稳定,请预测NH4F、NH4I中,较易分解的是。
-
(4) 第二周期中,第一电离能介于B元素和N元素间的元素为(填“元素符号”)。
-
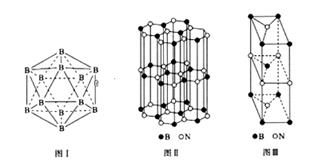
(5) 晶体硼有多种变体,但其基本结构单元都是由硼原子组成的正二十面体( 见图I),每个顶点为一个硼原子,每个三角形均为等边三角形。则每一个此基本结构单元由个硼原子构成;若该结构单元中有2 个原子为10B(其余为11B),那么该结构单元有种不同类型。
-
(6) 硼和氮构成的一种氮化硼晶体的结构与石墨晶体结构相类似,B、N原子相互交替排列(见图II),其晶胞结构如图III所示。该晶胞有个B和个N。
-
(1) 区分晶体硼和无定硼形科学的方法为。
-
(2) B原子基态的价层电子排布图中正确的是_______A .
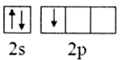 B .
B . 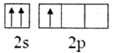 C .
C . 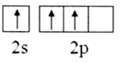 D .
D . 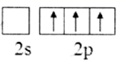
-
(3) NaBH4是重要的储氢载体,阴离子的立体构型为。
-
(1) 基态Ga原子价电子排布式,核外电子占据最高能级的电子云形状为;基态As原子最高能层上有个电子。
-
(2) 镓失去电子的逐级电离能(单位:kJ•mol-1)的数值依次为577、1985、2962、6192,由此可推知镓的主要化合价为和+3,砷的第一电离能比镓(填“大”或“小”)。
-
(3) 第四周期元素中,与基态As原子核外未成对电子数目相同的元素符号为。
-
(4) 砷化镓可由(CH3)3Ga和AsH3在700℃制得,(CH3)3Ga中C原子的杂化方式为,AsH3分子的空间构型为。
-
(5) 相同压强下,AsH3的沸点NH3(填“大于”或“小于”),原因为。
-
(6) GaAs为原子晶体,其晶胞结构如图所示,Ga与As以(填“共价键”或“离子键”)键合。设阿伏加德罗常数的值为NA , 该晶胞边长为a pm则GaAs晶体的密度为g•cm-3(列出计算式即可)。
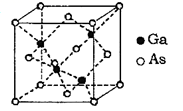
-
(1) 氟代硼酸钾中各元素原子的第一电离能大小顺序是F>O>。基态K+电子占据最高能级的电子云轮廓图为形。
-
(2) NaBH4是有机合成中常用的还原剂,其中阴离子的键角为。
-
(3) 下列硼原子电子排布图表示的状态中,能量最低和最高的分别为、(填字母标号)。
A.
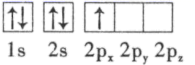 B.
B. 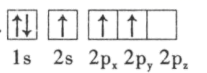
C.
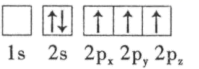 D.
D. 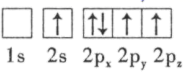
-
(4) 硼元素的简单氢化物BH3不能游离存在,常倾向于形成较稳定的B2H6或与其他分子结合。
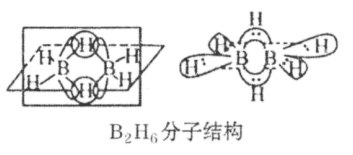
①B2H6分子结构如图,则B原子的杂化方式为。
②氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是,写出一种与氨硼烷互为等电子体的分子(填化学式)。
-
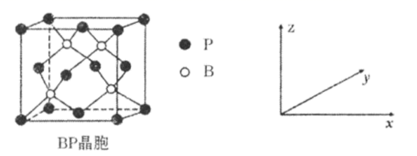
(5) 磷化硼(BP)是受高度关注的耐磨材料,可作为金属表面的保护层,其结构与金刚石类似,晶胞结构如图所示。P的配位数为,磷化硼晶胞沿z轴在平面的投影图中,B原子构成的几何形状是,已知晶胞边长为apm,则磷化硼晶体的密度是g·cm-3。
 )=0.2mol
C . 共价化合物中,电负性大的成键元素表现为负价
D . 两个p轨道之间只能形成π键,不能形成σ键
)=0.2mol
C . 共价化合物中,电负性大的成键元素表现为负价
D . 两个p轨道之间只能形成π键,不能形成σ键
-
(1) 基态Y原子价层电子排布式为。原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+
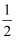 , 表示,则与之相反的用-
, 表示,则与之相反的用-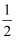 表示,这称为电子的自旋量子数。对于基态的Y原子,其价电子的自旋量子数代数和为。
表示,这称为电子的自旋量子数。对于基态的Y原子,其价电子的自旋量子数代数和为。
-
(2) X、Y、E三种元素的第一电离能由小到大的顺序为(填元素符号,下同);电负性由小到大的顺序为。
-
(3) X、Z和氢元素按原子数目比为1:1:2形成常温下呈气态的物质,其分子中键角约为,其中X原子的杂化轨道类型为。
-
(4) F2+与NH3能形成[F(NH3)4]2+离子,[F(NH3)4]2+中的配位原子为(填元素符号)。若[F(NH3)4]2+离子中2个NH3被2个Cl-替代可以得到2种不同的结构,则[F(NH3)4]2+离子的空间结构名称是。(填“平面四方形”或“正四面体”)。
-
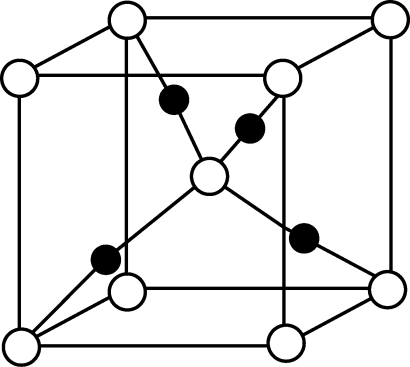
(5) F2Z的晶胞中(结构如图所示)所包含的F离子数目为。若其晶体密度为ρ g·cm-3 , F离子的半径为r1 pm,Z离子的半径为r2 pm,阿伏加德罗常数的值为NA , 则该晶胞中原子的空间利用率(即原子的体积占晶胞体积的百分率)为。(用含ρ、r1、r2、NA的代数式表示,列式即可,不需化简)。
-
(1) 基态铜原子有种运动状态不相同的电子,其价层电子排布式为。
-
(2) 已知铜与氯形成化合物的立方晶胞如下图所示。

①该晶体的化学式为。
②该晶体中,每个氯原子周围与它最近且等距离的氯原子有个。
-
(3)
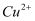 能与多种物质形成配合物,为研究配合物的形成及性质,某小组进行如下实验。
能与多种物质形成配合物,为研究配合物的形成及性质,某小组进行如下实验。序号
实验步骤
实验现象或结论
ⅰ
向
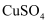 溶液中逐滴加入氨水至过量
溶液中逐滴加入氨水至过量产生蓝色沉淀,随后溶解并得到深蓝色的溶液
ⅱ
再加入无水乙醇
得到深蓝色晶体
ⅲ
测定深蓝色晶体的结构
晶体的化学式为

ⅳ
将深蓝色晶体洗净后溶于水配成溶液,再加入稀NaOH溶液
无蓝色沉淀生成
①深蓝色的配离子
 的结构简式:。
的结构简式:。②
 晶体中
晶体中 的中心原子杂化轨道类型为:。
的中心原子杂化轨道类型为:。③加入乙醇有晶体析出的原因:。
④该实验条件下,
 与
与 的结合能力(填“大于”“小于”或“等于”)
的结合能力(填“大于”“小于”或“等于”) 与
与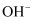 的结合能力。
的结合能力。⑤
 能与
能与 形成
形成 , 而
, 而 不能,其原因是。
不能,其原因是。
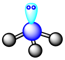 C . As的原子结构示意图:
C . As的原子结构示意图: 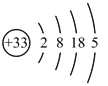 D . HCl的形成过程:
D . HCl的形成过程: 
- 实验室常采用分解H2O2的水溶液(MnO2作催化剂)的方法制取氧气。 (1) 写出用分解H2O2的水溶液(MnO2作催化
- 国内某企业家说:“我觉得我们企业家要负起自己的责任。我们最应该做的事情就是把自己的企业做好,为社会提供更好的产品和服务。
- 在国际贸易领域中,发达国家工业制成品的出口价格通常高于其价值,发展中国家的初级产品的出口价格则低于其价值。产生这种价格“
- 一个足球运动员用100N的力踢一个重为5N的足球,球离脚后在水平草地上向前滚动了30m.在球滚动的过程中,运动员对足球做
- They used to nod to each other when they met, and now and th
- (2011浙江省嘉兴,9,4分)一个纸环链,纸环按红黄绿蓝紫的顺序重复排列,截去其中的一部分,剩下部分如图所示,则被截去
- 有人说:“对于西方的挑战,中国的反应之所以迟钝,是由于中国社会在19世纪中叶面临很不寻常的历史环境。内部事务万分火急,至
- 下列各组词语中加点字的注音,完全正确的一组是( ) A.锃亮(zènɡ) 拓片(tuò) 同仇敌忾
- 国际文化交流中心将组织一次由各国学生参加的“和平、友谊”夏令营活动,要求报名者提交英文个人简历。假设你是王珊,请根据下列
- 要把木箱拉到斜面顶端,小明想办法把木箱放在小车上,用沿斜面方向的轻质细绳把车和木箱匀速拉上斜面顶端,如图所示,整个过程历
- 根据下表回答问题。温度/℃ 0 20 40 60 80 100 溶解度 (g/100g水) NaCl 35.7 36.0
- 1915年,陈独秀在某杂志的创刊号上发表了一篇激情喷涌的文章,称“青年如初春,如朝日……人生最可宝贵之时期也。”刊发该文
- 做“验证力的平行四边形定则”实验中,实验步骤如下:(1)在水平放置的木板上,固定一张白纸. (2)把橡皮条的一端固定在O
- 下列词语中加点的字,每对读音都不相同的一组是( ) A.纰缪/未雨绸缪 哥俩/肮脏伎俩 称职/称体裁
- 一容积恒定的密闭容器中盛有1molPCl5,加热到200℃时发生反应:PCl5(g)PCl3(g)+Cl2(g),反应达
- 阅读下面文言文,按要求答题。 子曰:“诵《诗三百》,授之以政,不达;使于四方,不能专对;虽多,亦奚以为?” (《论语·子
- 南美某地,每年有200多天被大雾笼罩。当地的居民制作“捕雾网”收集水资源(如图所示)。完成5-6题。5.该地的植被特点
- 若,则x的取值范围是______.
- 复数z1=3+i,z2=1-i,则z=z1·z2在复平面内对应的点位于( )A.第一象限 B.第二象限
- 在已调平衡的托盘天平两边各放一个等质量的烧杯,向烧杯中各倒入质量相等、质量分数也相等的足量的稀硫酸,分别在左、右两盘的烧



