原子核外电子的运动状态 知识点题库
(2)写出Ni的元素名称 ,该元素在周期表的位置为第 周期,第 族.
(3)第四周期基态原子中未成对电子数最多的元素是 ,该元素基态原子的价电子轨道表示式为 .
(4)第三电子层上有 个能级,作为内层最多可容纳 个电子,作为最外层时,最多可含有 个未成对电子.
Ⅱ.写出下列元素基态原子的电子排布式:
(1)Ca (2)Kr
(3)Co (4)Ge
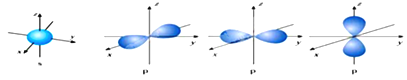
CuSO4和Cu(NO3)2是自然界中重要的铜盐。回答下列问题:
-
(1) Cu2+基态核外电子排布式为,S、O、N三种元素的第一电离能由大到小为。
-
(2) SO42-的立体构型是,与SO42-互为等电子体的一种分子为(填化学式)。
-
(3) 往Cu(NO3)2溶液中通入足量NH3能生成配合物[Cu(NH3)4](NO3)2。其中NO3-中心原子的杂化轨道类型为。
-
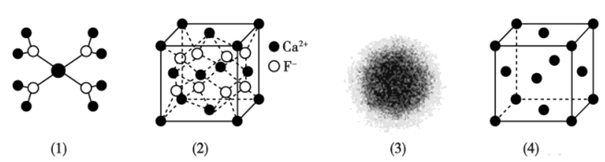
(4) 利用CuSO4和NaOH制备的Cu(OH)2检验醛基时,生成红色的Cu2O,其晶胞结构如图所示,其中O2-的配位数是。
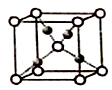
-
(5) B.[实验化学]
实验室以苯甲醛为原料制备间溴苯甲醛 (实验装置见图,相关物质的沸点见附表)。其实验步骤为:
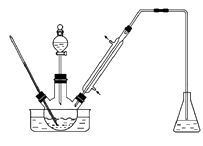
步骤1:将三颈瓶中的一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛充分混合后,升温至60℃,缓慢滴加经浓硫酸干燥过的液溴,保温反应一段时间,冷却。
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机相用10%NaHCO3溶液洗涤。
步骤3:经洗涤的有机相加入适量无水MgSO4固体,放置一段时间后过滤。
步骤4:减压蒸馏有机相,收集相应馏分。
实验装置中冷凝管的主要作用是,锥形瓶中的溶液应为。
-
(6) 步骤1所加入的物质中,有一种物质是催化剂,其化学式为。
-
(7) 步骤2中用10%NaHCO3溶液洗涤有机相,是为了除去溶于有机相的(填化学式)。
-
(8) 步骤3中加入无水MgSO4固体的作用是。
-
(9) 步骤4中采用减压蒸馏技术,是为了防止。
附表 相关物质的沸点(101kPa)
物质
沸点/℃
物质
沸点/℃
溴
58.8
1,2-二氯乙烷
83.5
苯甲醛
179
间溴苯甲醛
229
-
(1) a的M层比N层多个电子;b的L层比M层少个电子。a的稳定性(填“大于”或“小于”)b的稳定性。
-
(2) 写出A原子的电子排布式:;a的最外层的电子排布图是。
-
(1) 现代化学中,常利用上的特征谱线来鉴定元素。Ga的外围电子排布式为:,基态Ga原子核外有种运动状态不同的电子。
-
(2) 锗、砷、硒、溴的第一电离能由大到小的顺序为(用元素符号表示);其中锗的化合物四氯化锗可用作光导纤维掺杂剂,其熔点为-49.5℃,沸点为83.1℃,则其晶体类型为,中心原子的杂化类型为;砷酸的酸性弱于硒酸,从分子结构的角度解释原因。
-
(3) 铁能形成[Fe(Bipy)2Cl2]ClO4等多种配合物(Bipy结构如下图A)。
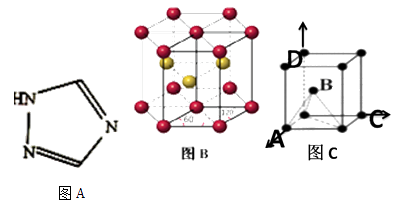
①该配合物中中心原子的化合价为;与中心原子形成配位键的原子是。
②与ClO4-互为等电子体的一种非极性分子是(举1例)。
③1 mol Bipy中所含σ键mol。
-
(4) 钛(Ti)被誉为“21世纪金属”,Ti晶体的堆积方式是六方最密堆积如图B所示,晶胞可用图C表示。设金属Ti的原子半径为a cm,空间利用率为。设晶胞中A点原子的坐标为(1,0,0),C点原子的坐标为(0,1,0),D点原子的坐标为(0,0,1),则B点原子的坐标为。
-
(1) 铁离子(Fe3+)最外层电子排布式为,其核外共有种不同运动状态的电子。
-
(2) 硒、砷、溴三种元素的第一电离能从大到小的顺序为(用元素符号表示)。
-
(3) 两种三角锥形气态氢化物PH3和NH3的键角分别为93.6°和107°,试分析PH3的键角小于NH3的原因。
-
(4) 常温下PCl5是白色晶体,在148℃时熔化成能导电的熔体。该熔体由A、B两种微粒构成,A、B分别与CCl4、SF6互为等电子体,则A的化学式为,其中心原子杂化方式为。
-
(5) Cu与Au的某种合金可形成面心立方最密堆积的晶体(密度为ρg·cm-3),在该晶胞中Cu原子处于面心,用NA表示阿伏加德罗常数的值。

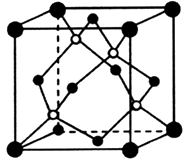
①与Au距离最近的Cu个数为。
②该晶体具有储氢功能,氢原子可进入到Cu原子与Au原子构成的立方体空隙中,储氢后的晶胞结构与金刚石晶胞结构(如图)相似,该晶体储氢后的化学式为,则晶胞中Cu原子与Au原子中心的最短距离d=cm。若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为(
 )。
)。
 D . 3d3表示3d能级有3个轨道
D . 3d3表示3d能级有3个轨道
-
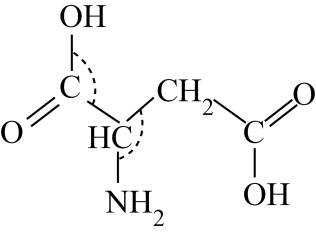
(1) 天门冬氨酸中C、N、O三种元素的第一电离能由大到小的顺序是,电负性最大的元素的价层电子轨道表示式。铬元素位于周期表第周期族,其基态原子的电子排布式为。
-
(2) 天门冬氨酸中的共价键类型为(填“σ键”、“π键”),其中N原子的杂化轨道类型为,图中O-C-C的键角-C-C-N的键角(填“大于”或“小于”)。
-
(3) H2S和H2Se热稳定性较好的是,从分子结构角度解释其原因:。
-
(4) 分子结构修饰在药物设计与合成中有广泛的应用。若将天门冬氨酸中的—NH2 , 换成—NO2 , 得到的新物质的酸性会增强,原因是。
-
(5) 四个主族元素部分简单氢化物沸点随周期序数的变化如图所示。其中表示第VIA族元素简单氢化物沸点变化的是曲线(填字母),用分子间作用力解释该曲线:。O—H…O的键能小于F—H…F,但水的沸点高于HF的原因可能是。

某些氢键的键能和键长
氢键X—H…Y
键能/(kJ·mol-1)
键长/pm
代表性例子
F—H…F
28.1
255
(HF)n
O—H…O
18.8
276
冰
O—H…O
25.9
266
甲醇,乙醇
N—H…F
20.9
268
NH4F
N—H…O
20.9
286
CH3CONH2
N—H…N
5.4
338
NH3
元素编号 | 元素性质与原子(或分子)结构 |
T | 最外层电子数是次外层电子数的3倍 |
X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
Y | M层比K层少1个电子 |
Z | 第三周期元素的简单离子中半径最小 |
-
(1) 写出元素T原子的电子排布式:。
-
(2) 元素Y与元素Z相比,金属性较强的是(用元素符号表示)。下列表述中能证明这一事实的是 (填序号)。
a.Y单质的熔点比Z单质低
b.Y的化合价比Z低
c. Y单质与水反应比Z单质与水反应剧烈
d. Y最高价氧化物对应的水化物的碱性比Z的强
-
(3) 写出T与Y形成的化合物的化学式:,。
-
(4) 元素T和氢元素以原子个数比1: 1化合形成化合物Q,元素X与氢元素以原子个数比1:2化合形成常用作火箭燃料的化合物W,Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式:。
-
(5) 固体A的化学式为XH5 , 它的所有原子的最外层都符合相应的稀有气体原子电子层结构,该物质适当加热就分解成两种气体,试完成:
①固体A属于晶体,它的电子式为。
②A溶于水后溶液呈 (填“酸”、“碱”或“中”)性,其原因是 (用化学方程式表示)。
- 中国发射“天宫一号”运载火箭使用的燃料是偏二甲肼,同时用四氧化二氮为氧化剂,两种物质反应的化学方程式为2N2O4+R==
- I ________ mycellphone last night. Now the battery is runnin
- 阅读下面的文言文,完成下列小题。 王求礼,许州长社人。武后时,为左拾遗、监察御史。后方营明堂,雕饰谲怪,侈而不法。求礼以
- Don't worry. There is _____ wrong with the TV set. It'sonly
- 含角的直角三角板()绕直角顶点沿逆时针方向旋转角(),再沿的对边翻折得到,与交于点,与交于点,与相交于点. (1)求证:
- 在政府的强有力的干预下,抢购食盐的风波很快平息了,但同学们发现,在这场风波中,有些市民盲目抢购,整箱地买,有人甚至买下全
- 阅读下面文段,完成后面作文。 又是一年芳草绿,依然花重锦官城。当春日的惠风吹拂面庞,那些发生在春天里的如烟往事,会在我们
- 下列各项中加点的成语,使用不正确的一项是( ) A.志愿不过是记忆的奴隶,总是有始无终,虎头蛇尾,像未熟的果
- They_________ play football last Friday because Simon forgot
- 下列化学用语既能表示一种元素,又能表示一个原子,还能表示一种物质的是A.H2 B.Al C.O
- 据《张居正集》(第三册卷三十七)载:“古之为国者,使商通有无,农力本穑。商不得通有无以利农,则农病;农不得力本穑以资商,
- (08北京密云)如图所示,物体A的长度是mm。
- 德国诗人莱辛说:“追求真理比占有真理更宝贵。”这句话强调的是 A.认识具有反复性 B.认识
- 根据提示填空。(每空1分,共6分) ⑴ ,问苍茫大地,谁主沉浮?(《沁园春·长沙》) ⑵真的猛士,敢于直面惨淡的人生
- 下列概念中,后者不包含前者的是 A.非金属、单质 B.物质
- 在空间图形中取互相________的x轴和y轴,两轴交于O点,再取z轴,使∠xOz=________,且∠yOz=___
- “别样”是与众不同的意思。总有一些人,带给我们别样的感受;总有一些事,带给我们别样的感触;总有一些景,带给我们别样的情思
- 假定地球上某个纬度之间存在这样一个广阔的区域,该地最热月气温是2月份,最冷月气温为8月,在8月份时测得该地的等温线如图所
- 下列做法不存在安全隐患的是 A.氢气还原氧化铜实验中,先加热氧化铜后通氢气 B.实验室做钠的实验时,余下
- “他们从旁观察世局,认真思索宇宙的真象,使用着抽象度高且不带意识形态的执着的 语言,描述天道与人事变化的法则,属于原理



