原子核外电子的运动状态 知识点题库
-
(1) 基态Ti原子中,最高能层电子的电子云轮廓形状为,与Ti同周期的所有过渡元素的基态原子中,最外层电子数与钛不同的元素有种。
-
(2) 琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+ , 从结构角度来看,Fe2+ 易被氧化成Fe3+的原因是。
-
(3) SCN-离子可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S)。
①写出与SCN-互为等电子体的一种微粒(分子或离子);
②硫氰酸分子中π键和σ键的个数之比为;
③异硫氰酸的沸点比硫氰酸沸点高的原因是。
-
(4) 成语“信口雌黄”中的雌黄分子式为As2S3 , 分子结构如图,As原子的杂化方式为,雌黄和SnCl2在盐酸中反应转化为雌黄(As4S4)和SnCl4并放出H2S气体,写出该反应方程式。SnCl4分子的空间构型为。
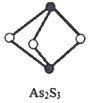
-
(5) 高子化合物CaC2的一种晶体结构如图所示。该物质的电子式。一个晶胞含有的π键平均有个。
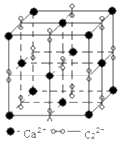
-
(6) 硒化锌的晶胞结构如图所示,图中X和Y点所堆积的原子均为(填元素符号);该晶胞中硒原子所处空隙类型为(填“立方体”、“正四面体”或正八面体”),该种空隙的填充率为;若该晶胞密度为pg•cm-3 , 硒化锌的摩尔质量为Mg•mol-1。用NA代表阿伏加德罗常数的数值,则晶胞参数a 为nm。
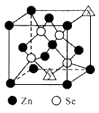
-
(1) 人工合成的蓝宝石晶体(Al2O3)是目前半导体工业中应用最广泛的材料。
①基态Al原子中有种运动状态不同的电子,核外电子占据最高能级的符号是,占据该能级电子的电子云轮廓图形状为。
②比较第一电高能:MgAl(填“>”、”<”或“=”)。在现代化学中,常利用上的特征谱线来鉴定元素,称为光谱分析。
-
(2) 羰基硫(COS)存在于许多种植物中,杀虫效果显著。
①1molCOS分子中含有σ键的数目为,其中心原子的杂化方式为。
②CS2、CO2、COS的分解温度由低到高的顺序为。
-
(3) NaCl 和MgO都属于离子化合物.NaCl的熔点为801.3℃,MgO的熔点高达2800℃。造成两种晶体熔点差距的主要原因是。
-
(4) 铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。
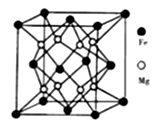
则:①距离一个Fe原子最近的Mg原子个数是,与此晶胞结构相似的常见的离子晶体是(填名称)。
②若该晶体储氢时,H2 分子在晶胞的体心和棱心位置,晶胞的参数为dnm,則距离最近的两个H2分子之间的距离为cm;含铁56g的该储氢合金可储存标准状况下H2 的体积为L。
-
(1) 基态氮原子最高能级上电子的自旋方向有种,硒原子的电子排布式为[Ar]。
-
(2) 铁的一种配合物Fe(CO)5熔点为-20.5℃,沸点为103℃,易溶于CCl4 , 据此可以判断Fe(CO)5晶体属于(填晶体类型)。
-
(3) 与BF3互为等电子体的分子和离子分别为(各举1例);已知分子中的大π键可用符号Ⅱnm表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Ⅱ66),则BF3中的大π键应表示为。
-
(4) 金属晶体的四种堆积如下图,金属钠的晶体堆积模型为(填字母)。
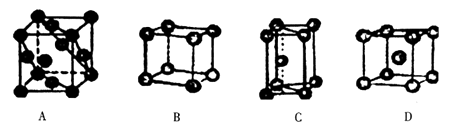
-
(5) 砷化硼(BAs)晶体结构与金刚石相似,则:
①BAs晶体中,As的杂化形式为.
②已知B原子的电负性比As原子的电负性大,则As与B之间存在的化学键有(填字母)。
A.离子键
B.金属键
C.极性键
D.氢键 E.配位键 F.σ键 G.π键
③BAs晶体的晶胞参数为bpm,则其晶体的密度为(列出表达式,设NA为阿伏加德罗常数的数值)g/cm3。
-
(1) 铜或铜盐的焰色反应为绿色,该光谱是(填“吸收光谱”或“发射光谱”)。
-
(2) 基态Cu原子中,核外电子占据的最低能层符号是,其价电子层的电子排布式为,Cu与Ag均属于IB族,熔点:CuAg (填“>”或“<”)。
-
(3) [Cu(NH3)4]SO4 中阴离子的立体构型是;中心原子的轨道杂化类型为,[Cu(NH3)4]SO4 中Cu2+与NH3之间形成的化学键称为。
-
(4) 用Cu作催化剂可以氧化乙醇生成乙醛,乙醛再被氧化成乙酸,等物质的量的乙醛与乙酸中σ键的数目比为。
-
(5) 氯、铜两种元素的电负性如表: CuCl属于(填“共价”或“离子”)化合物。
元素
Cl
Cu
电负性
3.2
1.9
-
(6) Cu 与Cl 形成某种化合物的晶胞如图所示,该晶体的密度为ρ g·cm-3 , 晶胞边长为a cm,则阿伏加德罗常数为(用含ρ、a的代数式表示)。
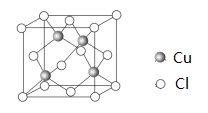
-
(1) 人体的构成元素,从周期表来看,元素数目最多族为 族。属于第三周期的非金属元素的原子半径由大到小的顺序。人体还有许多微量元素,请列举其中的一种。
-
(2) 含量最高的元素原子核外运动状态有种,最外层电子轨道表示式;与它同族的另一种元素的活动性相比>。(用元素符号表示),请用一个事实说明该结论。
-
(3) 含量前3位的元素按原子个数比1:1:2形成的物质的名称是(写出一种即可)。
 B . 氯离子的结构示意图:
B . 氯离子的结构示意图:  为碳原子的一种激发态
D . 聚丙烯的结构简式:
为碳原子的一种激发态
D . 聚丙烯的结构简式: 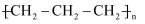

-
(1) LiCoO2、LiFePO4常用作锂离子电池的正极材料。基态Co原子核外电子排布式为,基态磷原子中,电子占据的最高能层符号为,该能层能量最高的电子云在空间有个伸展方向,原子轨道呈形。
-
(2) [CO(NO
 )4]2-中Co2+的配位数为4,配体中N原子的杂化方式为,该配离子中各元素的第一电离能由小到大的顺序为(填元素符号),1mol该配离子中含σ键数目为NA。
)4]2-中Co2+的配位数为4,配体中N原子的杂化方式为,该配离子中各元素的第一电离能由小到大的顺序为(填元素符号),1mol该配离子中含σ键数目为NA。
-
(3) MnCl2可与NH3反应生成[Mn(NH3)6]Cl2 , 新生成的化学键为键。NH3分子的空间构型为,其中N原子的杂化轨道类型为。
-
(4) 钴蓝晶体结构如图,该立方晶胞由4个I型和4个II型小立方体构成,共化学式为,晶体中Al3+占据O2-形成的(填“四面体空隙”或“八面体空隙”)。NA为阿伏加德罗常数得值,钴蓝晶体的密度为g•cm-3(列计算式)。
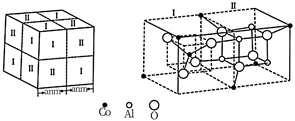
 B . 铍原子最外层的电子云图为
B . 铍原子最外层的电子云图为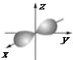 C . 基态Fe原子的价电子轨道表示式为
C . 基态Fe原子的价电子轨道表示式为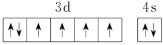 D .
D . 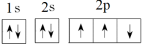 ,该轨道表示式违背了泡利不相容原理
,该轨道表示式违背了泡利不相容原理
-
(1) 基态Si原子中,核外电子占据的最高能层的符号为,占据最高能级的电子的电子云轮廓图形状为;基态Ga原子的核外电子排布为[Ar]3d104s2p1 , 其转化为下列激发态时,吸收能量最少的是(填选项字母)。
A.[Ar]
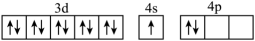 B.[Ar]
B.[Ar]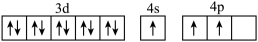
C.[Ar]
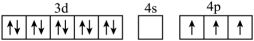 D.[Ar]
D.[Ar]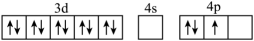
-
(2) C与Si是同主族元素,C原子之间可以形成双键、叁键,但Si原子之间难以形成双键、叁键。从原子结构分析,其原因为。
-
(3) 硼(B)与Ga是同主族元素,硼氢化钠(NaBH4)是有机合成中重要的还原剂,其阴离子BH
 的立体构型为;另一种含硼阴离子的结构如图所示,其中B原子的杂化方式为。
的立体构型为;另一种含硼阴离子的结构如图所示,其中B原子的杂化方式为。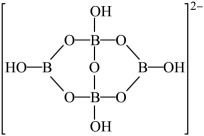
-
(4) GaCl3的熔点为77.9℃,GaF3的熔点为1000℃,试分析GaCl3熔点低于GaF3的原因为;气态GaCl3常以二聚体形式存在,二聚体中各原子均满足8e-结构,据此写出二聚体的结构式为。
-
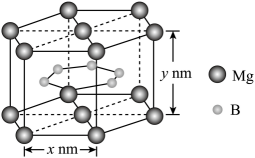
(5) B和Mg形成的化合物刷新了金属化合物超导温度的最高记录。该化合物的晶体结构单元如图所示,其中Mg原子间形成正六棱柱,6个B原子分别位于六个三棱柱体心。则该化合物的化学式可表示为;相邻B原子与Mg原子间的最短距离为nm(用含x、y的代数式表示)。
-
(1) 基态铁原子最外层电子所在能级的电子云轮廓图为形。
-
(2) H、C、O三种元素的电负性由大到小的排序为(填元素符号)。
-
(3) 锰和铁处于同一周期,锰、铁电离能数据如表所示:
元素
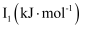
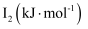
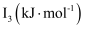
Mn
717.3
1509.9
3248
Fe
762.5
1561.9
2953
请解释
 的主要原因:。
的主要原因:。 -
(4) H、C、O三种元素可以组成很多种物质。
①
 、
、 、
、 、
、 、
、 中属于非极性分子的有(填化学式)。
中属于非极性分子的有(填化学式)。②
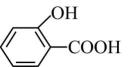 的沸点(填“大于”、“小于”或“等于”)
的沸点(填“大于”、“小于”或“等于”)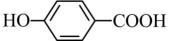 的沸点。
的沸点。 -
(5) 用X射线衍射仪测定发现铁晶体有两种晶胞结构,如图1、图2所示。
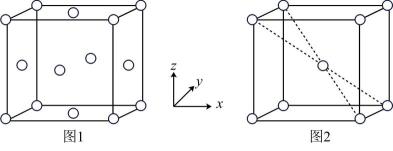
①原子坐标参数可以描述晶胞内部各微粒的相对位置。设图1中1号原子的坐标参数为(0,0,0),3号原子的坐标参数为(1,1,1),则2号原子的坐标参数为。
②若图2中晶胞参数为apm,则该晶胞的空间利用率(
 )为(用含π的式子表示)%。
)为(用含π的式子表示)%。
- 如图,在河岸上用细绳拉船,为了使船匀速靠岸,拉绳的速度必须是( )A.加速拉 B.减速拉 C. 匀速
- 已知,圆C:,直线:. (1) 当a为何值时,直线与圆C相切; (2) 当直线与圆C相交于A,B两点,且时,求直线的方程
- 下列有关生物体内基因与酶关系的叙述,正确的是 A.绝大多数酶是基因转录的重要产物 B.酶和基因都是细胞内染色体的组成成分
- 有赤道穿过的一组大洲是 A.非洲、北美洲
- . “He will come tomorrow.” “But I’d rather he _____ the day
- 《中华人民共和国侵权责任法》将于2010年7月1日起施行,该法规定因同一侵权行为造成多人死亡的,可以以相同数额确定死亡赔
- After talking with him for a few minutes I ______theconclusi
- 根据下列自养生物合成有机物的反应式,推测三类生物在进化中出现的先后顺序,以及参与碳的生物地球化学循环的生物种类 : 光
- 科学上把具有相同质子数,不同中子数的同一元素的不同原子称为同位素。日本福岛核电站爆炸后在我国境内检测到微量的放射性碘-1
- 马克思、恩格斯说:“由于阶级对立的发展是同工业的发展步调一致的,所以这些发明家不可能看到无产阶级解放的物质条件,于是他们
- 在17、18世纪的殖民扩张中,北美和印度成为英法争夺的主要地区,其主要原因是该地区 A. 是潜在的商品市场和原料产地
- 用不等号连接下列各对数:.
- 被尊崇为兵学圣典的是( )A.《吴子》 B.《孙子兵法》 C.《孙膑兵法》 D.《韩非
- 如图,在平面直角坐标系中,矩形ABCO的面积为15,边OA比OC大2.E为BC的中点,以OE为直径的⊙O′交x轴于D点,
- 水是生命之源、生产之要、生态之基。黄河、长江哺育了中华民族,从古至今,气壮山河的水利建设,取得了举世瞩目的成就。治水使中
- 1 mol甲烷与2 mol氯气混合,光照条件下充分反应,所得产物的物质的量最多的是( ) A.CH3Cl
- 已知a>0,b>0,则++2 的最小值是() A.2 B.2C.4 D.5
- 一个质点做简谐振动,它的振动图像如图4-1所示,下列判断正确的是( )A.图中的曲线部分是质点的运动轨迹 B.有向
- 下列结构中,原核细胞没有的是( ) A. 细胞膜 B.核被膜
- 图1所示的匀强电场E的区域内,由A、B、C、D、A′、B′、C′、D′作为顶点构成一正方体空间,电场方向与面ABCD垂直



