电解质溶液 知识点题库
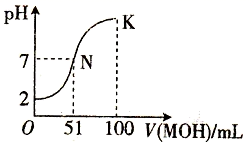
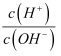 的关系如右图所示。下列说法错误的是( )
的关系如右图所示。下列说法错误的是( )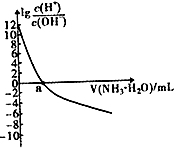
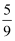 ×10-9
D . 当滴入氨水的体积V=20mL时,溶液中存在c(NH4+)>c(A-)
×10-9
D . 当滴入氨水的体积V=20mL时,溶液中存在c(NH4+)>c(A-)
![]()
【资料】:+5价钒在溶液中的主要存在形式与溶液pH的关系:
pH | 4~6 | 6~8 | 8~10 | 10~12 |
主要离子 | VO2+ | VO3− | V2O74− | VO43− |
-
(1) 焙烧:向石煤中加生石灰焙烧,将V2O3转化为Ca(VO3)2的化学方程式是。
-
(2) 酸浸: ① Ca(VO3)2难溶于水,可溶于盐酸。若焙砂酸浸时溶液的pH=4,Ca(VO3)2溶于盐酸的离子方程式是。
② 酸度对钒和铝的溶解量的影响如图所示:酸浸时溶液的酸度控制在大约3.2%,根据如图推测,酸浸时不选择更高酸度的原因是。
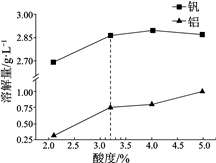
-
(3) 转沉:将浸出液中的钒转化为NH4VO3固体,其流程如下:

① 浸出液中加入石灰乳的作用是。
② 已知CaCO3的溶解度小于Ca3(VO4)2。向Ca3(VO4)2沉淀中加入(NH4)2CO3溶液,可使钒从沉淀中溶出。结合化学用语,用平衡移动原理解释其原因:。
③ 向(NH4)3VO4溶液中加入NH4Cl溶液,控制溶液的pH=7.5。当pH>8时,NH4VO3的产量明显降低,原因是。
-
(4) 测定产品中V2O5的纯度:
称取a g产品,先用硫酸溶解,得到(VO2)2SO4溶液。再加入b1 mL c1 mol·L−1 (NH4)2Fe(SO4)2溶液(VO2+ + 2H+ + Fe2+ = VO2+ + Fe3+ + H2O)。最后用c2 mol·L−1 KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液的体积为b2 mL。已知 MnO4−被还原为Mn2+ , 假设杂质不参与反应。则产品中V2O5的质量分数是。(V2O5的摩尔质量:182 g·mol−1)
回答下列问题:
-
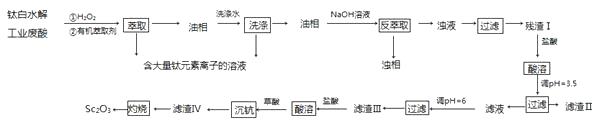
(1) 在钛白水解工业废酸中,加入双氧水是为了使TiO2+转化为难萃取的[Ti(O2)(OH(H2O)4]+。[Ti(O2)(OH(H2O)4]+中Ti 的化合价为+4,其中非极性键的数目为。
-
(2) 钪的萃取率(E%)与O/A 值[萃取剂体积(O)和废酸液体积(A)之比]的关系如左下图,应选择的最佳O/A值为;温度对钪、钛的萃取率影响情况见右下表,合适的萃取温度为10-15℃,其理由是。

-
(3) 洗涤“油相“可除去大量的钛离子。洗染水是用浓硫酸、双氧水和水按一定比例混合而成。混合过程的实验操作为。
-
(4) 25℃时,用氨水调节滤液的pH,当pH=3.5时,滤渣II的主要成分是;当pH=6时,滤液中Sc3+的浓度为。(Ksp[Fe(OH)3]=2.6×10-39 , Ksp[Sc(OH)3]=9.0×10-31)
-
(5) 写出用草酸(H2C2O4)“沉钪”得到Sc2(C2O4)3的离子方程式。
-
(6) 若从1m3该工厂的钛白水解度酸中提取得到24.4gSc2O3 , 则钪的提取率为(保留三位有效数字)。
下列有关推断合理的是( )
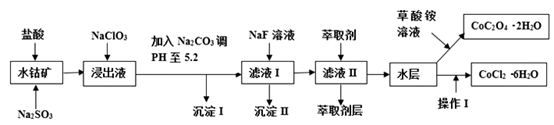
已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+、Mg2+、Ca2+等;②沉淀I中只含有两种沉淀;③流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
|
沉淀物 |
Fe(OH)3 |
Fe(OH)2 |
Co(OH)2 |
Al(OH)3 |
Mn(OH)2 |
|
开始沉淀 |
2.7 |
7.6 |
7.6 |
4.0 |
7.7 |
|
完全沉淀 |
3.7 |
9.6 |
9.2 |
5.2 |
9.8 |
-
(1) 浸出过程中Co2O3发生反应的离子反应方程式为。
-
(2) NaClO3在浸出液中发生的离子反应方程式为。
-
(3) 加入Na2CO3调pH至5.2,目的是;萃取剂层含锰元素,则沉淀II的主要成分为。
-
(4) 操作I包括:将水层加入浓盐酸调整pH为2-3,、、过滤、洗涤、减压烘干等过程。
-
(5) 为测定粗产品中CoCl2·6H2O含量,称取一定质量的粗产品溶于水,加入足量硝酸酸化的硝酸银溶液,过滤、洗涤、干燥,测沉淀质量。通过计算发现粗产品中CoCl2·6H2O质量分数大于100%,其原因可能是(回答一条原因即可)。
 )+c(CO
)+c(CO  )+c(OH-)
C . 0.1 mol·L-1Na2S溶液中:2c(Na+)=c(S2-)+c(HS-)+c(H2S)
D . Na2 CO3溶液中:c(OH-)=c(H+)+c(HCO
)+c(OH-)
C . 0.1 mol·L-1Na2S溶液中:2c(Na+)=c(S2-)+c(HS-)+c(H2S)
D . Na2 CO3溶液中:c(OH-)=c(H+)+c(HCO  )+2c(H2CO3)
)+2c(H2CO3)
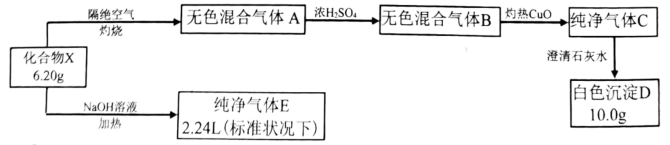
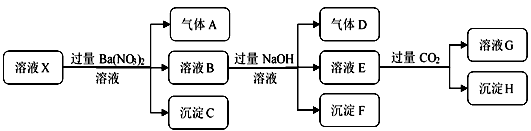
已知:①纯净气体E能使湿润的红色石蕊试纸变蓝色;②流程中所用转化试剂均过量。
请回答下列问题:
-
(1) 化合物X中所含的元素有H、O和, X的化学式为。
-
(2) 写出化台物X隔绝空气灼烧生成混合气体A的化学方程式。
-
(3) 在实验室,X常用作沉淀剂。写出化合物X与CaCl2溶波反应的离子方程式。
-
(4) 气体E也能与灼热CuO发生氧化还原反应,只生成一种固体产物。 请推测固体产物的组成(假设CuO完全反应),并设计实验方案验证之。
-
(5) 某同学认为可以用点燃的方法将混合气体B转变为纯净气体C,你认为是否可行,并说明理由。
 C . CO
C . CO  的空间构型:平面三角形
D . CO
的空间构型:平面三角形
D . CO  的水解方程式:CO
的水解方程式:CO  +2H2O
+2H2O  H2CO3+2OH−
H2CO3+2OH−
 )的大小顺序为①>②>③
C . 在NH4Cl溶液中加入稀HNO3 , 能抑制
)的大小顺序为①>②>③
C . 在NH4Cl溶液中加入稀HNO3 , 能抑制  水解
D . 将硫酸亚铁溶液加热蒸干得不到原溶质
水解
D . 将硫酸亚铁溶液加热蒸干得不到原溶质
-
(1) 写出醋酸的电离方程式
-
(2) 达平衡时,溶液中氢离子浓度约是(25℃时,醋酸电离平衡常数为2. 25×10 -6)
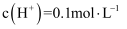 溶液中:
溶液中: 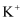 、
、  、
、  、
、  B . 某无色透明溶液中:
B . 某无色透明溶液中:  、
、  、
、  、
、 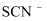 C . 能使酚酞变红的溶液中:
C . 能使酚酞变红的溶液中:  、
、  、
、 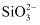 、
、  D .
D . 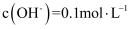 溶液中:
溶液中:  、
、 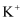 、
、  、
、 

 H++SO
H++SO  (K2=1.0×10-2)。设NA为阿伏加德罗常数的值,下列说法正确的是( )
(K2=1.0×10-2)。设NA为阿伏加德罗常数的值,下列说法正确的是( )
 )+c(OH-)+2c(SO
)+c(OH-)+2c(SO  )=c(H+)
)=c(H+)
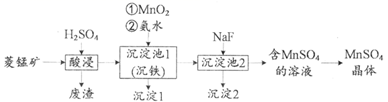
已知:常温下,Ksp(MnS)=1×10-11.金属离子生成氢氧化物沉淀的pH如下表:
| 金属离子 | Fe3+ | Fe2+ | Mn2+ | Mg2+ |
| 开始沉淀 | 1.5 | 6.3 | 7.6 | 9.6 |
| 完全沉淀 | 2.8 | 8.3 | 10.2 | 11.6. |
-
(1) 酸浸时选择H2SO4而不是HCl的原因可能是和,沉淀池1中,加入MnO2时发生反应的离子方程式为。
-
(2) 该工艺流程中废渣和沉淀1、2均需用水洗涤,并将洗涤液返回酸浸工序,目的是。
-
(3) 沉淀2的化学式是,不能用NaOH代替NaF,其原因是。
-
(4) 含MnSO4溶液中还含有杂质(填离子符号),利用KMnO4溶液与Mn2+反应生成黑色沉淀的现象可以检验Mn2+ , 发生反应的离子方程式为。
-
(5) 电解MnSO4溶液可进一步获得二氧化锰,电解后的废水中还含有Mn2+ , 常用石灰乳进行一级沉降得到Mn(OH)2沉淀,过滤后再向滤液中加入适量Na2S,进行二级沉降。欲使溶液中c(Mn2+)≤1.0×10-5 mol·L-1 , 则应保持溶液中c(S2-)≥mol·L-1。
 沉淀溶解平衡曲线如图,下列结论正确的是( )
沉淀溶解平衡曲线如图,下列结论正确的是( ) 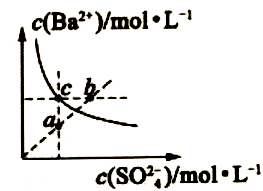
 沉淀生成
B . 蒸发可使溶液由a点到c点
C . 曲线上任意点的Ksp相同
D . 向a点加入
沉淀生成
B . 蒸发可使溶液由a点到c点
C . 曲线上任意点的Ksp相同
D . 向a点加入  固体,溶液可达b点
固体,溶液可达b点
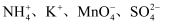 B . 使甲基橙变红的溶液中:
B . 使甲基橙变红的溶液中: 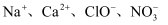 C . 中性溶液中:
C . 中性溶液中: 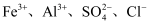 D .
D . 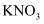 溶液中:
溶液中: 
-
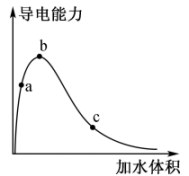
(1) a、b、c三点溶液的pH从大到小顺序为。
-
(2) a、b、c三点溶液用
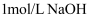 溶液中和,消耗
溶液中和,消耗 溶液的体积大小关系为。
溶液的体积大小关系为。
-
(3) 用蒸馏水稀释c点的醋酸,则下列各式表示的数值随水量的增加而增大的是____(填字母)。A .
 B . 电离度
B . 电离度 C .
C . 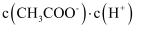 D .
D . 
-
(4) 已知
 的电离平衡常数
的电离平衡常数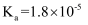 ,
,  中
中 约为
约为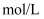 。
。
-
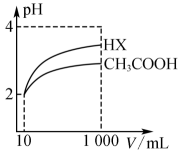
(5) 体积为
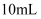 ,
, 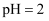 的醋酸溶液与
的醋酸溶液与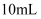 ,
, 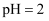 的一元酸
的一元酸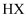 分别加水稀释至
分别加水稀释至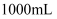 , 稀释过程
, 稀释过程 变化如图,若将相同表面积的
变化如图,若将相同表面积的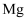 分别加入等浓度的醋酸和
分别加入等浓度的醋酸和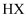 溶液中,初始反应速率为
溶液中,初始反应速率为 (填“<”“>”或“=”)
(填“<”“>”或“=”)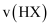 。
。
- —Do youhave to do chores at home, Mike? —Of course, I was m
- Who is it up decide to hold themeeting at the weekend
- 如图所示电路中,已知I=3A,I1=2A,R1=10Ω,R2=5Ω,R3=30Ω,则通过电流表的电流方向为向______
- 如图是电解水的实验装置,对该实验描述正确的是( ) A.正极产生的气体是氢气 B.
- 该城镇欲依托矿产资源,调整工业结构,发展循环经济,你认为最适宜在该城镇布局的工厂是( ) A、水泥厂
- 一个盒子里装有n-1个白球,1个红球,每次随机地取出一个球,若取到白球则放回再取,若取到红球则停止取球,则取球次数ξ的数
- 善于归纳知识,有利于培养我们的科学素质.下列知识整理的内容有错误的一组是A.化学与安全 B.化学与生活 油锅着火——用锅
- 发动安史之乱的两位叛军首领是 ( ) ①安禄山 ②李光弼 ③郭子仪 ④史思明
- A、B、C、D、E、F为原子序数依次增大的主族元素。已知A、C、F三原子的最外层共有12个电子,且这三种元素的最高价氧化
- “引吭高歌”和“低声细语”中的“高”与“低”指的是( ) A.音调高低 B.响度大小 C.
- 阅读理解 Once upon a time there lived two brothers named Jacob
- 5、下列句子,没有语病的一句是( ) A.采用各种办法培养现代企业人员的水平,尤其是青年同志的水平,是我国许多
- 在盛有少量无水乙醇的试管中,加入一小块新切的、擦干表面煤油的金属钠,迅速用配有导管的单孔塞塞住试管口,用一小试管收集并验
- 2010年我国继续实施积极的财政政策和适度宽松的货币政策,把握好政策实施的力度、节奏和重点。实施积极的财政政策应该()
- 读某城市居住区空间结构模式图,完成10~11题。 10.该城市 A.主城区为煤炭资源初加工从业者聚居区 B.不同聚
- 【2012高考江苏12】在平面直角坐标系中,圆的方程为,若直线上至少存在一点,使得以该点为圆心,1为半径的圆与圆有公共点
- 第二天,中午的时候,非常闷热。一轮红日当天,水面上浮着一层烟气。小火轮开得离苇塘远一些,鬼子们又偷偷地爬下来洗澡了。十几
- 如图为验证水的组成的实验装置,下列有关说法正确的是()
- (文)已知数列{}满足,且,且则数列{}的通项公式为 A. B. C. D.
- 一般来说,动物细胞体外培养需要满足以下条件 ( )①无毒的环境 ②无菌的环境 ③合成培养基需加血浆 ④温



