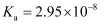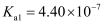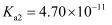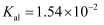电解质溶液 知识点题库
常温下,0.1mol·L-1某一元酸(HA)溶液中 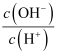 =1×10-8 , 下列叙述正确的是( )
=1×10-8 , 下列叙述正确的是( )
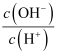 =1×10-8 , 下列叙述正确的是( )
=1×10-8 , 下列叙述正确的是( )
A . 溶液中水电离出的c(H+)=10-10mol·L-1
B . 溶液中c(H+)+c(A-)=0.1mol·L-1
C . 上述溶液加NaA晶体,溶液的c(OH-)增大
D . 常温下将HA稀释十倍,氢离子浓度变为原来的十分之一
下图所示的实验装置图正确且能达到相应实验目的的是()
图1 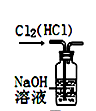 图2
图2  图3
图3 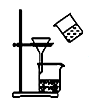 图4
图4 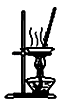
A . 用图1所示装置除去Cl2中的HCl
B . 用图2所示装置实验室制NH3
C . 用图3所示装置分离MnO2和KCl
D . 用图4所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
下列说法正确的是( )
A . 无论是纯水,还是酸性、碱性或中性稀溶液,其c(H+)·c(OH-)=1×10-14
B . c(H+)=1×10-7 mol·L-1的溶液一定是中性溶液
C . 常温下,Ksp[Mg(OH)2]=5.6×10−12 , pH=10的含Mg2+溶液中,c(Mg2+)≤5.6×10−4 mol·L−1
D . 加热蒸干AlCl3溶液然后灼烧得到Al(OH)3固体
pH=1的两种一元酸HZ和HY的溶液,分别取50 mL,加入足量的镁粉,充分反应后收集H2的体积分别为V(HZ)和V(HY),若V(HZ)>V(HY),下列说法正确的是( )
A . HY一定是强酸
B . HZ不一定为弱酸
C . HZ的酸性强于HY的酸性
D . 反应开始时二者生成H2的速率相同
下列说法正确的是 ( )
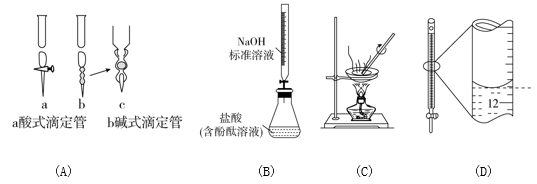
A . 碱式滴定管注入Na2CO3溶液之前应检查是否漏液
B . 测定盐酸浓度
C . 蒸干AlCl3饱和溶液制备AlCl3晶体
D . 记录滴定终点读数为12.20 ml
下列离子在对应的溶液中能大量共存的是( )
A . 在强酸性溶液中: CH3COO-、 NO3-、Fe2+、 Na+
B . 在能使酚酞试液变深红色的溶液中:Ca2+、 Ba2+、 NO3-、HCO3-
C . 在含有Cl-、 Ba2+的溶液中:Na+、K+、HCO3-、NO3-
D . 在无色透明溶液中:Ba2+、Fe3+、Mg2+、 Cl-、NO3-
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A . 0.1 mol/LNa2CO3溶液:K+、  、Cl-、
、Cl-、  B . 使甲基橙变红色的溶液:K+、Na+、
B . 使甲基橙变红色的溶液:K+、Na+、  、
、  C . 0.1 mol/L FeSO4溶液中:H+、Al3+、Cl-、
C . 0.1 mol/L FeSO4溶液中:H+、Al3+、Cl-、  D .
D .  =0.1 mol/L的溶液中:Na+、
=0.1 mol/L的溶液中:Na+、  、CH3COO-、
、CH3COO-、 
 、Cl-、
、Cl-、  B . 使甲基橙变红色的溶液:K+、Na+、
B . 使甲基橙变红色的溶液:K+、Na+、  、
、  C . 0.1 mol/L FeSO4溶液中:H+、Al3+、Cl-、
C . 0.1 mol/L FeSO4溶液中:H+、Al3+、Cl-、  D .
D .  =0.1 mol/L的溶液中:Na+、
=0.1 mol/L的溶液中:Na+、  、CH3COO-、
、CH3COO-、 
重金属离子有毒性。实验室有甲、乙两种废液,均有一定毒性。经化验可知甲废液呈碱性,主要有毒离子为  ,若将甲、乙两废液按一定比例混合,毒性明显降低。乙废液中可能含有的离子是( )
,若将甲、乙两废液按一定比例混合,毒性明显降低。乙废液中可能含有的离子是( )
 ,若将甲、乙两废液按一定比例混合,毒性明显降低。乙废液中可能含有的离子是( )
,若将甲、乙两废液按一定比例混合,毒性明显降低。乙废液中可能含有的离子是( )
A .  和
和  B .
B .  和
和  C .
C . 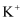 和
和  D .
D . 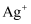 和
和 
 和
和  B .
B .  和
和  C .
C . 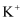 和
和  D .
D . 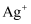 和
和 
下列物质属于电解质且在该状态下能导电的是( )
A . Cu
B . 熔融 NaCl
C . KOH 溶液
D . BaSO4 固体
在体积都为1 L、pH都等于2的盐酸和醋酸溶液中,投入0.69 g 锌粒,则如图所示比较符合客观事实的是( )
A . 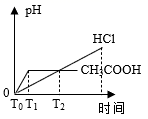 B .
B . 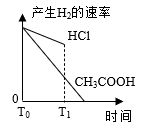 C .
C . 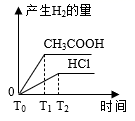 D .
D . 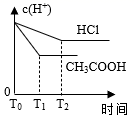
 B .
B .  C .
C .  D .
D . 
SO2 是中学化学中的常见气体,也是大气污染物的主要组成成分。回答下列问题:
-
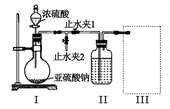
(1) 甲组同学利用下列装置制备并收集干燥的 SO2:
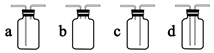
装置Ⅰ中盛装亚硫酸钠的仪器名称是,装置 II 的作用是对 SO2 气体进行干燥,该装置中所盛 试剂名称为,装置 III 为集气装置,应选取填入 III 中的集气装置为(选填字母代号)。
-
(2) 乙组同学利用下列装置制备 SO2 并探究其性质:
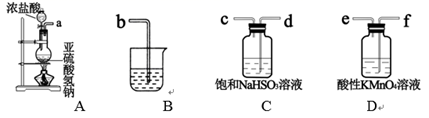
①该组同学的实验装置中,依次连接的合理顺序为a→。装置C中饱和NaHSO3溶液的作用是。
②能证明SO2具有还原性的现象是,该反应的离子方程式为。
③装置B的作用吸收SO2尾气,该装置中盛装的试剂是。
-
(3) 设计实验证明H2SO3为弱电解质:。
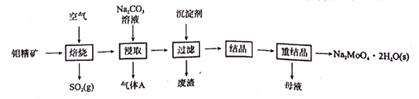
钼酸钠晶体(Na2MoO4·2H2O) 常用于配制金属缓蚀剂。图为利用钼精矿(主要成分是MoS2 , 含少量PbS等)为原料生产钼酸钠晶体的工艺流程图。回答下列问题:
-
(1) 为了提高焙烧效率,除增大空气量外还可以采用的措施是(写一条即可),写出焙烧时生成MoO3的化学方程式。
-
(2) “浸取"时产生的气体A是。
-
(3) 若“过滤”前加入的沉淀剂为Na2S,则废渣的成分为(填化学式)。
-
(4) “结晶”前需向滤液中加入Ba(OH)2 固体以除去CO32-。 若滤液中c(MoO42- )=0.40mol/L,c(CO32-)=0.20mol/L,要使钼元素无损失,CO32- 的最大去除率是[已知:Ksp(BaCO3)= 1.0×10-9 , Ksp(BaMoO4)=4.0×10-8]。
-
(5) 重结晶得到的母液可以在下次重结晶时亚复使用,但达到一定次数后必须净化处理,原因是。
-
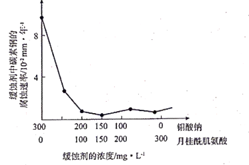
(6) 钼酸钠和月桂酰肌氨酸的混合液常作为碳素钢的缓蚀剂。常温下,碳素钢在缓蚀剂中的腐蚀速率实验结果如图所示。要使碳素钢的缓蚀效果最好,缓蚀剂中钼酸钠(摩尔质量为M)的物质的量浓度为mol/L。
体积相同、pH相同的HCl溶液和CH3COOH溶液,与NaOH溶液中和时,两者消耗NaOH的物质的量( )
A . 无法比较
B . 相同
C . 中和HCl的多
D . 中和CH3COOH的多
下列物质中,既属于有机物,又是非电解质的是( )
A . 乙酸
B . 二氧化碳
C . 乙醇钠
D . 葡萄糖
往 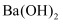 溶液中滴加(或通入)某物质X,溶液的导电能力如图所示,其中Ⅹ不可能是( )
溶液中滴加(或通入)某物质X,溶液的导电能力如图所示,其中Ⅹ不可能是( )
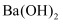 溶液中滴加(或通入)某物质X,溶液的导电能力如图所示,其中Ⅹ不可能是( )
溶液中滴加(或通入)某物质X,溶液的导电能力如图所示,其中Ⅹ不可能是( ) 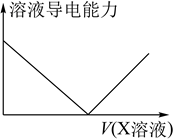
A .  B . 稀硫酸
C . 稀硝酸
D .
B . 稀硫酸
C . 稀硝酸
D . 
 B . 稀硫酸
C . 稀硝酸
D .
B . 稀硫酸
C . 稀硝酸
D . 
某固体可能含有  、
、  、
、  、
、  、
、  、
、  中的几种离子,取等质量的两份该固体,进行如下实验(不考虑盐类的水解及水的电离)
中的几种离子,取等质量的两份该固体,进行如下实验(不考虑盐类的水解及水的电离)
 、
、  、
、  、
、  、
、  、
、  中的几种离子,取等质量的两份该固体,进行如下实验(不考虑盐类的水解及水的电离)
中的几种离子,取等质量的两份该固体,进行如下实验(不考虑盐类的水解及水的电离) ⑴一份固体溶于水得无色透明溶液,加入足量  溶液,得沉淀4.30 g,在沉淀中加入过量稀盐酸,仍有2.33 g沉淀。
溶液,得沉淀4.30 g,在沉淀中加入过量稀盐酸,仍有2.33 g沉淀。
⑵另一份固体与过量NaOH固体混合后充分加热,产生 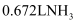 (标准状况)。
(标准状况)。
下列说法正确的是( )
A . 根据以上实验,无法确定该固体中有  B . 该固体中一定含有
B . 该固体中一定含有  、
、  、
、  、
、  C . 该固体中只含有
C . 该固体中只含有  、
、  、
、  、
、  D . 该固体中一定没有
D . 该固体中一定没有  、
、  、
、 
 B . 该固体中一定含有
B . 该固体中一定含有  、
、  、
、  、
、  C . 该固体中只含有
C . 该固体中只含有  、
、  、
、  、
、  D . 该固体中一定没有
D . 该固体中一定没有  、
、  、
、 
下列实验操作能达到实验目的且现象描述正确的是( )
| 选项 | 实验操作及现象 | 实验目的 |
| A | 向无色溶液中滴加FeCl3溶液和CCl4 , 振荡、静置,下层显紫红色 | 证明溶液中含有I- |
| B | 向某溶液中先加入少量氯水,然后加入KSCN溶液,溶液变为血红色 | 证明溶液中含有Fe2+ |
| C | 在盛有漂白粉的试管中滴入70%的硫酸,立刻产生黄绿色气体 | 证明硫酸具有还原性 |
| D | 将3 LSO2和1 LO2混合通过灼热的V2O5充分反应,产物先通入BaCl2溶液,有白色沉淀,再通入品红溶液,溶液褪色 | 验证SO2与O2的反应为可逆反应. |
A . A
B . B
C . C
D . D
已知部分弱酸的电离常数如表所示:
| 弱酸 | HClO | | |
| 电离常数 ( | | | |
下列离子方程式正确的是( )
A . 少量  通入NaClO溶液中:
通入NaClO溶液中: 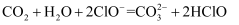 B . 少量
B . 少量  通入
通入 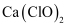 溶液中:
溶液中: 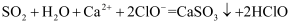 C . 少量
C . 少量  通入
通入  溶液中:
溶液中: 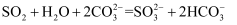 D . 相同浓度
D . 相同浓度  溶液与
溶液与  溶液等体积混合:
溶液等体积混合: 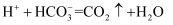
 通入NaClO溶液中:
通入NaClO溶液中: 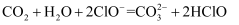 B . 少量
B . 少量  通入
通入 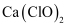 溶液中:
溶液中: 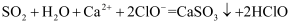 C . 少量
C . 少量  通入
通入  溶液中:
溶液中: 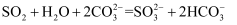 D . 相同浓度
D . 相同浓度  溶液与
溶液与  溶液等体积混合:
溶液等体积混合: 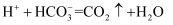
某油脂厂废弃的油脂加氢镍催化剂,主要含金属Ni、Fe、Al及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·7H2O):
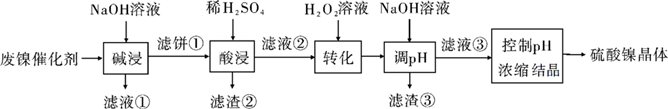
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀时(c=0.01 mol·L−1)的pH | 7.2 | 3.7 | 2.2 | 7.5 |
| 沉淀完全时(c=1.0×10−5 mol·L−1)的pH | 8.7 | 4.7 | 3.2 | 9.0 |
回答下列问题:
-
(1) “碱浸”中NaOH的两个作用分别是;写出NaOH与Al2O3反应的离子方程式。
-
(2) “滤液②”中含有的金属离子是。
-
(3) “转化”中可替代H2O2的物质是。若工艺流程改为先“调pH”后 “转化”,即
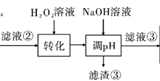 ,“滤液③”中可能含有的杂质离子为。
,“滤液③”中可能含有的杂质离子为。
-
(4) 利用上述表格数据,计算Ni(OH)2的Ksp=。如果“转化”后的溶液中Ni2+浓度为1.0 mol·L−1 , 则“调pH”应控制的pH范围是。
-
(5) 硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式。
有下列十种物质:①  粉末②铜③氯化氢④
粉末②铜③氯化氢④  ⑤
⑤  固体⑥
固体⑥ 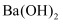 固体⑦红褐色的氢氧化铁胶体⑧氨水⑨稀硝酸⑩熔融的氢氧化钠。
固体⑦红褐色的氢氧化铁胶体⑧氨水⑨稀硝酸⑩熔融的氢氧化钠。
 粉末②铜③氯化氢④
粉末②铜③氯化氢④  ⑤
⑤  固体⑥
固体⑥ 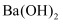 固体⑦红褐色的氢氧化铁胶体⑧氨水⑨稀硝酸⑩熔融的氢氧化钠。
固体⑦红褐色的氢氧化铁胶体⑧氨水⑨稀硝酸⑩熔融的氢氧化钠。
-
(1) 上述物质中,属于盐的是;可导电的是;属于电解质的是;属于混合物的是。(填序号)
-
(2) 写出⑤和⑨在水溶液中的电离方程式:、。
-
(3) 写出③和⑩在水溶液中反应的离子方程式:。
最近更新
- 直升机悬停在空中向地面投放装有救灾物资的箱子。设投放初速度为零,箱子所受的空气阻力大小与箱子下落速度的平方成正比,且运
- 当光束通过下列分散系:①尘埃的空气 ②稀硫酸 ③蒸馏水 ④墨水,能观察到有丁达尔现象的是 A.①② B.②③ C.①④
- 已知砒霜As2O3与Zn可以发生如下反应: As2O3+6Zn+6H2SO4===2AsH3↑+6ZnSO4+3H2O
- (4分)化学与我们的生活息息相关。现有:①氮气 ②生石灰 ③熟石灰 ④二氧化硫。回答下列问题(均填序号): (1)可
- 氢能源具有来源广、热值高、无污染等优点.氢气的热值为14.3×107J/kg,完全燃烧0.5 kg的氢气可放出_____
- 萧山素以“萝卜干之乡”著称.某乡组织20辆汽车装运A、B、C三种不同包装的萝卜干42吨到外地销售.按规定每辆车只装同一种
- 复数 ( ) A.
- 某物质X在氧气中燃烧生成二氧化碳和水.X一定含有的元素有.X属于(填“有机物”或“无机物”).什么情况可判断X中不含氧元
- We will goswimming if it ______ next week. A. rains
- 为了检验某化合物中是否含有、、Fe2+和结晶水,设计了下列操作步骤:①取少量该化合物加热,发现试管口处有液体,该液体能使
- 下列关于基因工程的叙述中,正确的是 A.目的基因的核苷酸序列都是已知的 B.接受外源基因的转基因植物成为一个新物种 C.
- 为了测量木板和斜面间的动摩擦因素,某同学设计如下实验. 在小木板上固定一个轻弹簧秤, 弹簧秤下面掉一个光滑的小球
- ____ a letter from her parents, Lily is now looking forward
- ______ the Town Hall, we saw a stone statue of about 10 mete
- 下表是三个城市的气候资料,据此回答下面试题。 1.城市①、②、③可能分别是() A.上海 莫斯科 孟买 B
- When difficult people express themselves orally, theygener
- 设为坐标原点,,若点满足,则取得最小值时,点的个数是 A. B.
- 阅读宋词《酹江月》,回答①一②题。神州沉陆,问谁是,一范一韩人物。北望长安应不见,抛却关西半壁。塞马晨嘶,胡茄夕引,赢得
- 1851年和1911年都辛亥年,在中国都发生了大规模的革命化运动,这两场革命运动的相似之处有
- 下列关于我国土地资源特点的叙述,正确的是()A.北方耕地以旱地为主,南方则以水田为主B.荒漠、石山等土地较多,后备耕地充
 )
)