电解质溶液 知识点题库
下列物质属于电解质的是( )
A . 铝制导线
B . 氨水
C . 稀硫酸
D . 硝酸钠
某温度时,AgCl(s)  Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是( )
Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是( )
 Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是( )
Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是( ) 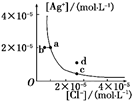
A . 加入AgNO3 , 可以使溶液由c点变到d点
B . c点对应的K等于a点对应的K
C . d点没有AgCl沉淀生成
D . 加入少量水,平衡右移,Cl-浓度减小
常温下,下列各组离子一定能在指定溶液中大量共存的是( )
A . pH=1的溶液中:Ba2+、Fe3+、Cl-、SCN-
B . 能使酚酞溶液变红的溶液中:Ca2+、K+、HCO3-、CO32-
C . c(OH-)/c(H+)=10-12的溶液中:NH4+、Cu2+、NO3-、SO42-
D . 水电离产生的c(OH-)=10-12 mol·L-1的溶液中:Na+、Al3+、Cl-、NO3-
下列叙述正确的是( )
A . 焓减或熵增的过程在任何条件下都能自发进行
B . 向饱和AgCl溶液中加入盐酸,Ksp变大
C . 将饱和FeCl3溶液滴入到沸水中可制备Fe(OH)3胶体
D . pH=5的CH3COOH溶液加水稀释1 000倍后pH=8
电解质在水溶液中存在各种行为,如电离、水解、沉淀溶解,据所学知识回答下列问题:
-
(1) t℃时,纯水中c(H+)=1×10-6 mol·L-1 , 该温度下,pH=10的Ba(OH)2溶液的物质的量浓度为 mol·L-1。
-
(2) 25℃时,将 a mol·L-1 的醋酸和 b mol·L-1 的氢氧化钠溶液等体积混合后,溶液的pH=7,则溶液中c(CH3COO-)+c(CH3COOH)= mol·L-1 , a b(填“﹥”、“﹤”或“=”)。
-
(3) 工业上采取用氨水除去SO2 , 已知25 ℃,NH3• H2O的Kb=1.8×10-5 , H2SO3的 Ka1=1.3 × 10一2 , Ka2=6.2 × 10一8。若氨水的浓度为2.0 mo1/ L,溶液中的c(OH-)= mo1/ L;将SO2通入该氨水中,当c(OH-)降至2.0 × 10一6mo1/ L时,溶液中的
 =。
=。
-
(4) 将AgCl分别放入:①5 mL水 ②10 mL 0.1 mol·L-1 MgCl2溶液③40 mL 0.3mol·L-1 盐酸溶液中溶解至溶液饱和 ④20 mL 0.5mol·L-1 NaCl溶液 ,各溶液中Ag+的浓度分别为a、b、 c、d,它们由大到小的排列顺序是(用字母表示)。
下列各组离子一定能大量共存的是( )
A . 在碱性溶液中:CO32-、K+、S2-、Na+
B . 在含有大量Ba2+的溶液中:NO3-、AlO2-、Na+、HCO3-
C . 水电离出来的c(H+)=10-13mol/L 的溶液:K+、HCO3-、Br+、Ba2+
D . 在中性溶液中:K+、Cl-、Al3+、NO3-
下列物质的水溶液在空气中小心加热蒸干灼烧至质量不再减少,能得到较纯净的原溶质的是( )
①CuSO4 ②FeSO4 ③K2CO3 ④Ca(HCO3)2 ⑤NH4HCO3 ⑥KMnO4 ⑦FeCl3
A . 全部都可以
B . 仅③
C . 仅①③
D . 仅①③⑥
常温下0.1 mol/L氨水的pH=a,下列能使溶液的pH=(a-1)的措施是( )
A . 将溶液稀释到原体积的10倍
B . 加入适量的氯化铵固体
C . 加入等体积0.2 mol/LNaOH溶液
D . 提高溶液的温度(不考虑挥发)
下列物质的水溶液因水解而显酸性的是( )
A . Na2CO3
B . NaHSO4
C . NH4Cl
D . NaOH
某二元酸(化学式用H2B表示)在水中的电离方程式是:H2B=H++HB-;HB-  H++B2- , 回答下列问题:
H++B2- , 回答下列问题:
-
(1) NaHB溶液显(填“酸性”、“中性”或“碱性”或“无法确定”),理由是。
-
(2) 某温度下,向0.1mol·L-1的NaHB溶液中滴入0.1mol·L-1KOH溶液至中性,此时溶液中以下关系一定正确的是(填序号)。
a.c(H+)·c(OH-)=1×10-14 b.c(Na+)+c(K+)=c(HB-)+2c(B2-)
c.c(Na+)>c(K+) d.c(Na+)+c(K+)=0.05 mol·L-1
-
(3) 已知0.1mol·L-1NaHB溶液的pH=2,则0.1 mol·L-1H2B溶液中氢离子的物质的量浓度可能是0.11mol·L-1(填“<”、“>”或“=”);理由是。
下列反应不属于水解反应或水解方程式正确的是( )
①HCl+H2O  H3O++Cl− ②NH
H3O++Cl− ②NH  + H2O
+ H2O  NH3·H2O + H+
NH3·H2O + H+
③Na2CO3+2H2O  H2CO3+2NaOH ④Al2(CO3)3+2H2O=2Al(OH)3↓+3CO2↑
H2CO3+2NaOH ④Al2(CO3)3+2H2O=2Al(OH)3↓+3CO2↑
A . ①②
B . ②④
C . ①②④
D . 全部
将  溶于水配成
溶于水配成 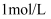 的溶液,溶解过程如图所示.
的溶液,溶解过程如图所示.
 溶于水配成
溶于水配成 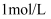 的溶液,溶解过程如图所示.
的溶液,溶解过程如图所示. 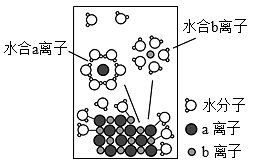
下列说法正确的是( )
A . a离子为Na+ , b离子为Cl-
B . 溶液中含有  个水合
个水合  C . 溶液中存在
C . 溶液中存在 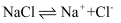 D . 水分子与
D . 水分子与  晶体作用表明水分子中氧原子端带负电
晶体作用表明水分子中氧原子端带负电
 个水合
个水合  C . 溶液中存在
C . 溶液中存在 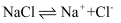 D . 水分子与
D . 水分子与  晶体作用表明水分子中氧原子端带负电
晶体作用表明水分子中氧原子端带负电
下列物质不能导电的是( )
A . 稀硫酸
B . 液态HCl
C . 熔融NaCl
D . 石墨棒
某实验小组要进行Cl2的制取并回收MnCl2的实验。下列装置能达到实验目的的是( )
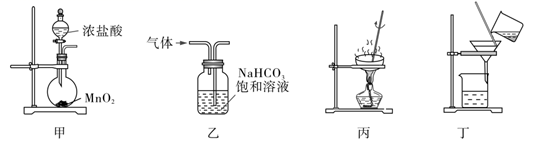
A . 用装置甲制取Cl2
B . 用装置乙除去Cl2中的少量HCl气体
C . 用装置丙蒸干MnCl2溶液制MnCl2·4H2O
D . 用装置丁分离MnO2和MnCl2溶液
下列物质①Cu ②SO2 ③NaCl溶液
④盐酸 ⑤熔融的BaSO4 ⑥NH3 ⑦酒精 ⑧硫酸溶液 ⑨固体NaOH ⑩固体NaHCO3
-
(1) 其中属于电解质的有;
-
(2) 属于非电解质的有;
-
(3) 能导电的有;
-
(4) 上述物质中发生离子反应为OH-+H+=H2O的组合
-
(5) ⑨和⑩在水溶液中反应的离子方程式:
下列各组离子能大量共存且溶液为无色的是( )
A . Na+、NO  、Cl-、Cu2+
B . Mg2+、Cl-、OH-、K+
C . K+、Cl-、SO
、Cl-、Cu2+
B . Mg2+、Cl-、OH-、K+
C . K+、Cl-、SO  、NO
、NO  D . K+、Fe3+、NO
D . K+、Fe3+、NO  、Cl-
、Cl-
 、Cl-、Cu2+
B . Mg2+、Cl-、OH-、K+
C . K+、Cl-、SO
、Cl-、Cu2+
B . Mg2+、Cl-、OH-、K+
C . K+、Cl-、SO  、NO
、NO  D . K+、Fe3+、NO
D . K+、Fe3+、NO  、Cl-
、Cl-
下列物质属于电解质且在该状态下能导电的是( )
A . 氯水
B . HCl
C . Cu
D . 熔融NaCl
常温下,某研究小组用数字传感器探究AgSCN的沉淀溶解平衡(AgSCN是白色沉淀)。实验测得悬浊液中溶解的SCN-浓度变化如图所示,其中a点表示AgSCN溶于KNO3溶液形成的悬浊液。下列说法错误的是( )
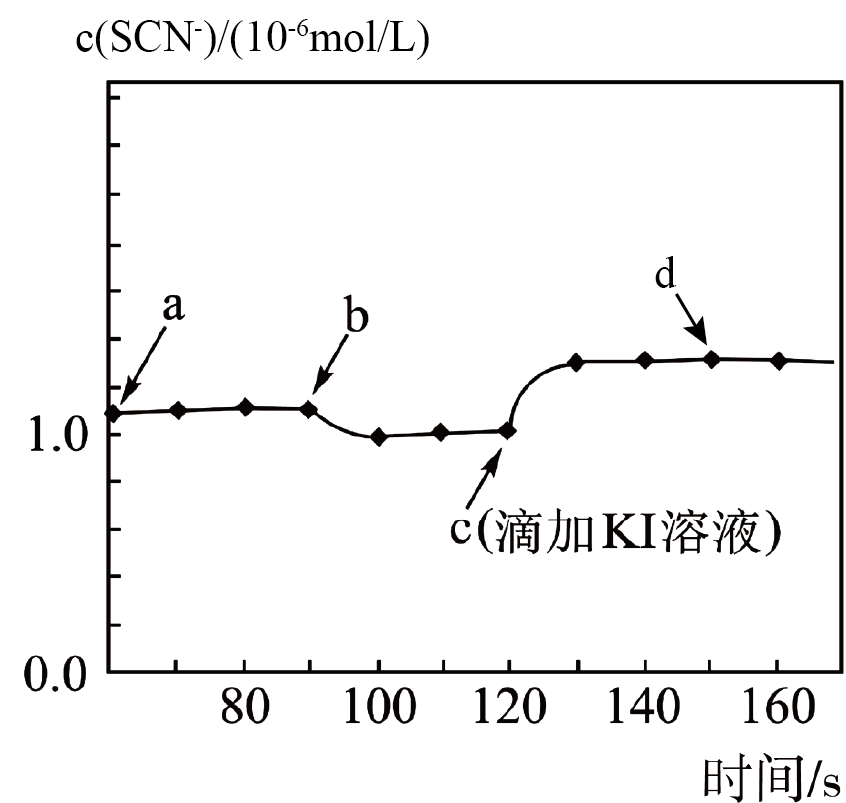
A . 图中b点可能是加少量水稀释了
B . 图中c点后有黄色沉淀生成
C . 图中d点c(Ag+)<c(SCN-)
D . 由图可知:Ksp(AgI)<Ksp(AgSCN)
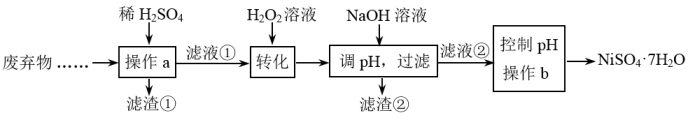
硫酸镍晶体是重要的工业原料。某学习小组用处理过的工厂废弃物(主要含NiO、Fe2O3和Fe3O4 , 还有少量其他不溶性物质)制备硫酸镍晶体(NiSO4·7H2O),部分工艺流程如下:
常温下溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 | Ni2+ | Fe3+ | Fe2+ |
开始沉淀时(c=0.01mol·L−1)的pH | 7.2 | 2.2 | 7.5 |
沉淀完全时(c=1.0×10−5mol·L−1)的pH | 8.7 | 3.2 | 9.0 |
回答下列问题:
-
(1) “滤液①”中含有的金属离子是;滤渣②的成分为。
-
(2) 操作a所用到的玻璃仪器有。
-
(3) 加H2O2的目的是(用离子方程式表示)。
-
(4) 已知滤液②中c(Ni2+)=0.01mol·L−1 , 进行操作b时应控制pH范围为,操作b为、过滤、洗涤、干燥。
-
(5) 利用上表数据,计算常温下Fe(OH)3的Ksp=。
下列说法正确的是( )
A . 强电解质都是离子化合物,而弱电解质都是共价化合物
B . SO2的水溶液能导电,则SO2为电解质
C . Cl2不导电,则Cl2为非电解质
D . BaSO4难溶于水,但BaSO4属于强电解质
最近更新
- 国际互联网上报道“目前世界上约有20亿人患有缺铁性贫血”,这里的“铁”是指()A. 四氧化三铁 B. 铁单质 C. 氧化
- Hawking is one of the most famous ___________(physic) in the
- 读图一和图二, 回答下列问题。 (1) 图一中阴影部分代表的农业地域类型是( ) A.大
- 如图,是我们学过的用直尺画平行线的方法示意图,画图原理是( )A.同位角相等,两直线平行
- 如图所示,竖直平面内有一半径为r、内阻为R1、粗细均匀的光滑半圆形金属环,在M、N处与相距为2r、电阻不计的平行光滑金属
- After the mew technique was introduced ,the factory produced
- 函数的图象大致为( ) A. B.
- 下列各句中加点的成语,使用恰当的一句是( ) A、罗兰·艾默里奇执导的《2012》在全球公映,影片中用电脑技术制作的
- .读英国人均国民生产总值的指数变化(1500-1900年)示意图,分析正确的是( ) A.英国国民生产总值领先世界
- 2015年国家相继出台了各项楼市政策,其中二套房贷最低首付款比例调整为不低于40%,相比此前, 首付款的比例下调了两
- The old theatre will close soon__________ some extradonation
- President-elect Barack Obama has asked his economic team for
- 14.下列各句中,没有语病的一句是(3分) A.假如城市化过程中不注意城市之间的相互影响,不考虑污染物稀释扩散结构的话,
- 如图,Rt△ABC中,∠ACB=90°,D、E、F分别是AB、AC、BC的中点,连接DE、DF、CD,如果AC=BC,那
- 已知A只能由某种烯烃与氢气加成而得到,且A分子中含碳82.8%;B、C分别为A的一氯代物。A—I物质有如下转化关系(反应
- 仿照例句的形式,在横线处填上恰当的语句。 例句:狂妄自大的民族不喜欢聆听,他们只会穷兵黩武,贪欲和傲慢遮挡了他们的视线。
- 下列既是复分解反应,又是中和反应的是() A.CuO+2HCl=CuCl2+H2O B.BaCl2+H2SO4=B
- .有理数、在数轴上的位置如图所示,则化简的结果为( ) A.B.-C.D.
- 孟子说:“天将降大任于斯人也,必先苦其心志,劳其筋骨。”我们读过的名著中不少人物的经历都能印证这个观点。请仿照示例,为这
- 以前,我国一直以“地大物博”而自豪,而现在却有“地大物薄”之说。我国自然资源的特征是 A.总量不足,种类多



