常见无机物及其应用 知识点题库
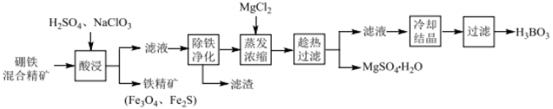
已知:UO22+在pH为4~5的溶液中生成UO2(OH)2沉淀。
回答下列问题:
-
(1) “酸浸”时,为了提高浸出率可采取的措施有:(至少答两个措施),该步骤中NaClO3可将UO2转化为UO22+ , 则该反应的离子方程式为 。
-
(2) “除铁净化”需要加入 (填化学式)把溶液pH调节至4~5,滤渣的成分是。
-
(3) “蒸发浓缩”时,加入固体MgCl2的作用是 。
-
(4) 铁精矿(Fe3O4、Fe2S)经过一系列加工后,可用于制备氢氧化铁固体。已知T℃Ksp[Fe(OH)3]=4.0×10-39、Ksp[Fe(OH)2]=8.0×10-16 、Kw=10-a , 回答下列问题:
①在T℃,假设Fe3+水解的离子方程式是:Fe3+(aq)+3H2O(l)= Fe(OH)3 (s)+3H+(aq),则该条件下Fe3+水解反应的平衡常数K=(用含a的字母表示)。
②在T℃向饱和的Fe(OH)3、Fe(OH)2混合溶液中,加入少量NaOH固体(忽略溶液体积变化),则溶液中的
 会(填“变大”“变小”或“不变”),请结合相关数据推理说明: 。
会(填“变大”“变小”或“不变”),请结合相关数据推理说明: 。
|
|
A |
B |
C |
D |
|
垃圾 |
废易拉罐 |
废塑料瓶 |
废荧光灯管 |
不可再生废纸 |
|
垃圾分类 |
可回收物 |
其他垃圾 |
有害垃圾 |
可燃垃圾 |
-
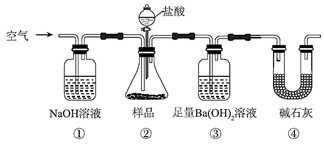
(1) 上述实验所利用的过氧化钠跟水反应的特点是:
第一,有氧气生成,第二,。Na2O2 跟水反应的离子方程式是。
-
(2) 某研究性学习小组拟用如图所示装置(气密性良好)进行实验,以证明上述特点。用以验证反应的第一个特点的实验操作及现象是:。
用以验证第二个反应特点的实验操作及现象是:。
-
(3) 实验(2)向试管中加水至固体完全溶解且不再有气泡生成后,取出试管,向试管中滴入酚酞试液,发现溶液先变红后褪色,为探究其原因,该小组同学从查阅有关资料中得知:Na2O2 与水反应可生成 H2O2 , H2O2 具有强氧化性和漂白性。
请设计一个简单的实验,验证 Na2O2 跟足量水充分反应后的溶液中有 H2O2 存在。(只要求写出实验所用的试剂及观察到的现象)试剂:;现象:。
-
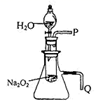
(4) 该小组同学提出用定量的方法探究 Na2O2 跟水反应后的溶液中是否含有 H2O2 , 其实验方法为: 称取 2.6gNa2O2 固体,使之与足量的水反应,测量产生 O2 的体积并与理论值比较,即可得出结论: 测量气体体积时,必须等到试管和量筒内的气体都冷却至室温时进行,应选用如图装置中的(忽略导管在量筒中所占的体积,导管伸入量筒的长度不同)(填字母)
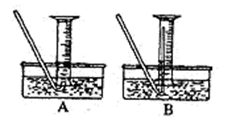
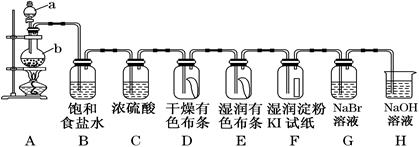
参考装置图回答下列问题:
-
(1) 请指出仪器a的名称写出装置A中反应的离子方程式
-
(2) 在装置D中可观察到的现象是,装置E中可观察到的现象是。
-
(3) 装置B的作用为,装置C的作用为,装置H的作用为,
-
(4) 写出装置H中的离子方程式。
| 选项 | 物质(括号内为杂质) | 除杂试剂或物质 | 除杂操作 |
| A | Fe(Cu)固体 | 磁铁 | 吸引后弃去剩余固体 |
| B | FeCl2(FeCl3)溶液 | Fe | 加入过量 Fe 粉, 充分反应后过滤 |
| C | CO2(HCl)气体 | 饱和 NaHCO3 溶液、浓 H2SO4 | 依次充分洗气 |
| D | Na2CO3(NaHCO3)溶液 | CO2 | 通入过量 CO2 |
 CuSO4 + SO2↑ + 2H2O。现将一定量的铜与20mL 18mol/L浓硫酸反应,当铜全部溶解时测得生成气体体积为448mL(标况下)。试计算:
CuSO4 + SO2↑ + 2H2O。现将一定量的铜与20mL 18mol/L浓硫酸反应,当铜全部溶解时测得生成气体体积为448mL(标况下)。试计算:
-
(1) 加入铜的质量是多少?
-
(2) 将反应后的溶液稀释至100mL,求稀释后溶液中硫酸根离子的物质的量浓度?
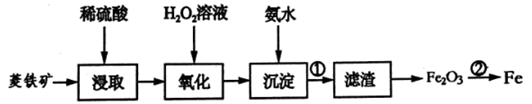
-
(1) “氧化”和“沉淀”是将“浸取”过程中产生的 Fe2+转化为Fe(OH)3沉淀, 则操作①的名称为(填“蒸发”或“过滤”),所用到主要玻璃仪器有 。
-
(2) 写出“沉淀” 过程中发生反应的离子方程式: 。
下列说法错误的是( )
-
(1) B元素在元素周期表中的位置是,B、C、D形成的简单离子的半径由大到小的顺序是(用化学符号表示)。
-
(2) B与C能形成一种淡黄色的固体,其电子式为,它能用于呼吸面具的原因是(用其中一个化学方程式表示)。
-
(3) D的单质常用于焊接钢轨,请用化学方程式表示其反应原理。D、E的最高价氧化物对应水化物之间发生反应的离子方程式为。
 He与地球上的
He与地球上的  He互为同素异形体
B .
He互为同素异形体
B .  He和
He和  H互为同位素
C .
H互为同位素
C .  He原子核外电子数为3
D . 居里夫人用
He原子核外电子数为3
D . 居里夫人用 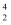 He原子核轰击
He原子核轰击 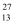 Al原子核,得到核素Y:
Al原子核,得到核素Y: 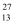 Al+
Al+ 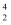 He→Y+
He→Y+  n,则Y为磷元素
n,则Y为磷元素
 2SO3)的说法正确的是( )
2SO3)的说法正确的是( )
①含有3种元素 ②属于碳的同素异形体 ③属于氧化物 ④属于盐 ⑤可由CO2与Mg(OH)2反应生成制得
-
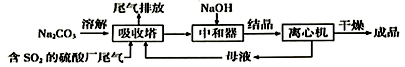
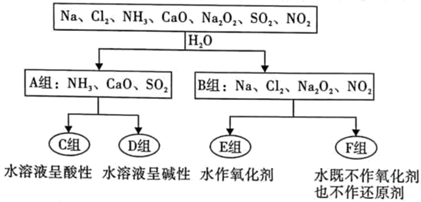
(1) 根据物质与水反应的情况,分成A、B组的分类依据是。
-
(2) A组中的CaO经常用作食品包装袋中的干燥剂,CaO所属物质类别为(填序号)。
①金属氧化物 ②酸性氧化物 ③碱性氧化物 ④两性氧化物
-
(3) B组物质中,可用作潜水艇供氧剂的是(填化学式)。写出B组中红棕色气体与水反应的化学方程式。
-
(4) 工业上常用D组中的(填化学式)消除C组中物质对大气的污染。
-
(5) 实验室用
 制备
制备 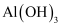 时,可选择上述物质中某一物质的水溶液,该过程涉及的离子反应方程式为。
时,可选择上述物质中某一物质的水溶液,该过程涉及的离子反应方程式为。
-
(6) C组中某一物质可使酸性
 溶液褪色,用离子方程式表示溶液褪色的原因。
溶液褪色,用离子方程式表示溶液褪色的原因。
-
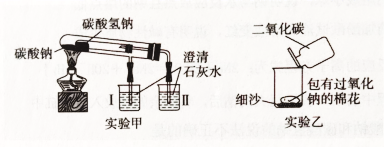
(1) 实验甲在加热过程中能观察到产生白色沉淀的烧杯是(填“I”或“II”),请写出实验甲中较不稳定物质的分解方程式。
-
(2) 实验乙用来探究Na2O2与CO2的反应,观察到的实验现象为包有Na2O2的棉花着火。写出Na2O2与CO2反应的化学方程式:。
-
(3) 下列对Na2O2的叙述中,正确的是___________。A . Na2O2能与酸反应生成盐和水,所以Na2O2是碱性氧化物 B . Na2O2能与水反应,所以Na2O2可以作气体的干燥剂 C . Na2O2与CO2反应时,Na2O2只作氧化剂 D . Na2O2与CO2反应产生氧气,可用于呼吸面具中氧气的来源
|
实验 |
装置 |
试剂 |
现象 |
|
① |
|
紫色的石蕊试液 |
溶液先变红后褪色 |
|
② |
|
产生气泡 |
|
|
③ |
|
产生白色沉淀 |
|
|
④ |
Na2S |
产生黄色沉淀 |
由上述实验可得新制氯水的性质与对应的解释或离子方程式不相符的是( )
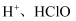 B . 实验②发生的反应为
B . 实验②发生的反应为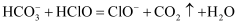 C . 实验③说明新制氯水中有
C . 实验③说明新制氯水中有 D . 实验④体现氯气的氧化性,S2-+Cl2=S↓ +2Cl-
D . 实验④体现氯气的氧化性,S2-+Cl2=S↓ +2Cl-
-
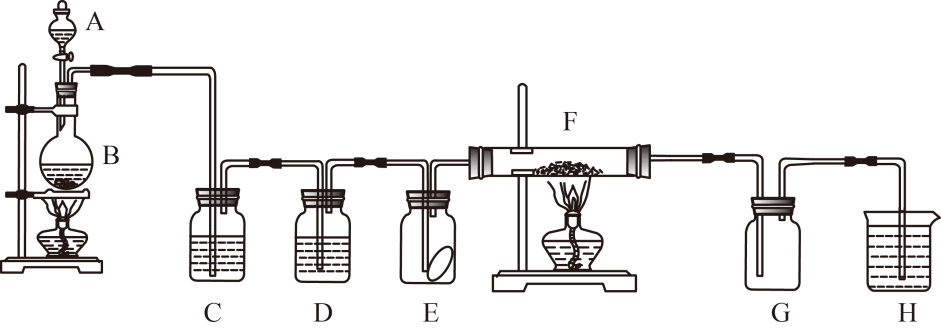
(1) 仪器A的名称为。写出装置B中的化学反应方程式:。
-
(2) 装置C中盛装的试剂是,D中试剂是,写出F中反应的化学反应方程式:。
-
(3) H中的试剂为氢氧化钠溶液,其作用是,写出H中的反应的离子方程式。
 与
与 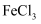 溶液的反应。
溶液的反应。
-
(1) 实验一:用如图所示实验装置制备
 ,并将足量
,并将足量  通入
通入 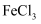 溶液中,溶液迅速变为血红色;停止通入气体,将血红色溶液密闭放置5小时后,溶液变为浅绿色。
溶液中,溶液迅速变为血红色;停止通入气体,将血红色溶液密闭放置5小时后,溶液变为浅绿色。 
制备
 的化学反应方程式为;
的化学反应方程式为; -
(2) 仪器a的名称为,按图示装好药品后,打开K之前的操作是。
-
(3) 某同学取适量酸性
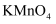 于试管中,滴入几滴血红色溶液,溶液的紫色褪去,据此推断血红色溶液中含有Fe2+。此结论(填“正确”、“不正确”),理由是。
于试管中,滴入几滴血红色溶液,溶液的紫色褪去,据此推断血红色溶液中含有Fe2+。此结论(填“正确”、“不正确”),理由是。
-
(4) 实验二:探究血红色溶液产生的原因
实验过程如下表:
实验序号
假设
实验内容
结论
①
与溶液中c(H+)有关
取适量上述血红色溶液,滴入Y溶液,溶液又变为黄色
假设不成立
②
与c(H2SO3)或c(SO2)有关
1溶液中,滴入1mol/LNaHSO3溶液,溶液呈血红色,再逐滴滴入HCl溶液,出现×××现象
假设不成立
③
与c(
 )或c(
)或c(  )有关
)有关在FeCl3溶液中加入Na2SO3溶液,立即变为血红色。
实验①中,Y是(填化学式);实验②中现象是;实验③的结论是。
-
(5) 为了进—步探究血红色物质产生主要原因,又进行了以下实验:
在0.5mL1mol/L的FeCl3溶液中,加入浓度相同的Na2SO3溶液V1mL,NaHSO3溶液V2mL并混合均匀,改变V1、V2的值并维持V1+V2=4.0进行多组实验,测得混合溶液的吸光度与
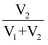 的关系如图所示。(已知吸光度越大,溶液颜色越深)。
的关系如图所示。(已知吸光度越大,溶液颜色越深)。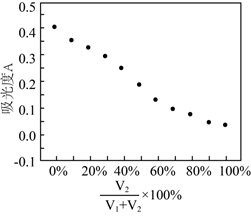
①维持V1+V2=4.0的目的是。
②该实验得出的结论是。
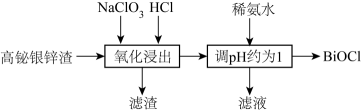
已知:BiCl +H2O
+H2O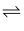 BiOCl↓+2H++3Cl-
BiOCl↓+2H++3Cl-
2BiOCl(白色)+2OH- 2Cl-+H2O+Bi2O3(黄色)
2Cl-+H2O+Bi2O3(黄色)
-
(1) “氧化浸出”生成BiCl
 的实验装置如图所示。
的实验装置如图所示。
①写出生成BiCl
 的离子方程式:。
的离子方程式:。②工业在“氧化浸出”时常加入适量NaCl(s),其目的是。
③反应一段时间后,Bi完全浸出。将滤渣加入足量稀硝酸中,充分反应后,观察到滤渣部分溶解。该滤渣的成分为。
-
(2) 加入稀氨水调节溶液pH不宜过大的原因是。
-
(3) 请补充完整利用含少量Fe(OH)3杂质的BiOCl粗品制备Bi2O3的实验方案:,过滤、洗涤、干燥,得Bi2O3。(须使用的试剂有:1mol·L-1H2SO4溶液、4mol·L-1NaOH溶液、1mol·L-1BaCl2溶液、蒸馏水)
- 已知集合A={0,1,2},则满足A∪B={0,1,2}的集合B的个数为 .
- 分析肽链,得到以下结果(单位:个)元素或基团 C H O N 氨基 羧基201 348 62 53 3 2182 294
- 图A为某生物体细胞有丝分裂示意图,图B表示在一个细胞周期(G1、S、G2组成分裂间期,M为分裂期)中细胞核内DNA含量的
- 跟元素的化学性质关系最密切的是原子的 【 】
- 铁钉和碳棒用导线连接后,浸入到0.01 mol·L-1 NaCl溶液中,可能发生的是( ) ①碳棒上有氢气析出
- 填入下列句子横线处的词语,最恰当的一组是①“看病难,看病贵”只是医疗体制矛盾暴露出来的 ,只有加快医疗体制改革
- 一颗人造卫星绕地球作匀速圆周运动,其轨道半径为月球绕地球轨道半径的1/3,则此卫星运行的周期约是A.1~4天之间 B.
- (2011广西梧州,17,3分)图9是由两个长方体组合而成的一个立体图形的三视图,根据图中所标尺寸(单位:mm),计算出
- 号称世界最大生态工程的“三北”防护林跨越的地区是 A.东北、华北、西北 B.华北、华东、华中
- 下列反应的离子方程式正确的是A.石英与烧碱溶液共热:SiO2+2OH-SiO32-+H2OB.在氯化铝溶液中滴加过量的氨
- 一辆电动自行车的铭牌上给出了如下的技术参数表:规格 后轮驱动直流永磁毂电机 车型 26″电动自行车 额定机械功率 120
- 已知函数图象上斜率为3的两条切线间的距离为,函数. (1)若函数g(x)在x=1处有极值,求g(x)的解析式; (2)若
- (08济宁高一历史期末)秦始皇开创的中央集权制度对我国历史发展产生的最重要影响是 ( ) A.维护了国家
- 做自由落体运动的物体,如果下落过程中某时刻重力突然消失,物体的运动情况将是( ) A.悬浮在空中不动
- 建国六十周年庆典上,天安门广场以复兴之路为主题,举行了盛大的阅兵式和群众游行。打头的游行方阵分别命名为:开天辟地、艰苦创
- 请用一句话概括下面新闻的主要内容。(不超过20个字)(5分)据《泰晤士报》12月3日报道,世界顶级气候科学家之一、美国宇
- 将函数的图象向右平移个单位后,其图象的一条对称轴方程可以是 .
- 人体内的血液能按一定的方向流动,其原因是 A.肌肉收缩压挤血管 B.血管壁有一定的弹性 C.
- 如图,将一根塑料绳一端扎紧,把绳尽可能撕成细丝,用手从上向下捋几下,观察到的现象是_______,说明的道理是_____
- 下列物质在生活中应用时,起还原作用的是( ) A.铁粉作食品袋内的脱氧剂 B.用生石灰做干燥剂 C.漂粉




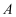
 溶液
溶液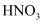 酸化的
酸化的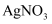 溶液
溶液


