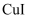常见无机物及其应用 知识点题库
向四支试管中分别加入少量不同的无色溶液进行如下操作,结论正确的是( )
| 操作 | 现象 | 结论 | |
| A | 先滴加BaCl2溶液,再加稀HNO3 | 生成白色沉淀,且沉淀不溶解 | 原溶液中有SO42﹣ |
| B | 滴加氯水和CCl4 , 振荡、静置 | 下层溶液显紫红色 | 原溶液中有I﹣ |
| C | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有Na+、K+ |
| D | 滴加NaOH溶液加热,将红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
A . A
B . B
C . C
D . D
下列“实验方案”不宜用于完成“实验目的”的是( )
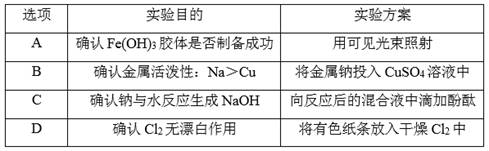
A . A
B . B
C . C
D . D
化学与人类生活、社会可持续发展密切相关,下列说法中错误的是( )
A . 煤的气化与液化均为化学变化
B . 大自然利用太阳能最成功的是植物的光合作用
C . 砖瓦、陶瓷、渣土、普通一次性电池、鱼骨等属于其他垃圾
D . 用CO2合成可降解的聚碳酸酯塑料,可以实现“碳”的循环利用
A~H为中学化学中常见的物质,转化关系如图所示,其中“○”代表化合物,“□”代表单质,A为医学上治疗胃酸过多的一种药剂,G为淡黄色固体,C在通常状况下为无色液体。
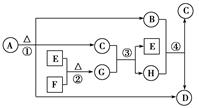
请回答下列问题:
-
(1) G的化学式为。
-
(2) 反应①②③④中(填序号)属于氧化还原反应。
-
(3) 写出下列反应的化学方程式:
A→B+C+D:。
F+C:。
“皮鞋很忙”的恶搞段子曾经风靡网络,揭露了某些行业用烂皮鞋制造酸奶或毒胶囊的不法行为。央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
-
(1) 已知
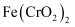 中铬元素是+3价,则其中铁元素是价。
中铬元素是+3价,则其中铁元素是价。 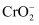 是一种酸根离子,则
是一种酸根离子,则 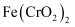 属于(填“酸”“碱”“盐”或“氧化物”)。
属于(填“酸”“碱”“盐”或“氧化物”)。
-
(2) 明胶的水溶液和
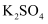 溶液共同具备的性质是(填序号)。
溶液共同具备的性质是(填序号)。 a.都不稳定,密封放置沉淀
b.能产生丁达尔效应
c.分散质粒子可通过滤纸
-
(3) 现有10mL明胶的水溶液与5mL
 溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明
溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明  能够透过半透膜:。
能够透过半透膜:。
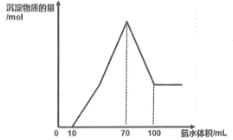
现有一包铝粉和铜粉的混合物,用100mL 某浓度的稀硝酸溶解,生成的气体全部是NO, 待粉末完全溶解后,逐滴加入3mol•L-1 的氨水,产生沉淀的物质的量与加入氨水的体积关系如图。
-
(1) 写出图中滴加氨水10~100mL 的过程中铜元素参与反应的离子方程式。
-
(2) 所用硝酸的物质的量浓度为mol• L-1;写出简要计算过程。
下列关于NO2和SO2的说法中错误的是( )
A . 它们都是易溶于水的有色气体
B . 它们都是具有刺激性气味的有毒气体
C . 大气中的NO2和SO2可以形成酸雨
D . 提高机动车尾气排放标准有利于提高空气质量
已知:  。向含0.01 mol
。向含0.01 mol 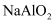 和0.02 mol NaOH的稀溶液中缓慢通入CO2 , 溶液中,
和0.02 mol NaOH的稀溶液中缓慢通入CO2 , 溶液中,  随通入的
随通入的  的变化如图,下列对应关系正确的是( )
的变化如图,下列对应关系正确的是( )
 。向含0.01 mol
。向含0.01 mol 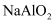 和0.02 mol NaOH的稀溶液中缓慢通入CO2 , 溶液中,
和0.02 mol NaOH的稀溶液中缓慢通入CO2 , 溶液中,  随通入的
随通入的  的变化如图,下列对应关系正确的是( )
的变化如图,下列对应关系正确的是( ) 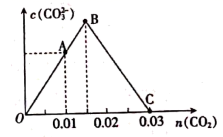
A . A点: 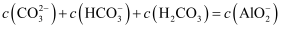 B . B点:
B . B点: 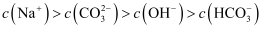 C . C点:
C . C点:  D . O点:
D . O点: 
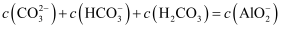 B . B点:
B . B点: 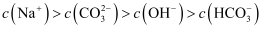 C . C点:
C . C点:  D . O点:
D . O点: 
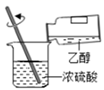
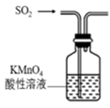
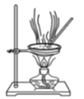
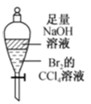
下列实验操作或相关说法合理的是( )
| A | B | C | D |
| | | | |
| 混合浓硫酸和乙醇 | 验证SO2的漂白性 | 蒸干MgCl2溶液制取无水MgCl2 | 充分振荡后下层为无色 |
A . A
B . B
C . C
D . D
三氯氧磷(POCl3)和氯化亚砜(SOCl2)均为重要的化工产品。现以氯气、二氧化硫和三氯化磷为原料,采用二级间歇式反应装置联合制备三氯氧磷和氯化亚砜。实验过程中,控制氯气和二氧化硫通入的体积比为1:1.实验过程示意图如图:
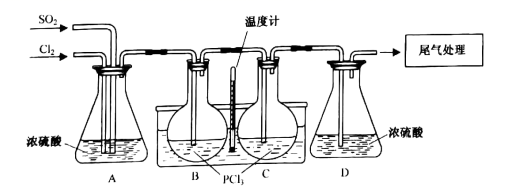
已知:
| 名称 | 熔点/℃ | 沸点/℃ | 溶解性 | 理化性质 |
| 三氯氧磷 | 2 | 105.3 | 可溶于有机溶剂 | 遇水分解 |
| 氯化亚砜 | -105 | 78.8 | 可溶于有机溶剂 | 遇水分解,加热分解 |
-
(1) 实验室制备氯气或二氧化硫时均可能用到的仪器有_______。A . 温度计 B . 酒精灯 C . 分液漏斗 D . 圆底烧瓶
-
(2) A装置的作用为:、、使气体充分混合。
-
(3) 实验开始时需水浴加热,一段时间后改为冷水浴,其原因是。
-
(4) B中发生反应的化学方程式是。
-
(5) 反应5~6小时后,暂停通入气体。将B瓶拆下,C瓶装在图中B瓶处,并在原C瓶处重新装上一个盛有PCl3的圆底烧瓶。继续通气反应一段时间后重复以上步骤,上述操作的优点是;B瓶中的物质可采用.(填实验方法)使其分离。
-
(6) 已知反应前加入三氯化磷550g,最终得到357g氯化亚砜,则三氯氧磷的产率为。
下列三星堆出土的文物属于合金制品的是( )
| | | | |
| A.青铜人面具 | B.椭圆形玉器 | C.陶三足炊器 | D.带孔海贝壳 |
A . A
B . B
C . C
D . D
某研究小组通过实验探究Cu及其化合物的性质,操作正确且能达到实验目的的是( )
A . 将表面有铜绿  的铜器放入盐酸中浸泡,除去铜绿
B . 将铜丝插入浓硫酸中并加热,反应后再加入水,观察硫酸铜溶液的颜色
C . 将
的铜器放入盐酸中浸泡,除去铜绿
B . 将铜丝插入浓硫酸中并加热,反应后再加入水,观察硫酸铜溶液的颜色
C . 将 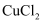 溶液在蒸发皿中加热蒸干,得到无水
溶液在蒸发皿中加热蒸干,得到无水 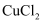 固体
D . 常温下将铜丝伸入盛满氯气的集气瓶中,观察
固体
D . 常温下将铜丝伸入盛满氯气的集气瓶中,观察 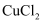 的生成
的生成
 的铜器放入盐酸中浸泡,除去铜绿
B . 将铜丝插入浓硫酸中并加热,反应后再加入水,观察硫酸铜溶液的颜色
C . 将
的铜器放入盐酸中浸泡,除去铜绿
B . 将铜丝插入浓硫酸中并加热,反应后再加入水,观察硫酸铜溶液的颜色
C . 将 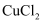 溶液在蒸发皿中加热蒸干,得到无水
溶液在蒸发皿中加热蒸干,得到无水 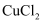 固体
D . 常温下将铜丝伸入盛满氯气的集气瓶中,观察
固体
D . 常温下将铜丝伸入盛满氯气的集气瓶中,观察 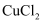 的生成
的生成
根据下列实验操作及现象,可以得出相应实验推论的是。( )
| 选项 | 实验操作 | 实验现象 | 实验推论 |
| A | 向某溶液中加入 | 未产生能使湿润红色石蕊试纸变蓝的气体 | 原溶液中不含有 |
| B | 测定饱和 | 前者 | |
| C | 向红热的木炭滴加浓硝酸 | 产生大量的红棕色气体 | 木炭和浓硝酸反应生成 |
| D | 向 | 有白色沉淀生成,四氯化碳层呈紫色 | 白色沉淀可能为 |
A . A
B . B
C . C
D . D
核心元素的化合价及类别是研究物质性质的两个重要视角。硫及其化合物的分类与相应硫元素的化合价关系如图所示。下列说法错误的是( )
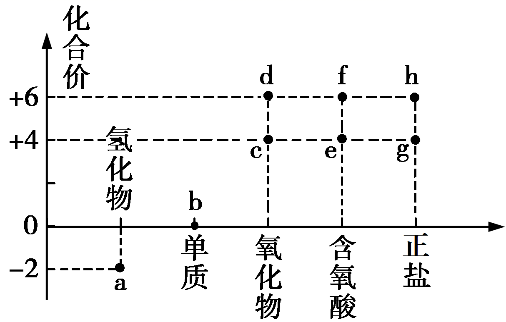
A . 适量的c可作为葡萄酒的添加剂
B . 常温下,a与f的浓溶液反应可生成b和c
C . 将c通入紫色石蕊试液中,溶液先变红后褪色
D . 在自然界中,部分的c会转化成d,最后转化为f或h
已知A是常见的无色液体,M、R是两种常见的金属,M是地壳中含量最多的金属元素的单质,T是淡黄色固体,B、C是无色无味的气体,E是具有磁性的黑色晶体,H是红褐色固体。(注意:有的反应物和生成物未标出)
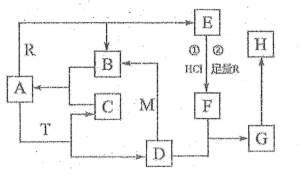
-
(1) 物质T的电子式为,T含有的化学键类型有;
-
(2) D和M在溶液中反应生成B的离子反应方程式为:;
-
(3) G在潮湿空气中变成H的实验现象是,化学方程式为。
-
(4) T和F反应只生成C、H和一种正盐,其离子反应方程式为:。
-
(5) 0.1 mol E和R的混合物,加盐酸后固体全部溶解,共收集到0.02 mol H2 , 且向反应后的溶液中加入KSCN溶液不显红色,则原混合物中铁的物质的量百分数为。
SO2属于严重的大气污染物,可用H2与SO2高温反应消除SO2的污染,其反应原理可分为两步,过程如图所示:
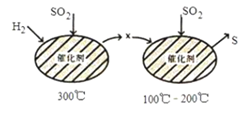
下列说法正确的是( )
A . SO2排放到空气中会形成pH≈5.6的酸雨
B . 可用CuSO4溶液检验是否有X气体生成
C . 在100℃~200℃温度时发生的是置换反应
D . 工业上可用浓硝酸处理工业尾气中的SO2
下列物质性质和用途都正确且相关的是( )
选项 | 性质 | 用途 |
A | FeCl3溶液显酸性 | 用于刻蚀电路板 |
B | SO2具有氧化性 | SO2常用于漂白秸秆、织物 |
C | HF溶液具有酸性 | HF溶液能在玻璃上刻图案 |
D | CH3CH2OH完全燃烧生成二氧化碳和水并放出大量热量 | 乙醇常作清洁能源 |
A . A
B . B
C . C
D . D
关于化合物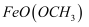 的性质,下列推测不合理的是( )
的性质,下列推测不合理的是( )
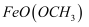 的性质,下列推测不合理的是( )
的性质,下列推测不合理的是( )
A . 与稀盐酸反应生成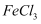 、
、 、
、 B . 隔绝空气加热分解生成
B . 隔绝空气加热分解生成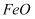 、
、 、
、 C . 溶于氢碘酸(
C . 溶于氢碘酸(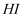 ),再加
),再加 萃取,有机层呈紫红色
D . 在空气中,与
萃取,有机层呈紫红色
D . 在空气中,与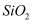 高温反应能生成
高温反应能生成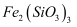
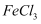 、
、 、
、 B . 隔绝空气加热分解生成
B . 隔绝空气加热分解生成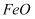 、
、 、
、 C . 溶于氢碘酸(
C . 溶于氢碘酸(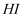 ),再加
),再加 萃取,有机层呈紫红色
D . 在空气中,与
萃取,有机层呈紫红色
D . 在空气中,与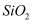 高温反应能生成
高温反应能生成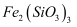
下列实验结论正确的是( )
A . 取适量待测溶液于试管中,滴加硝酸钡溶液和足量稀硝酸,无明显现象,再滴加硝酸银溶液,出现白色沉淀,说明该溶液中一定含有Cl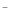 B . 取一根洁净的铂丝,在酒精灯火焰上灼烧至无色,然后蘸取少量待测液,置于火焰上灼烧,火焰呈黄色,则溶液中一定含有氯化钠
C . 取适量待测液于试管中,滴入足量KSCN溶液,无明显现象,再滴入适量氯水,溶液变为血红色,则原待测液中一定含有Fe3+
D . 于试管中加热某固体纯净物样品,试管口出现小水珠,则该样品中一定存在结晶水
B . 取一根洁净的铂丝,在酒精灯火焰上灼烧至无色,然后蘸取少量待测液,置于火焰上灼烧,火焰呈黄色,则溶液中一定含有氯化钠
C . 取适量待测液于试管中,滴入足量KSCN溶液,无明显现象,再滴入适量氯水,溶液变为血红色,则原待测液中一定含有Fe3+
D . 于试管中加热某固体纯净物样品,试管口出现小水珠,则该样品中一定存在结晶水
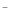 B . 取一根洁净的铂丝,在酒精灯火焰上灼烧至无色,然后蘸取少量待测液,置于火焰上灼烧,火焰呈黄色,则溶液中一定含有氯化钠
C . 取适量待测液于试管中,滴入足量KSCN溶液,无明显现象,再滴入适量氯水,溶液变为血红色,则原待测液中一定含有Fe3+
D . 于试管中加热某固体纯净物样品,试管口出现小水珠,则该样品中一定存在结晶水
B . 取一根洁净的铂丝,在酒精灯火焰上灼烧至无色,然后蘸取少量待测液,置于火焰上灼烧,火焰呈黄色,则溶液中一定含有氯化钠
C . 取适量待测液于试管中,滴入足量KSCN溶液,无明显现象,再滴入适量氯水,溶液变为血红色,则原待测液中一定含有Fe3+
D . 于试管中加热某固体纯净物样品,试管口出现小水珠,则该样品中一定存在结晶水
中华文化源远流长,从古至今有很多的发明创造,下列有关说法正确的是( )
A . 北京冬奥会礼服内胆添加了石墨烯发热材料,石墨烯属于烯烃类物质
B . “天机芯”是全球首款异构融合类电脑芯片,其主要成分和光导纤维相同
C . 我国唐代赵蕤所题《嫘祖圣地》碑文就记载种桑养蚕之法,蚕丝水解可以生成葡萄糖
D . 《本草纲目》中的“石碱”条目下写道:“采蒿萝之属,晒干烧灰,以水淋汁,久则凝淀如石,浣衣发面”,说明石碱的主要成分为K2CO3
最近更新
- 纯锌跟稀H2SO4反应速率很小,为了加快锌的溶解和放出H2的速率,并且使产生H2的量不变,当稀H2SO4过量时,可向其中
- 已知NaHSO4在水中的电离方程式为:NaHSO4=Na++H++SO.某温度下,向pH=6的蒸馏水中加入NaHSO4晶
- ---- I haven’t found any money though I’ve searched the draw
- 在正四面体ABCD中,E,F分别为BC,AD的中点, 求异面直线AE与CF所成角的大小。
- 已知向量a=,b=(x,1),其中x>0,若(a-2b)∥(2a+b),则实数x=.
- 自有人类以来,思想领域内的斗争就一刻也没有停止过,而哲学上的斗争是最高形式的斗争。这里说的哲学上的斗争,最根本的是(
- 当时,下面的程序段结果是__________。
- 隋唐时期,三省长官都是宰相,后来,常常同时有七八个宰相议政。统治者这样做的直接目的是( ) A.加强对地方的控
- 2.若以图代表与生命系统相关概念的范围,其中正确的是() A、生物大分子、细胞、组织 B、个体
- Follow your doctor’s advice, ______ yourcough will get wors
- C_____________ is a small tube of paper containing tobacco w
- 足球运动员将一只沿水平方向飞来的足球反向踢回的过程中,若足球动量变化量的大小为10kg·m/s,则 ( )
- Modern Chinese use the solar calendar(阳历)as English people d
- 已知向量a,b满足,则 A. 0 B. C. 4 D. 8
- (8分)如图,在电线杆上的C处引拉线CE、CF固定电线杆,拉线CE和地面成60°角.在离电线杆6米的B处安置测角 仪,
- 如果一个数的绝对值与这个数的商等于-1,则这个数是( )A.正数 B
- 2011年6月30日开通的京沪高速铁路,列车运行时间约为4小时55分钟,回答24—25题。 24.京沪高速铁路建设
- 下列各句中,没有语病的一项是( ) A.这样重大的问题,你事先既不请示,过后更不报告,这种做法是不符合财务制度的。
- 2010年3月5日十一届全国人大三次会议通过的新选举法做出如下的规定:上述规定( ) ①体现了国家机构民主集中制
- 细菌蛋白质在极端环境条件下可通过肽链之间的二硫键维持稳定。已知不同的多肽产物可因分子量不同而以电泳方式分离。下列左图是一



 溶液
溶液
 溶液和饱和
溶液和饱和  溶液的
溶液的  值
值 的水解程度小于
的水解程度小于 

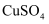 溶液中加入
溶液中加入  溶液,再加入四氯化碳振荡
溶液,再加入四氯化碳振荡