常见无机物及其应用 知识点题库
化学与我们的日常生活密切相关。按要求回答以下问题:
-
(1) 明矾可用作净水剂,其化学式是,漂白粉的有效成分是 (填化学式)。
-
(2) 光导纤维在强碱性条件下容易发生“断路”,用离子方程式解释其原因
-
(3) 小苏打通常用来治疗胃酸过多,但同时患有胃溃疡的病人却不能服用,其原因是(用化学方程式表示)。
-
(4) SO2和氯水都有漂白性,将SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象那样。请你分析该现象的原因(用化学方程式表示)
有关Al与NaOH溶液反应的说法中,正确的是( )
A . 还原产物是H2 , 且由H2O还原所得的H2与由NaOH还原所得的H2物质的量之比为2∶1
B . Al是还原剂,NaOH既不是氧化剂也不是还原剂
C . 此反应说明铝具有两性
D . 此反应中,只有H2O是氧化剂,3molNaOH参加反应生成2molH2
下列实验现象与新制氯水中的某些成分(括号内物质)没有关系的是( )
A . 铁片加入新制氯水中,有无色气泡产生(H+)
B . 将NaHCO3固体加入新制氯水中,有无色气泡产生(HClO)
C . 向新制氯水中滴加石蕊溶液,溶液先变红后褪色(H+、HClO)
D . 滴加AgNO3溶液有白色沉淀产生(Cl-)
用如图所示实验装置进行相关实验探究,其中装置不合理的是( )
A . 升华提纯碘 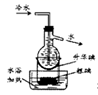 B . 鉴别纯碱与小苏打
B . 鉴别纯碱与小苏打 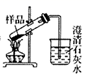 C . 证明Cl2能与烧碱溶液反应
C . 证明Cl2能与烧碱溶液反应 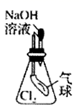 D . 探究钠与Cl2反应
D . 探究钠与Cl2反应 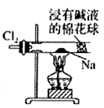
 B . 鉴别纯碱与小苏打
B . 鉴别纯碱与小苏打  C . 证明Cl2能与烧碱溶液反应
C . 证明Cl2能与烧碱溶液反应  D . 探究钠与Cl2反应
D . 探究钠与Cl2反应 
科学家制得一种新型分子O4。关于O4和O2的说法错误的是( )
A . 互为同素异形体
B . 等质量的O4和O2所含原子数相同
C . 它们的摩尔质量相同
D . 等物质的量的O4和O2所含原子数之比为2:1
为确定某纯净的气体X的成分,进行了如下几种实验,其中错误的是( )
| 选项 | 操作(现象) | 结论 |
| A | 闻X气味(有刺激性) | X一定是SO2 |
| B | 闻X气味(有刺激性) | X一定是SO2 |
| C | X | X一定是SO2 |
| D | X | X一定不是SO2 |
A . A
B . B
C . C
D . D
国产航母山东舰已经列装服役,它是采用模块制造然后焊接组装而成的,对焊接有着极高的要求。实验室模拟在海水环境和河水环境下对焊接金属材料使用的影响(如图)。下列相关描述中正确的是( )
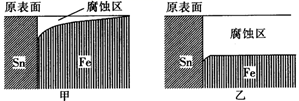
A . 由图示的金属腐蚀情况说明了Sn元素的金属性强于Fe元素
B . 由图示可以看出甲是海水环境下的腐蚀情况,乙是河水环境下的腐蚀情况
C . 两种环境下铁被腐蚀时的电极反应式均为Fe-3e-=Fe3+
D . 为了防止舰艇在海水中被腐蚀,可在焊点附近用锌块打“补丁”
“海带提碘”中,下列关于装置和操作的说法正确的是( )
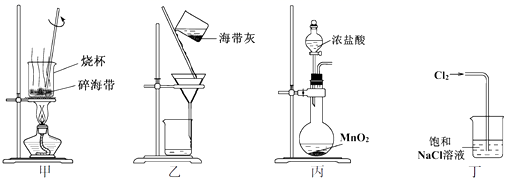
A . 用装置甲灼烧碎海带
B . 用装置乙过滤海带灰的浸泡液
C . 用装置丙制备Cl2 , 用于氧化浸泡液中I-
D . 用装置丁吸收尾气中的Cl2
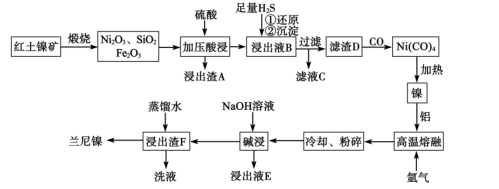
兰尼镍是一种带有多孔结构的细小晶粒组成的镍铝合金,具有优良的储氢性能。以红土镍矿(主要成分为NiS、FeS和SiO2等)为原料制备兰尼镍的工艺流程如图:
-
(1) 形成Ni(CO)4时碳元素的化合价没有变化,则Ni(CO)4中的Ni的化合价为,Ni(CO)4含有的化学键类型。
-
(2) Ni2O3有强氧化性,加压酸浸时,有气体产生且镍被还原为Ni2+ , 则产生的气体为(填化学式)。
-
(3) 滤渣D为单质镍、硫的混合物,请写出向浸出液B中通入H2S气体生成单质镍的离子方程式:。
-
(4) “高温熔融”时通入氩气的目的是。
-
(5) 检验滤液C中金属阳离子的试剂是(填标号)。
a.KSCN溶液 b.K3[Fe(CN)6] c.酸性高锰酸钾 d.苯酚
-
(6) 碱浸的目的是使镍铝合金产生多孔结构,其原理(用化学方程式表示)。
下列说法错误的是( )
A . 误吸入氯气、氯化氢气体时,可吸入少量酒精或乙醚的混合蒸气解毒
B . 焰色反应实验可用细铁丝代替铂丝
C . 为保持滴定的精确,滴定过程中严禁滴定管的尖嘴接触锥形瓶内壁
D . 将两块未擦去氧化膜的铝片分别投入到1mol·L-1CuSO4溶液和1mol·L-1CuCl2溶液中,一段时间后,在CuCl2溶液中铝片表面能观察到明显的反应现象
下列关于金属钠的叙述中,正确的是( )
A . 钠与氯化铁溶液反应时,钠浮在水面上四处游动,并置换出金属铁
B . 钠着火时用干燥的沙土灭火
C . 钠在空气中受热时,熔化成银白色小球,产生黄色火花,生产白色粉末
D . 钠在空气中长期放置,最终主要产物为过氧化钠
下列反应的离子方程式书写正确的是( )
A . 钠和冷水反应:Na+2H2O=Na++2OH-+H2↑
B . 铁和稀盐酸反应:Fe+2H+=Fe3++H2↑
C . NH4HCO3溶液和足量NaOH溶液混合:  +OH-=
+OH-=  +H2O
D . 金属铝溶于盐酸:2Al+6H+=2Al3++3H2↑
+H2O
D . 金属铝溶于盐酸:2Al+6H+=2Al3++3H2↑
 +OH-=
+OH-=  +H2O
D . 金属铝溶于盐酸:2Al+6H+=2Al3++3H2↑
+H2O
D . 金属铝溶于盐酸:2Al+6H+=2Al3++3H2↑
下列关于金属钠的叙述错误的是( )
A . 金属钠可以保存在煤油中
B . 钠元素只能以化合态形式存在于自然界中
C . 实验室取用金属钠可直接用手拿
D . 钠元素在自然界中主要以NaCl的形式存在
国际化学年的中国宣传口号是“化学……我们的生活,我们的未来”。学习化学应该明白“从生活中来,到生活中去”道理。请填空:
-
(1) 若金属钠等活泼金属着火时,应该用来灭火。金属钠应保存在中。
-
(2) 金属钠在空气中燃烧生成色的固体,其生成物与水反应的化学方程式:。
-
(3) NaHCO3固体中混有少量Na2CO3固体,除杂方法是,化学方程式是。
学习元素化合物时可以借助“价类二维图”预测物质性质。如下部分含硫化合物的二维图的相关信息。

-
(1) 图中“X”代表的物质类别是;
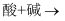 ;Y转化为X体现了Y的性。
;Y转化为X体现了Y的性。
-
(2)
 是重要的大气污染物,会导致“酸雨”。
是重要的大气污染物,会导致“酸雨”。 产生硫酸型酸雨有两条途径:途径一是
产生硫酸型酸雨有两条途径:途径一是
 ;另一途径是:
;另一途径是: 。
。
-
(3) 将装有
 的试管倒立在水槽中,可观察到。取出试管中的溶液,分别进行如下实验:
的试管倒立在水槽中,可观察到。取出试管中的溶液,分别进行如下实验:
①滴加品红溶液振荡,观察到红色褪去,说明
 具有性。
具有性。②滴加
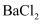 溶液,无明显现象,再滴入
溶液,无明显现象,再滴入 溶液后出现白色沉淀。出现白色沉淀的原因是。
溶液后出现白色沉淀。出现白色沉淀的原因是。 -
(4) 根据
 的性质提出一种燃煤脱硫的方法。
的性质提出一种燃煤脱硫的方法。
海水中不仅含有丰富的水资源,而且蕴藏着宝贵的化学资源。海水资源利用的部分过程如图。下列有关说法错误的是( )
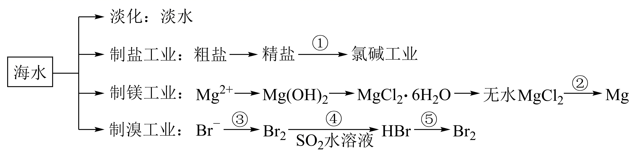
A . 海水淡化的方法主要有蒸馏法、电渗析法和离子交换法等
B . 在氯碱工业中,电解饱和食盐水可获得金属钠
C . 在制镁工业中,常用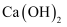 做沉淀剂
D . 在制溴工业中,步骤分别为氧化、还原、氧化
做沉淀剂
D . 在制溴工业中,步骤分别为氧化、还原、氧化
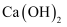 做沉淀剂
D . 在制溴工业中,步骤分别为氧化、还原、氧化
做沉淀剂
D . 在制溴工业中,步骤分别为氧化、还原、氧化
将12.8 g Cu投入50 mL某浓度的浓HNO3中,随着Cu的不断减少,反应生成气体的颜色逐渐变浅,当Cu全部溶解时,硝酸恰好完全消耗,共收集到NO2和NO气体3.36 L(标准状况)。回答下列问题:
-
(1) 写出生成NO的离子方程式;
-
(2) 混合气体中NO和NO2的体积比为;
-
(3) 将生成的气体收集在大试管中,然后倒扣在水中,若往试管中通入氧气让液体充满试管,则通入氧气的质量为;
-
(4) 原硝酸的物质的量浓度为。
下列实验方案中,不能测定出 和
和 的混合物中
的混合物中 质量分数的是( )
质量分数的是( )
 和
和 的混合物中
的混合物中 质量分数的是( )
质量分数的是( )
A . 取ag混合物充分加热,剩余固体质量为bg
B . 取ag混合物与足量 溶液充分反应,得到bg溶液
C . 取ag混合物与足量稀盐酸反应,加热、蒸干、灼烧,得到bg固体
D . 取ag混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,质量增加bg
溶液充分反应,得到bg溶液
C . 取ag混合物与足量稀盐酸反应,加热、蒸干、灼烧,得到bg固体
D . 取ag混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,质量增加bg
 溶液充分反应,得到bg溶液
C . 取ag混合物与足量稀盐酸反应,加热、蒸干、灼烧,得到bg固体
D . 取ag混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,质量增加bg
溶液充分反应,得到bg溶液
C . 取ag混合物与足量稀盐酸反应,加热、蒸干、灼烧,得到bg固体
D . 取ag混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,质量增加bg
工业上生产硫酸时,其中SO2与O2反应生成SO3的热化学方程式为2SO2(g)+O2(g)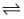 2SO3(g) ΔH=-196.6 kJ·mol-1。在生产过程中,充分利用反应放出的热量对SO2和O2进行加热,并将尾气进行循环利用。下列有关SO2的说法正确的是( )
2SO3(g) ΔH=-196.6 kJ·mol-1。在生产过程中,充分利用反应放出的热量对SO2和O2进行加热,并将尾气进行循环利用。下列有关SO2的说法正确的是( )
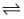 2SO3(g) ΔH=-196.6 kJ·mol-1。在生产过程中,充分利用反应放出的热量对SO2和O2进行加热,并将尾气进行循环利用。下列有关SO2的说法正确的是( )
2SO3(g) ΔH=-196.6 kJ·mol-1。在生产过程中,充分利用反应放出的热量对SO2和O2进行加热,并将尾气进行循环利用。下列有关SO2的说法正确的是( )
A . SO2与H2S反应有淡黄色固体生成,体现了SO2的氧化性
B . SO2使溴水褪色利用了SO2的漂白性
C . 将SO2通入Ba(NO3)2溶液中不可能产生白色沉淀
D . SO2分子的空间构型为直线形
下列不属于海水淡化的方法是( )
A . 蒸馏法
B . 电渗析法
C . 石灰纯碱法
D . 离子交换法
最近更新
- 国务院也决定10月9日起对储蓄存款利息所得暂免征收个人所得税。这是中国货币当局充分考量国际、国内经济金融形势之后作出的有
- 两个点电荷Q1、Q2固定于x轴上,将一带正电的试探电荷从足够远处沿x轴负方向移近Q2(位于坐标原点)的过程中,试探电荷的
- Withtime changing so fast, to keep _____ with time, anyone s
- 据报道,近年北京市食品垃圾呈现上升趋势,竟然占垃圾总量的17%左右,以至于市环卫局垃圾分选站在回收类别中专门增加了“馒头
- 根据右图回答问题: ⑴图中所示的内容在生命系统的结构层次中对应于 。 ⑵一只
- 实物资料是一种历史证据。二战中,日本侵略者对人类犯下了不可饶恕的罪行。下列可用来证明日军所犯罪行的史料包括( ) ①
- (1); (2)
- 20世纪50-70年代日本经济持续高速发展,成为仅次于美国的世界第二号资本主义经济大国。下列哪一项不是日本经济发展的原因
- 2008年世界上最重要的两个国家美国和俄罗斯进行总统大选,此外巴基斯坦议会、我国全国人大、台湾地方选举也将举行,上述选举
- 图中MN表示真空室中垂直于纸面的平板,它的一侧有匀强磁场,磁场方向垂直于纸面向里,磁感应强度大小为B.一带电粒子从平板上
- “空气中氧气含量的测定”有多种方法。甲生设计了如图所示的实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡
- a=3是直线ax+2y+3a=0和直线3x+(a-1)y=a-7平行且不重合的__________.
- 如下图,一个质量为m的圆环套在一根固定的、足够长的粗糙水平直杆上,现给环一个向右的初速度v0,如果在运动过程中圆环还受到
- The Beatles,________ many of you are old enough to remember,
- 在bLFeBr2溶液中通入amolCl2时,使溶液中50%的Br-氧化为Br2,则原FeBr2的物质的量浓度为(
- 下列物质性质与应用的因果关系正确的是() A.焦炭具有强还原性,高温下能将二氧化硅还原为硅 B.晶体硅用于制作半导体材料
- 请按要求完成下列反应的式子。 (1)银锌纽扣电池(总反应:Ag2O+Zn= 2Ag+ZnO,电解质溶液:氢氧化钾)的正极
- 读中国某地区局部图,完成图中河流P的补给主要来自
- 函数f(x)=-x4+2x2+3的最大值为 .
- “雪碧”是一种无色的碳酸饮料,将少量“雪碧”滴入紫色石蕊试液中,然后再加热, 溶液的颜色变化情况是 ( ) A.
 酸性KMnO4溶液(褪色)
酸性KMnO4溶液(褪色) 变红色
变红色


