常见无机物及其应用 知识点题库
 )轰击金属原子
)轰击金属原子 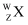 ,得到核素
,得到核素  ,开创了人造放射性核素的先河:
,开创了人造放射性核素的先河: 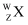 +
+  →
→  +
+  。其中元素X、Y的最外层电子数之和为8。下列叙述正确的是( )
。其中元素X、Y的最外层电子数之和为8。下列叙述正确的是( )
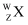 的相对原子质量为26
B . X、Y均可形成三氯化物
C . X的原子半径小于Y的
D . Y仅有一种含氧酸
的相对原子质量为26
B . X、Y均可形成三氯化物
C . X的原子半径小于Y的
D . Y仅有一种含氧酸

 B .
B .  C .
C . 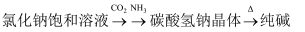 D .
D . 
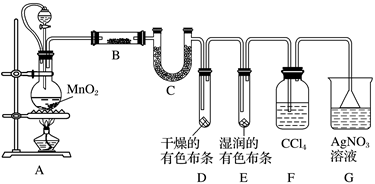
请回答下列问题:
-
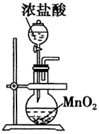
(1) 装置A中连接橡皮管的目的是。
-
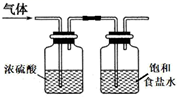
(2) 装置A中发生反应的离子方程式为。装置B中盛放的试剂是。
-
(3) 有同学基于实验的严谨性考虑,认为可在F、G两个装置之间再加一个装有湿润的淀粉KI试纸的装置,其目的是。
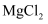 能导电,所以
能导电,所以 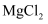 是电解质
是电解质
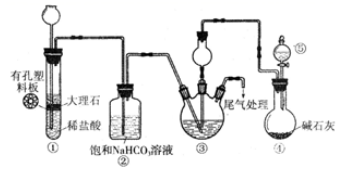
 制取氯气并探究氯气性质,设计了如图所示的实验装置:
制取氯气并探究氯气性质,设计了如图所示的实验装置: 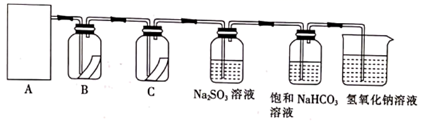
-
(1) 从装置I、Ⅱ、Ⅲ中选择合适的制氯气的装置( A处):( 填标号)。
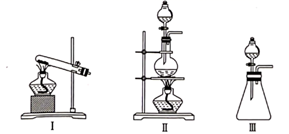
-
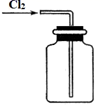
(2) 装置B、C中依次放的是干燥的红色布条和湿润的红色布条实验过程中该同学发现装置B中的布条也褪色,其原因可能是;说明该装置存在明显的缺陷,请提出合理的改进方法。
-
(3) 验证氯气的氧化性:将氯气通入
 溶液中,氯气可将
溶液中,氯气可将  氧化成
氧化成  。写出该反应的化学方程式:。
。写出该反应的化学方程式:。
-
(4) 氯气通入饱和
 溶液中能产生无色气体已知酸性:盐酸>碳酸>次氯酸。( 强酸可以制弱酸)该实验证明氯气与水反应的生成物中含有( 填“盐酸”或“次氯酸”)。
溶液中能产生无色气体已知酸性:盐酸>碳酸>次氯酸。( 强酸可以制弱酸)该实验证明氯气与水反应的生成物中含有( 填“盐酸”或“次氯酸”)。
-
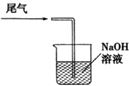
(5) 实验装置中烧杯内氢氧化钠溶液的作用是。
-
(1) 检验某次降雨是否为酸雨的方法是
-
(2) SO2是造成酸雨的主要原因。写出一条减少SO2排放的措施。
-
(3) 某酸雨样品的pH=5,则该样品中c(H+)=mol/L。该样品放置一段时间后,酸雨略有增大,其原因可能是(用化学方程式表示)。
A.O2和O3
B.  C和
C和  C
C
C.CH3CH2CH2CH3 和CH3CH(CH3)CH3
D. ![]() 和
和 ![]()
E. 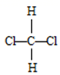 和
和 ![]()
-
(1) 组两物质互为同位素;
-
(2) 组两物质属于同系物;
-
(3) 组两物质互为同素异形体;
-
(4) 组两物质互为同分异构体;
-
(5) 组两物质是同一物质。
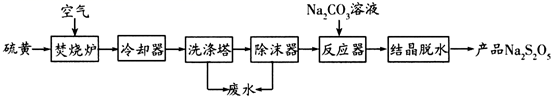
已知:结晶脱水发生的反应: 
回答下列问题:
-
(1) Na2S2O5中硫元素的化合价为。
-
(2) 焚烧炉中反应的化学方程式为。
-
(3) 反应器中发生反应的离子方程式为。
-
(4) 葡萄酒酿造过程中添加Na2S2O5会放出一种有刺激性气味的气体,该气体是一种食品添加剂。实验室中检验该气体的常用试剂是。
-
(5) 废水中的硫单质(S8)能与碱反应,化学反应:
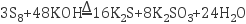 ,反应中氧化剂与还原剂的物质的量之比为。
,反应中氧化剂与还原剂的物质的量之比为。
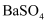 可用作医疗上检查肠胃的钡餐,还可用作白色颜料
C . 光照下,
可用作医疗上检查肠胃的钡餐,还可用作白色颜料
C . 光照下,  在空气中与碳氢化合物发生作用,可产生光化学烟雾
D . 铁的化合物应用广泛,
在空气中与碳氢化合物发生作用,可产生光化学烟雾
D . 铁的化合物应用广泛, 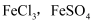 常用作净水剂
常用作净水剂
| 目的 | 方案设计 | 现象和结论 | |
| A | 检验某无色溶液中是否含有NH | 取少量该溶液于试管中,加足量NaOH溶液,加热后将湿润蓝色石蕊试纸置于试管口 | 若试纸变红,则该溶液中含有NH |
| B | 探究维生素C的还原性 | 向盛有2mL0.1mol•L-1黄色氯化铁溶液的试管中滴加2mL2mol•L-1的维生素C溶液 | 若溶液颜色变为浅绿色,说明维生素C具有还原性 |
| C | 判断某卤代烃中的卤素 | 取2mL卤代烃样品于试管中加入5mL20%KOH水溶液混合后加热,再滴加AgNO3溶液 | 若产生的沉淀为白色,则该卤代烃中含有氯元素 |
| D | 验证麦芽糖是否发生水解 | 取2mL20%的麦芽糖溶液于试管中,加入适量稀H2SO4后水浴加热5min,冷却后先加足量NaOH溶液再加入适量新制Cu(OH)2悬浊液并加热 | 若生成砖红色沉淀,则麦芽糖已水解 |
 性质和含量测定的探究活动。
性质和含量测定的探究活动。 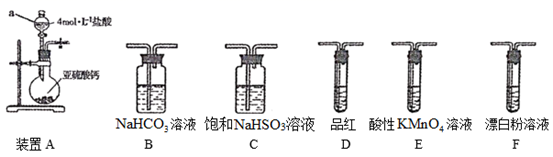
-
(1) 装置A中仪器
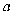 的名称为。写出
的名称为。写出  中
中 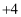 价的硫元素体现氧化性的化学反应(用化学方程式表示)。
价的硫元素体现氧化性的化学反应(用化学方程式表示)。
-
(2) 选用上图中的装置和药品探究亚硫酸与次氯酸的酸性强弱:
①甲同学认为按照
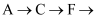 尾气处理顺序连接装置可以证明亚硫酸和次氯酸的酸性强弱,乙同学认为该方案不合理其理由是。
尾气处理顺序连接装置可以证明亚硫酸和次氯酸的酸性强弱,乙同学认为该方案不合理其理由是。②丙同学设计的合理实验方案为:按照
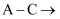
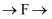 尾气处理(填字母)顺序连接装置。可以证明亚硫酸的酸性强于次氯酸的酸性的实验现象是。
尾气处理(填字母)顺序连接装置。可以证明亚硫酸的酸性强于次氯酸的酸性的实验现象是。③其中装置C的作用是。常温下,测得装置C中饱和
 溶液的
溶液的 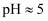 ,则该溶液中所有离子浓度由大到小的顺序为。(已知
,则该溶液中所有离子浓度由大到小的顺序为。(已知 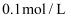 的
的 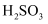 溶液
溶液 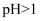 )
) -
(3) 测定某葡萄酒中抗氧化剂的残留量(以游离
 计算)的方案如下:
计算)的方案如下: 
(已知:滴定时反应的化学方程式为
 )
)①按上述方案实验,消耗标准
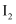 溶液
溶液 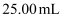 ,该次实验测得样品中抗氧化剂的残留量(以游离
,该次实验测得样品中抗氧化剂的残留量(以游离  计算)为
计算)为 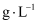 。
。②在上述实验过程中,若有部分
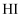 被空气氧化,则测得结果(填“偏高”、“偏低”或“不变”)。
被空气氧化,则测得结果(填“偏高”、“偏低”或“不变”)。
| A | B | C | D |
| | | | |
| 制备Cl2 | 净化Cl2 | 收集Cl2 | 尾气处理 |
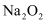 与足量的
与足量的 或
或 反应,转移的电子数目都为2NA
B . 常温下,27 g Al与足量的氢氧化钠溶液反应,转移的电子数目为3NA
C . 标准状况下,22.4 L
反应,转移的电子数目都为2NA
B . 常温下,27 g Al与足量的氢氧化钠溶液反应,转移的电子数目为3NA
C . 标准状况下,22.4 L  中含有的分子数目为NA
D . 物质的量浓度为0.5mol/L的
中含有的分子数目为NA
D . 物质的量浓度为0.5mol/L的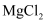 溶液中,含有
溶液中,含有 的个数为NA
的个数为NA
①准确量取5.00 mL血液样品,处理后配制成50.00
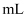 溶液;
溶液;
②准确量取溶液20.00 mL,加入过量
 溶液,使Ca2+完全转化成
溶液,使Ca2+完全转化成
 沉淀;
沉淀;
③过滤并洗净所得
 沉淀,用过量稀硫酸溶解,生成
沉淀,用过量稀硫酸溶解,生成
 和
和
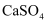 稀溶液;
稀溶液;
④加入
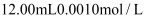 的酸性KMnO4溶液,使H2C2O4完全被氧化。
的酸性KMnO4溶液,使H2C2O4完全被氧化。
⑤用
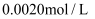 (NH4)2Fe(SO4)2溶液滴定过量的酸性KMnO4溶液。
(NH4)2Fe(SO4)2溶液滴定过量的酸性KMnO4溶液。
回答下列问题:
-
(1) 常温下
 , 欲使步骤②中Ca2+完全沉淀(
, 欲使步骤②中Ca2+完全沉淀(
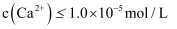 ),应保持溶液中
),应保持溶液中
 ≥mol/L。
≥mol/L。
-
(2) (NH4)2Fe(SO4)2中Fe元素基态原子的价层电子排布式为。
-
(3)
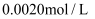 (NH4)2Fe(SO4)2溶液应装在滴定管中(填写“酸式”或“碱式”),该溶液中所有离子浓度大小顺序为。
(NH4)2Fe(SO4)2溶液应装在滴定管中(填写“酸式”或“碱式”),该溶液中所有离子浓度大小顺序为。
-
(4) 步骤⑤,滴定的过程中有以下实验操作:
a.向溶液中加入1~2滴指示剂
b.取待测的KMnO4溶液放入锥形瓶中
c.用蒸馏水洗净锥形瓶
d.用少量KMnO4溶液润洗锥形瓶
e.用(NH4)2Fe(SO4)2溶液滴定
f.重复以上操作
g.眼睛观察锥形瓶中溶液颜色的变化,至滴定终点
h.根据实验数据计算KMnO4溶液的物质的量
正确的操作顺序是(填序号)。
-
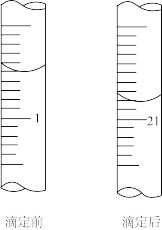
(5) 滴定过程中,滴定前后体积如图所示,则消耗(NH4)2Fe(SO4)2溶液的体积为mL。
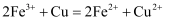 B . 二氧化硫与硝酸钡溶液反应的离子方程式:
B . 二氧化硫与硝酸钡溶液反应的离子方程式: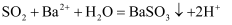 C . 二氧化硅与氢氧化钠溶液反应的离子方程式:
C . 二氧化硅与氢氧化钠溶液反应的离子方程式: D . 甲烷与氯气在光照条件下生成一氯甲烷的化学方程式:
D . 甲烷与氯气在光照条件下生成一氯甲烷的化学方程式: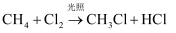
- 下列叙述正确的是 ( ) A.同温同压下,两种气体的体积之比等于摩尔质量之比B.同温同
- The Great Wall is famous all over the world.And visit
- 总书记在中共十七大中强调要“推进文化创新,增强文化发展活力”。之所以重视文化创新,是因为它( )①可以推动社会实践的
- 下图是某县参加2011年高考的学生身高条形统计图,从左到右的各条形图表示学生人数依次记为A1、A2、…A10(如A2表示
- 公民大会是雅典重要权力机关,所有合法的公民均有参与权、知情权、发言权、选举权和被选举权。但是“任何殴打父母的人,任何不赡
- 函数在点处的切线方程是( ) A. B. C. D.
- 下列关于生态系统物质循环的叙述中,错误的是() A. 物质循环指的是构成生物体的各种化合物在生物群落和无机
- 如果a、b同号,那么二次函数y=ax2+bx+1的大致图象是() A. B. C. D.
- (10分)(1)①根据图示,写出反应的热化学方程式: 。②根据如图所示情况,
- 因式分解: (x-1)(x-3)+1
- 设f′(x)是函数f(x)的导函数,y=f′(x)的图象如图所示,则y=f(x)的图象最有可能是( )
- 依次填入横线上的关联词,最恰当的一项是 ( ) 在信息处理这个环节上, 光计算有很大的潜力, 光
- 如图,已知a∥b,∠1=40°,则∠2=() A. 140° B. 120° C. 40° D. 50°
- 2012年5月份,鸡西地区一周空气质量报告中某项污染指数的数据是:31,35,30,31,34,32,31,这组数据的中
- 民族问题和宗教问题是当今世界最重要的国际问题之一。公元前6世纪,在印度兴起了佛教。相传佛教的创始人是 A.乔达摩·悉达多
- 对于放热反应,下列说法中正确的是 A.产物H2O所具有的总能量高于反应物H2和
- 在“用天平称物体质量”的实验中,用已调节好的天平在称物体质量时,通过增、减砝码后指针偏在分度盘中线左边一点,这时应该:A
- 在某次体育测试中,九年级(2)班6位同学的立定跳远成绩(单位:米)分别是:1.83,1.85,1.96,2.08,1.8
- 下列图片中能反映我国积极参与地区性国际组织的外交活动有 A.①②③④ B.②④ C.①②③
- I like her _____ she can be annoying(令人烦恼的).A.even if