化学研究方法与工业化学 知识点题库
乙苯催化脱氢制苯乙烯反应: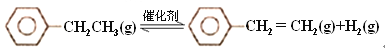
-
(1) 已知:
化学键
C-H
C-C
C=C
H-H
键能/kJ/mol
412
348
612
436
计算上述反应的△H= kJ·mol-1。
-
(2) 维持体系总压强p恒定,在温度T时,物质的量为n、体积为V的乙苯蒸汽发生催化脱氢反应。已知乙苯的平衡转化率为α,则在该温度下反应的平衡常数K= (用α等符号表示)。
-
(3)
工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1︰9),控制反应温度600℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)示意图如下:
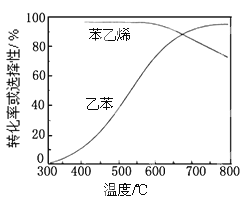
①掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实 。
②控制反应温度为600℃的理由是 。
-
(4) 某研究机构用CO2代替水蒸气开发了绿色化学合成工艺——乙苯-二氧化碳耦合催化脱氢制苯乙烯。保持常压和原料气比例不变,与掺水蒸汽工艺相比,在相同的生产效率下,可降低操作温度;该工艺中还能够发生反应:CO2+H2=CO+H2O,CO2+C=2CO。新工艺的特点有 (填编号)。
① CO2与H2反应,使乙苯脱氢反应的化学平衡右移
② 不用高温水蒸气,可降低能量消耗
③ 有利于减少积炭
④ 有利于CO2资源利用
-
(1) 硝酸铵的生产方法是采用硝酸与氨气化合,工业合成氨是一个放热反应,因此低温有利于提高原料的转化率,但实际生产中却采用400~500℃的高温,其原因是 ;工业生产中,以氨气为原料合成硝酸,写出工业生产硝酸的最后一步的化学方程式
-
(2)
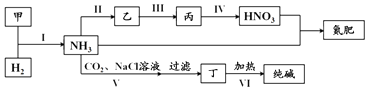
甲、乙、丙三个化肥厂生产尿素所用的原料不同,但生产流程相同(如图3所示):
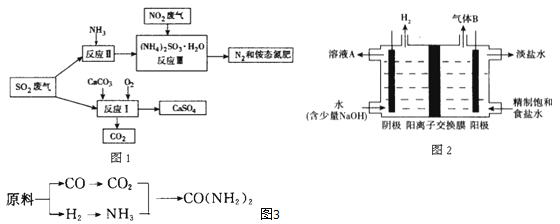
已知:CO+H2O
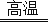 CO2+H2
CO2+H2①甲厂以焦炭和水为原料;
②乙厂以天然气和水为原料;
③丙厂以石脑油(主要成分为C5H12)和水为原料.
按工业有关规定,利用原料所制得的原料气H2和CO2的物质的量之比,若最接近合成尿素的原料气NH3(换算成H2的物质的量)和CO2的物质的量之比,则对原料的利用率最高.据此判断甲、乙、丙三个工厂哪个工厂对原料的利用率最高?
-
(3) 将工厂废气中产生的SO2通过下列流程如图1,可以转化为有应用价值的硫酸钙等.
①写出反应Ⅰ的化学方程式: .
②生产中,向反应Ⅱ的溶液中加入强还原性的对苯二酚等物质,目的是
③检验经过反应Ⅲ得到的氨态氮肥中SO42﹣所用试剂是
-
(4) 工业上利用氯碱工业产品治理含二氧化硫的废气.图2是氯碱工业中电解饱和食盐水的原理示意图.
①用溶液A吸收含二氧化硫的废气,其反应的离子方程式是
②用含气体B的阳极区溶液吸收含二氧化硫的废气,其反应的离子方程式是
-
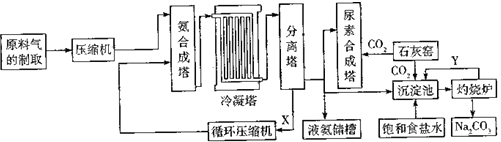
(1) 原料气进入压缩机前需要进行净化处理,其目的是.制备氨合成塔的材料(填“能”或“不能”)使用普通的碳素钢.
-
(2) N2、H2混合气体经压缩后再送入氨合成塔,优点是. 某整个生产中循环使用某些原料可提高生产效益,能循环利用的物质是.
-
(3) 请按要求填写下列空白.
①沉淀池中的离子方程式:.
②生产尿素的化学方程式:.
-
(4) 在较低温度下,可从沉淀池的溶液中分离出一种副产品由此可推断,低温下NH4Cl的溶解度很可能(填“小于”或“大于”)NaCL.NH4Cl是一种氮肥,但长期施用易使土壤酸化,用离子方程式表示其原因.
-
(5) 以焦炭、水为原料制备H2 (碳转化为CO2 , 则1000g纯度为a%((杂质不与水反应)焦炭最多可制备 g尿素(已知合成氨时h2的利用率为b%、合成尿素时NH3的利用率为c%)
完成下列填空:
-
(1) 写出上述制备小苏打的化学方程式;
-
(2) 滤出小苏打后,母液提取氯化铵有两种方法:
①通入氨,冷却、加食盐,过滤
②不通氨,冷却、加食盐,过滤
对两种方法的评价正确的是(选填编号)
a.①析出的氯化铵纯度更高 b.②析出的氯化铵纯度更高
c.①的滤液可直接循环使用 d.②的滤液可直接循环使用
-
(3) 提取的NH4Cl中含少量Fe2+、SO42﹣ . 将产品溶解,加入H2O2 , 加热至沸,再加入BaCl2溶液,过滤,蒸发结晶,得到工业氯化铵.
加热至沸的目的是.滤渣的主要成分是、.
-
(4) 称取1.840g小苏打样品(含少量NaCl),配成250ml溶液,取出25.00ml用0.1000mol/L盐酸滴定,消耗盐酸21.50ml.实验中所需的定量仪器除电子天平外,还有.样品中NaHCO3的质量分数为.(保留1位小数)
-
(5) 将一定质量小苏打样品(含少量NaCl)溶于足量盐酸,蒸干后称量固体质量,也可测定小苏打的含量.若蒸发过程中有少量液体溅出,则测定结果.(选填“偏高”、“偏低”或“无影响”)

-
(1) 铝粉和铁的氧化物(FeO-Fe2O3)可配成铝热剂用于焊接钢轨,反应的化学方程式是。
-
(2) 以铝土矿(主要成分为Al2O3.含SiO2和Fe2O3等杂质)为原料生产铝和铵明矾晶体[NH4Al(SO4)2·12H2O]的一种工艺流程如下(已知:SiO2在“碱溶”时转化为铝硅酸钠(NaAlSiO4·nH2O)沉淀)。
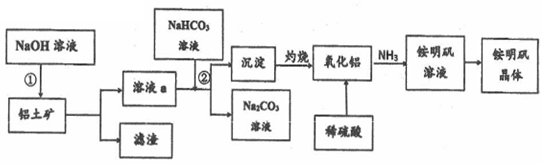
①实验前,要将铝土矿粉粹的目的是。
②用氧化物的形式表示铝硅酸钠的化学式。
③步骤②涉及到的离子方程式是: 。
④写出利用Al2O3制备金属Al的化学方程式: 。
⑤若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的物质的量之比为1 : 1,则投料时铝土矿中的Al2O3和H2SO4的物质的量之比为。
-
(1) 铝粉和铁的氧化物(FeO·Fe2O3)可配成铝热剂用于焊接钢轨,反应的化学方程式是。
-
(2) NaOH溶液可以除去铝表面的氧化膜,在处理过程中常会产生H2 , 产生H2的离子方程式是。
-
(3) 工业上以铝土矿(Al2O3·H2O)为原料生产铝,主要包括下列过程:
i.将粉粹、筛选后的铝土矿溶解在NaOH溶液中;
ii.加入过量的试剂A使所得溶液中析出Al(OH)3固体;
iii.使Al(OH)3脱水生成Al2O3;
iv.电解熔融Al2O3生成Al。
铝土矿粉粹的目的是,电解熔融Al2O3时,加入冰晶石,其作用是。写出电解熔融Al2O3的化学方程式。
-
(4) 明矾化学式为KAl(SO4)2·12H2O,向明矾溶液中加入Ba(OH)2溶液,当溶液中的SO42-恰好沉淀时,铝元素的存在形式是。
| 选项 | 实验 | 现象 | 结论 |
| A | 将镁条点燃后迅速伸入充满N2的集气瓶中 | 集气瓶内有黄绿色粉末产生 | N2具有氧化性 |
| B | 向2mLNa2S稀溶液中滴加0.1mol/LZnSO4溶液至不再有白色沉淀产生,然后再往上述溶液中滴加0.1mol/LCuSO4溶液 | 沉淀由白色变为黑色 | Ksp(ZnS)>Ksp(CuS) |
| C | 将镁片和铝片分别打磨后,用导线连接再插入NaOH溶液中 | 片刻后镁片上有大量气泡产生,铝片上产生的气泡很少 | 镁为电池正极 |
| D | 将装有CuCl2∙2H2O晶体的试管加热,在试管口放置湿润的蓝色石蕊试纸 | 试纸变为红色 | CuCl2显酸性 |
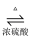 C17H35COOC2H5+H218O
B . 常温时,0.1 mol·L-1氨水的pH=11.1:NH3·H2O
C17H35COOC2H5+H218O
B . 常温时,0.1 mol·L-1氨水的pH=11.1:NH3·H2O  NH4++OH−
C . 由Na和Cl形成离子键的过程:
NH4++OH−
C . 由Na和Cl形成离子键的过程:  2NH3。起始时投入氮气和氢气的物质的量分别为1mol、3mol,在不同温度和压强下合成氨。平衡时混合物中氨的体积分数与温度的关系如图。
2NH3。起始时投入氮气和氢气的物质的量分别为1mol、3mol,在不同温度和压强下合成氨。平衡时混合物中氨的体积分数与温度的关系如图。 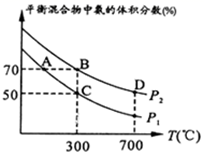
①恒压时,反应一定达到平衡状态的标志是(填序号)
A.N2和H2的转化率相等 B.反应体系密度保持不变
C.  保持不变 D.
保持不变 D. 
②该反应的平衡常数表达式K=,∆H。
③比较大小:P1P2 , 理由是
④平衡时B、D两点的正反应速率:υ(B)υ(D)。(填“<”或“>”或“=”)
-
(1) 实验一:电解饱和食盐水
实验约需40mL饱和食盐水,配置450mL饱和食盐水所需的玻璃仪器有:烧杯、_____。
A . 450mL容量瓶 B . 500mL容量瓶 C . 电子天平 D . 玻璃棒 E . 量筒 F . 胶头滴管 -
(2) 电解饱和食盐水的化学方程式为。
-
(3) Y电极附近产物的检验方法:。
-
(4) 实验二:电解不饱和食盐水及产物分析。相同条件下,电解1mol/L NaCl溶液并收集两极产生的气体。在X处收集到V1 mL气体。同时,在Y处收集到V2 mL气体,停止电解。结果发现V2<V1 , 且与电解饱和食盐水相比,Y处收集到的气体颜色明显较浅。经讨论分析,导致上述现象的原因有:
i.有部分Cl2溶于NaCl溶液中;
ii.有O2生成。
设计实验证明有部分Cl2溶于NaCl溶液中,实验方案为。
-
(5) 证明有O2生成并测定O2的体积。按如图所示装置进行实验,通过注射器缓缓地将在Y处收集到V2 mL气体全部推入装置A(盛有足量试剂NaOH溶液)中,最终,量气管中收集到V3 mL气体(设V1、V2、V3均在相同条件下测得)。
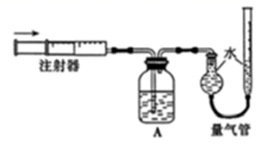
①装置A的作用是。
②本实验中,观察到的现象,说明石墨电极上有O2生成。
③实验中是否需要预先除尽装置中的空气?(填“是”或“否”)。
④实验二中,在石墨电极上产生的Cl2的总体积为mL(用代数式表示)。
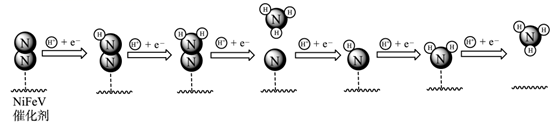
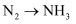 ,
,  均属于氮的固定
B . 硝酸应保存在棕色、细口、带玻璃塞的试剂瓶中
C .
均属于氮的固定
B . 硝酸应保存在棕色、细口、带玻璃塞的试剂瓶中
C .  很稳定,不支持任何物质的燃烧
D . 所有的铵盐受热分解都会产生
很稳定,不支持任何物质的燃烧
D . 所有的铵盐受热分解都会产生 
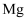 在
在 中燃烧生成
中燃烧生成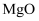 和C,则
和C,则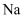 在
在 中燃烧可能生成
中燃烧可能生成 和C
B .
和C
B . 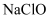 溶液与
溶液与 反应生成
反应生成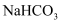 和
和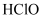 , 则
, 则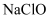 溶液与
溶液与 反应生成
反应生成 和
和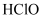 C . C在足量
C . C在足量 中燃烧生成
中燃烧生成 , 则S在足量
, 则S在足量 中燃烧生成
中燃烧生成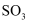 D . 往
D . 往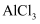 溶液中加入过量氨水生成
溶液中加入过量氨水生成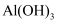 沉淀,则往
沉淀,则往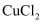 溶液中加入过量氨水生成
溶液中加入过量氨水生成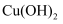 沉淀
沉淀
- 对美国夫妇,将他们精子、卵细胞做的胚胎冷藏在澳大利亚墨尔本一所不孕症治疗中心(防止胚胎移植不能一次成功时,以备下次再用)
- 下列示意图能正确表示H2与Cl2反应生成HCl过程中能量变化的是( )A.A B. B C. C
- 自然界和生活中的下列事例,与氧化还原反应无.关.的是 A.醋的酿造 B.金属生锈 C.动植物呼吸
- Heis seriously ill, so he has problems ________. A. breath
- 对于海洋能的开发利用,叙述正确的是() A.所有海洋能资源的利用技术都已经成熟 B.潮汐能的发电技术还没有进入实用阶段
- 生活中处处有化学。 (1)碘酒是家庭常备药物,碘酒中的溶剂是 。 (2)加了洗涤剂的水能除去衣服上的油
- 短周期的三种元素X、Y、Z,原子序数依次变小,原子核外电子层数之和是5。X元素原子最外电子层上的电子数是Y和Z两元素原子
- 在暗室里,用电灯作为光源,照射地球仪,自西向东拨动地球仪,演示地球自转运动,如下图所示。据此完成9~11题。9.该实验演
- 下列对有关实验事实的解释正确的是 A.向某溶液中滴加氯水后,再加入KSCN溶液,溶液呈红色,说明原溶液中含有Fe2+
- 3.In nature some animals actively defend the area___________
- 7、“如今有个趋势,人们怀念她的民主制度,并将其视为所有现代民主制度的源头”。(英国史学家约翰索利语)这里的“她”是指
- My mother______________ a birthday gift ______________ me ev
- 研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应: 2NO2(g)+NaCl(s)NaNO3(s
- 下图为沿某条经线的我国局部地形剖面示意图,回答图中①②③④地形区发展农业条件及面临的问题,叙述正确的是A.①处水土流失严
- —______ Mary her brother like eating Chinese food.They
- 由水电离产生的c(H+)和c(OH﹣)的乘积为1×10﹣18的溶液里,可能大量共存的离子组()A. NH4+、Na+、C
- 中国的责任首先是对中国人民的责任。今日中国以占世界9%的耕地、6%的水资源、4%的森林、1.8%的石油、0.7%的天然气
- 氨气可以做喷泉实验,这是利用氨气() A.易液化 B.比空气轻 C.极易溶于水 D.能跟水反应
- 20世纪50-60年代,我国开展了“剿灭麻雀”的运动,而现在有关专家发出了要保护麻雀的呼吁,其原因是 A.麻雀对维持生态
- does it take you to finishthe book?A. How long; to readB. Ho



