化学研究方法与工业化学 知识点题库
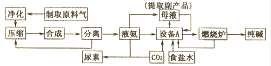
(1)图中制取的原料气体是 .原料气中的一种气体源于碳氢化合物和水.请写出甲烷和水在催化剂和高温条件下反应的方程式: .
(2)工业生产中,设备A中发生的化学反应方程式是 ,母液中可提取的副产品是 .
(3)尿素[CO(NH2)2]适用于各种土壤,在土壤中尿素发生水解,生成两种气体,其水解的化学方程式是 .
(4)纯碱的水溶液可用来洗涤油污,理由是 (结合相关离子方程式解释).
(5)上述流程中,可循环使用的物质是 .
(6)图中所示工业制法获得的纯碱中常含有NaCl杂质,用下述方法可以测定样品NaCl的质量分数.样品W克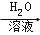 溶液
溶液 沉淀
沉淀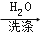
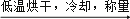 固体m克样品中NaCl质量分数的表达式为 .
固体m克样品中NaCl质量分数的表达式为 .
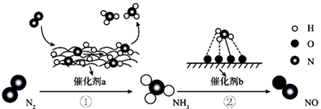
如图是有关氮的循环示意图.
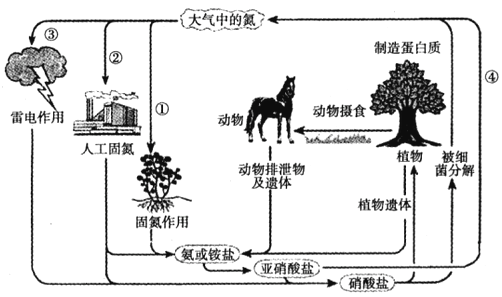
(1)过程①中通过的作用将空气中的氮气固定下来.
(2)请写出②中合成氨反应的化学方程式: .
(3)请写出③中固氮反应的方程式: .
(4)过程④中的亚硝酸盐有毒,工业上若直接排放将造成对环境的污染.已知NaNO2遇到还原性较强的NH4+等被还原为N2 . 在废液中加入下列物质不能使NaNO2无害化排放的是 .
a.H2O2 b.NH4Cl c.KNO3 .
 2NH3
B . 铝:2Al2O3(熔融)
2NH3
B . 铝:2Al2O3(熔融) 4Al+3O2↑
C . 氯气:MnO2+4HCl(浓)
4Al+3O2↑
C . 氯气:MnO2+4HCl(浓)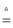 MnCl2+Cl2↑+2H2O
D . 硫酸:2SO2+O2
MnCl2+Cl2↑+2H2O
D . 硫酸:2SO2+O2 2SO3 , SO3+H2O═H2SO4
2SO3 , SO3+H2O═H2SO4
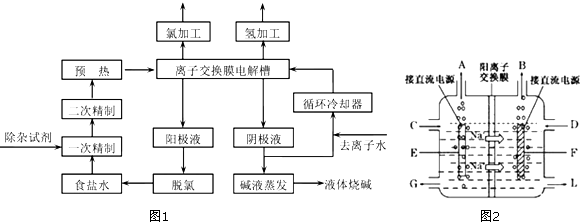
氯碱工业是最基本的化学工业之一,离子膜电解法为目前普遍使用的生产方法,其生产流程如图1所示:
-
(1) 该流程中可以循环的物质是.
-
(2) 电解法制碱的主要原料是饱和食盐水,由于粗盐水中含有Ca2+、Mg2+、SO42﹣等无机杂质,所以在进入电解槽前需要进行两次精制,得到精制饱和食盐水.
①第一次精制过程中所加除杂试剂顺序不合理的是
A.BaCl2、NaOH、Na2CO3、HCl B.BaCl2、Na2CO3、NaOH、HCl
C.NaOH、BaCl2、Na2CO3、HCl D.Na2CO3、BaCl2、NaOH、HCl
②一次精制后的食盐水仍会有少量的Ca2+、Mg2+ , 需要送入阳离子交换塔进行二次精制,若不经过二次精制,直接进入离子膜电解槽,这样会产生什么后果.
-
(3) 图2是工业上电解饱和食盐水的离子交换膜电解槽示意图(阳极用金属钛网制成,阴极由碳钢网制成),则A处产生的气体是,F电极的名称是.电解总反应的离子方程式为.
-
(4) 从阳极槽出来的淡盐水中,往往含有少量的溶解氯,需要加入8%~9%的亚硫酸钠溶液将其彻底除去,该反应的化学方程式为.
-
(5) 已知在电解槽中,每小时通过1A的直流电理论上可以产生1.492g的烧碱,某工厂用300个电解槽串联生产8h,制得32%的烧碱溶液(密度为1.342t/m3)113m3 , 电解槽的电流强度1.45×104A,该电解槽的电解效率为(保留两位小数).
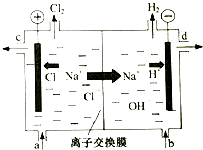
完成下列填空:
-
(1) 粗食盐的水溶液含有SO42﹣、Ca2+、Mg2+ . 若要除去SO42﹣ , 则需加的试列为.
-
(2) 精制饱和食盐水从图中位置补充,氢氧化钠溶液从图中位置流出(选填“a”、“”“b”、“c”或“d”)
-
(3) 0.1mol/L的Na2SO3溶液中各离子浓度从人到小的顺序为.
-
(4) 室温下,0.1mol/L的NaClO溶液的pH0.1mol/L的Na2SO3溶液的pH.(选填“大于”、“小于”或“等于”)(已知:H2SO3 K1=1.54×10﹣2 K2=1.02×10﹣7;HClO K=2.95×10﹣8)
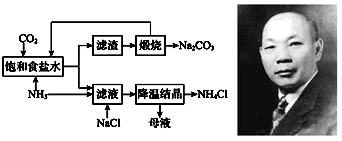
I.工业生产纯碱的工艺流程示意图如下:
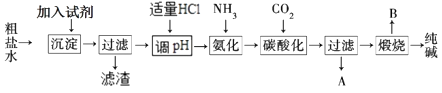
-
(1) 为除去粗盐水中的Mg2+、Ca2+、SO42-等杂质离子,加入试剂顺序合理的是________。A . 碳酸钠、氢氧化钠、氯化钡 B . 碳酸钠、氯化钡、氢氧化钠 C . 氢氧化钠、碳酸钠、氯化钡 D . 氯化钡、氢氧化钠、碳酸钠
-
(2) 工业生产纯碱工艺流程中,碳酸化时产生的现象是。
-
(3) 碳酸化后过滤,滤液A最主要的成分是(填写化学式),检验这一成分的阴离子的具体方法是:。
-
(4) 煅烧制取Na2CO3在(填字母序号)中进行。
a.瓷坩埚 b.蒸发皿 c.铁坩埚 d.氧化铝坩埚
-
(5) II.纯碱在生产生活中有广泛的用途。
工业上,可能用纯碱代替烧碱生产某些化工产品。如用饱和纯碱溶液与氯气反应可制得有效成分为次氯酸钠的消毒液,其反应的离子方程式为。
-
(6) 纯碱可制备重铬酸钠(Na2Cr2O7),铬铁矿中的1molCr2O3反应时需要通入标准状况下O2的体积为。
 2NH3 (g) ΔH< 0。在恒温恒容密闭容器中进行合成氨反应,各组分浓度与时间的关系如图所示。
2NH3 (g) ΔH< 0。在恒温恒容密闭容器中进行合成氨反应,各组分浓度与时间的关系如图所示。 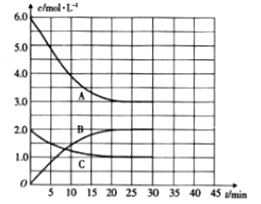
-
(1) 表示N2浓度变化的曲线是 (填字母),25 min 时c (NH3)=。
-
(2) 0~25min内,用H2 浓度变化表示的化学反应速率是。
-
(3) 此温度下,上述反应的平衡常数K 的数值为。
-
(4) 若升高温度,则平衡向(填“正反应”或“逆反应”)方向移动;正反应速率 (填“增大”“减小”或“不变”,下同 ), 逆反应速率。
下列叙述错误的是( )
 、Fe2+、Ag+
、Fe2+、Ag+
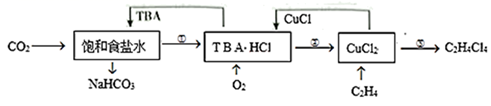
下列说法错误的是( )
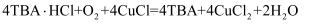 C . 理论上每产生
C . 理论上每产生 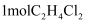 需要
需要 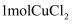 D . 流程中可循环利用的物质是TBA、CuCl
D . 流程中可循环利用的物质是TBA、CuCl
 等有害物质的排放
C . 铝及其合金是使用广泛的金属材料,工业上通常用电解氯化铝的方法制备铝
D . 食品工业以植物油和氢气为原料生产氢化植物油,利用了植物油的取代反应
等有害物质的排放
C . 铝及其合金是使用广泛的金属材料,工业上通常用电解氯化铝的方法制备铝
D . 食品工业以植物油和氢气为原料生产氢化植物油,利用了植物油的取代反应
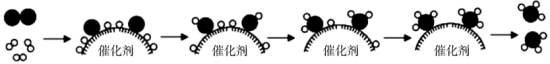
下列说法正确的是( )
 表示氢气分子
B . 过程中有“NH”“NH2”原子团生成
C . 催化剂增大了氢气的平衡转化率
D . 反应结束后催化剂的质量增加
表示氢气分子
B . 过程中有“NH”“NH2”原子团生成
C . 催化剂增大了氢气的平衡转化率
D . 反应结束后催化剂的质量增加
- 下列各句标点符号使用正确的一项是 A、“这题实在错得冤枉”!他恨得跺了一下脚说,“下次再不能‘大意失荆州’了。” B、如
- 设双曲线的渐近线与抛物线相切,则该双曲线的离心率为( ) A. B.
- 对于命题“我们班学生都是团员”,给出下列三种否定: ①我们班学生不都是团员;②我们班有学生不是团员;③我们班学生都不是团
- —Miss Li, are we going to have a picnic tomorrow?—Yes. But i
- Great changes ______in our city since 1980. A.took place
- 已知α-β=,且cosα+cosβ=,则cos(α+β)等于_________.
- 如图7所示,电阻R1与R3相等,电阻R2与R4相等,现有一个两端电压恒为10V的电源,当把该电源接在A、B两个接线柱时,
- 下列有关文献理解错误的是( ) A. “所在山洋,冬月地上有霜,扫取以水淋汁后,乃煎炼而成”过程包括了溶解、蒸发、
- 2003年,俄罗斯社会科学院某院士说:“把苏共送入停尸间的不是别人,而是我们苏联人自己。我们俄罗斯人以自己的沉痛灾难为代
- 设奇函数上是增函数,且对所有的都成立,当时,则t的取值范围是 ( ) A. B.
- “红色故都”江西瑞金农村流行这样的说法: 科技经纪人,教农一套点金术;信息经纪人,指农一条金光道;销售经纪人,给农一粒消
- 对下列实验中出现的异常现象分析合理的是 A.制取CO2气体时,始终收集不到CO2——收集CO2的集气瓶没盖严
- “视人之国,若视其国;视人之家,若视其家;视人之身,若视其身。”这一主张属于() A.儒家“仁爱”思想
- 在明亮的太阳照不到的地方,青苔的生命照常在萌动。青苔的花特别小,但一点也不自惭形秽,一点也不自暴自弃,而是象牡丹一样自豪
- 阅读下面这首唐诗,完成小题。 金陵望汉江 李 白 汉江回万里,派作九龙盘①。 横溃豁中国,崔嵬飞迅湍。 六帝沦亡后②,三
- 根据牛顿第一定律可知( ) A.物体运动状态改变时,一定受到外力的作用 B.物体若不受外力的作用,一定处于静止状
- 如图为某生态系统能量流动示意图。下列说法正确的是 A.图中甲所固定的能量是乙、丙的能量之和 B.若丙增
- 下列句子中文言词语解析错误的一项是 A.足以极视听之娱 (尽情享受)/ 形容词用作动词 B.子孙帝王万世之业也 (称
- 进行一氯取代反应后,只能生成三种沸点不同的产物的烷烃是( ) A.(CH3)2CHCH2CH3
- 下面几幅图是课本中的一些实验装置图,请在题中空格处填入相应的内容.(1)图a装置探究平面成像特点,选用玻璃板取代平面镜的



