化学研究方法与工业化学 知识点题库
-
(1) 高炉炼铁的原料有铁矿、焦炭和石灰石,其中起熔剂作用的是,目的是除去铁矿石中的脉石,在铁水的上部形成炉渣而与铁水分离.
-
(2) 焦炭在高炉炼铁中起着举足轻重的作用,下列不属于焦炭作用的是________.A . 作为燃料,为炼铁中的化学反应提供能量 B . 作为还原剂与二氧化碳反应产生还原氧化铁的一氧化碳 C . 对高炉中的物料起到支撑和疏散的作用 D . 作为溶剂,除去铁矿石中的杂质
-
(3) 高炉炼铁的污染非常严重,目前我国部分大城市中的钢铁厂借着搬迁的机会也在进行着工艺改进.高炉炼铁导致的环境污染有________.A . 臭氧空洞 B . 酸雨 C . 一氧化碳毒害 D . 沙尘暴
-
(4) 写出高炉炼铁中与碳元素有关的氧化还原反应化学方程式:.
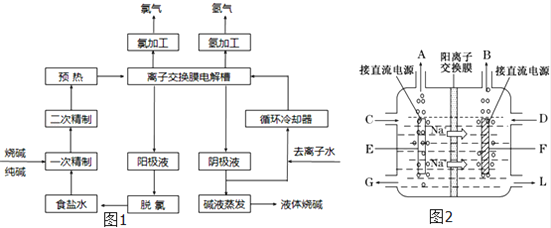
(1)该流程中可以循环的物质是 .
(2)电解法制碱的主要原料是饱和食盐水,由于粗盐水中含有Ca2+、Mg2+、SO42﹣等无机杂质,所以在进入电解槽前需要进行两次精制,写出一次精制中发生的离子方程式,若食盐水不经过二次精制就直接进入离子膜电解槽会产生什么后果 .
(3)图2是工业上电解饱和食盐水的离子交换膜电解槽示意图(阳极用金属钛网制成,阴极由碳钢网制成).则B处产生的气体是 ,E电极的名称是 .电解总反应的离子方程式为 .
(4)从阳极槽出来的淡盐水中,往往含有少量的溶解氯,需要加入8%~9%的亚硫酸钠溶液将其彻底除去,该反应的化学方程式为 .
(5)已知在电解槽中,每小时通过1安培的直流电可以产生1.492g的烧碱,某工厂用300个电解槽串联生产8小时,制得32%的烧碱溶液(密度为1.342吨/m3)113m3 , 电解槽的电流强度1.45×104A,该电解槽的电解效率为 .
(1)如表列举了不同温度下大气固氮和工业固氮的部分K值.
反应 | 大气固氮 N2(g)+O2(g)⇌2NO(g) | 工业固氮 N2(g)+3H2(g)⇌2NH3(g) | |||
温度/℃ | 27 | 2000 | 25 | 400 | 450 |
K | 3.84×10﹣31 | 0.1 | 5×108 | 0.507 | 0.152 |
①分析数据可知:大气固氮反应属于 (填“吸热”或“放热”)反应.
②分析数据可知:人类不适合大规模模拟大气固氮的原因 .
③从平衡视角考虑,工业固氮应该选择常温条件,但实际工业生产却选择500℃左右的高温,解释其原因 .
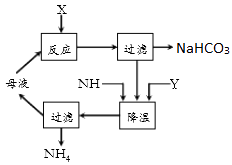
(2)工业固氮反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(р1、р2)下随温度变化的曲线,如图所示的图示中,正确的是 (填“A”或“B”);比较р1、р2的大小关系 .
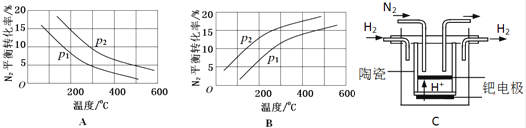
(3)20世纪末,科学家采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现高温常压下的电化学合成氨,提高了反应物的转化率,其实验简图如C所示,阴极的电极反应式是 .
(4)近年,又有科学家提出在常温、常压、催化剂等条件下合成氨气的新思路,反应原理为:2N2(g)+6H2O(1)⇌4NH3(g)+3O2(g),则其反应热△H= .
(已知:N2(g)+3H2(g)⇌2NH3(g)△H=﹣92.4kJ•mol﹣1 , 2H2(g)+O2(g)⇌2H2O(l)△H=﹣571.6kJ•mol﹣1)
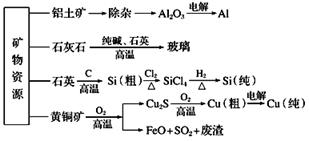
工业上以黄铁矿为原料,采用接触法生产硫酸.请回答下列问题:
(1)煅烧黄铁矿的设备名称是 ,进料前必须将黄铁矿粉碎,目的是 (填一种用途).
(2)进入接触室前的气体必须经过净化处理,目的是防止 .
(3)生产过程中,吸收三氧化硫常用的物质是 .
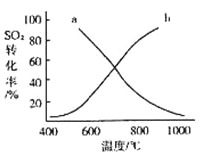
(4)温度变化与二氧化硫转化率的变化关系可用如图中的曲线 (填“a”或“b”)表示.
(5)工业上常用熟石灰和硫酸处理、回收尾气中的有害气体.反应的化学方程式为: 、 .
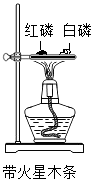 B .
B . 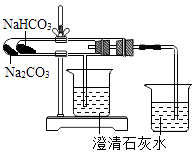 C .
C . 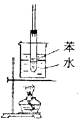 D .
D . 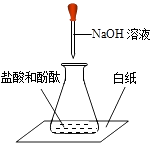
-
(1) 在一定条件下:2N2(g)+6H2O(g)═4NH3(g)+3O2(g).已知该反应的相关的化学键键能数据如下:
化学键
N≡N
H﹣O
N﹣H
O=O
E/(kJ/mol)
946
463
391
496
则该反应的△H=kJ/mol.
-
(2) 电厂烟气脱氮的主要反应I:4NH3(g)+6NO(g)⇌5N2(g)+6H2O(g)△H<0,副反应II:2NH3(g)+8NO(g)⇌5N2O(g)+3H2O(g)△H>0.
①反应I的化学平衡常数的表达式为.
②对于在2L密闭容器中进行的反应I,在一定条件下n(NH3)和n(N2)随时间变化的关系如图1所示:
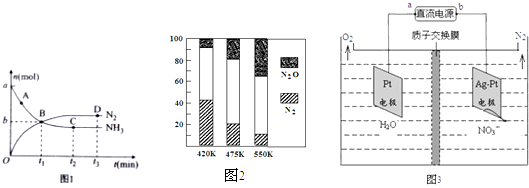
用NH3表示从开始到t1时刻的化学反应速率为(用a、b、t表示)mol/(L•min),图中表示已达平衡的点为.
③电厂烟气脱氮的平衡体系的混合气体中N2和N2O含量与温度的关系如图2所示,在温度420~550K时,平衡混合气体中N2O含量随温度的变化规律是,造成这种变化规律的原因是.
-
(3) 电化学降解法可治理水中硝酸盐的污染.电化学降解NO3﹣的原理如图3所示,电源正极为(填“a”或“b”),阴极电极反应式为.
 Al(OH)3+3H+
D . 粗铜(含Cu及少量Zn、Fe、Ag等)电解精炼时,阳极主要发生反应:Ag-e-=Ag+
Al(OH)3+3H+
D . 粗铜(含Cu及少量Zn、Fe、Ag等)电解精炼时,阳极主要发生反应:Ag-e-=Ag+
-
(1) Ⅰ.现代工业常以氯化钠为原料制备纯碱,部分工艺流程如图:
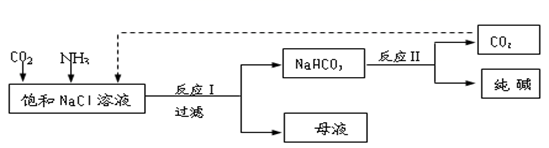
已知NaHCO3在低温下溶解度较小。
反应Ⅰ的化学方程式为。
-
(2) 处理母液的方法:向母液中加入石灰乳,反应的化学方程式为,目的是使循环利用。
-
(3) Ⅱ.某化学小组模拟“侯氏制碱法”,以NaCl、NH3、CO2和水等为原料以及如图所示装置制取NaHCO3 , 然后再将NaHCO3制成Na2CO3。
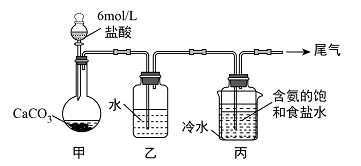
装置丙中冷水的作用是;由装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有、洗涤、灼烧。
-
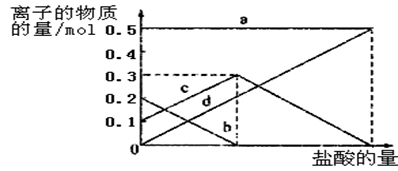
(4) 若灼烧的时间较短,NaHCO3将分解不完全,该小组对一份加热了t1min的NaHCO3样品的组成进行了以下探究。取加热了t1min的NaHCO3样品29.6g完全溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中有关离子的物质的量的变化如图所示。曲线c对应的溶液中的离子是(填离子符号);该样品中NaHCO3和Na2CO3的物质的量分别是mol、mol。
① 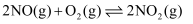
② 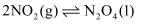
③ 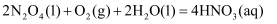
下列有关工业制取浓硝酸反应的说法错误的是( )
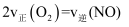 B . 使用高效催化剂能提高反应①中NO的平衡转化率
C . 反应②在一定温度下能自发进行,则正反应为放热反应
D . 标准状况下,反应③中每消耗22.4LO2 , 转移电子的数目约为
B . 使用高效催化剂能提高反应①中NO的平衡转化率
C . 反应②在一定温度下能自发进行,则正反应为放热反应
D . 标准状况下,反应③中每消耗22.4LO2 , 转移电子的数目约为 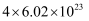

- 对于反应中的能量变化,表述正确的是 A.断开化学键的过程会放出能量 B.吸热反应中,反应物的总能量小于生成物的总
- 一项新研究预测,在距太阳系400光年远的地方,一个新的恒星“即将”诞生。这一事实充分说明() A.人能够能动地认识世界
- 今年4月14日,我国青海玉树地区发生7.1级地震。在灾后防预工作中,常用二氧化氯(化学式:ClO2)作消毒剂。二氧化氯在
- 2005年4月29日,台湾国民党主席连战与中共总书记实现了跨越60年的握手。想一想,如下图,60年前国共两党最高领导人曾
- 我们的政府是人民政府,要努力建设法治政府、责任政府和服务政府。这里的“建设法治政府”,就是要①用法律、法规规范政府行为
- 如图所示的工件的主视图是()
- 如图甲所示,将一个小木块轻轻地放在逆时针匀速转动的传送带上端。则乙图中描述小木块在传送带上的速度随时间变化关系的图像不可
- 文言文阅读(12分)既罢归国,以相如功大,拜为上卿,位在廉颇之右。廉颇曰:“我为赵将,有攻城野战之大功,而蔺相如徒以口舌
- 阅读下面一首宋诗,然后回答问题。 池口风雨留三日 黄庭坚 孤城三日风吹雨,小市人家只菜蔬。 水远山长双属玉,身闲心苦一舂
- 用32P标记了果蝇体细胞(含8条染色体)的DNA分子双链,再将这些细胞转入不含32P的培养基中培养,在第2次细胞分裂的前
- 2007年,青岛市生产总值突破3700亿元,同比增长16%,人均GDP超过6000美元,比2002年翻了一番以上。民营经
- 铁上镀铜,()做阳极,()阴极 A. 铁 铁 B. 铜 铜 C. 铁 铜 D. 铜
- 补写出下列名篇名句中的空缺部分。(两题任选一题,每空1分,共5分)(1)纤云弄巧, ,
- 如图4-2-18所示.两个高1.2 m左右的支架上,放着两条平行光滑铝合金导轨,且已调成水平状态,在光滑的导轨上放着两辆
- The visiting minister expressed his satisfaction with his ta
- 若二倍体生物正常体细胞中含8条染色体,则图中表示一个染色体组的是 ( )
- 2010年6月17日,外交部发言人秦刚举行例行记者会时指出,中国政府反对把人民币汇率问题政治化,反对某些国家借此问题施压
- 如图,在扇形纸片AOB中,OA =10,ÐAOB=36°,OB在桌面内的直线l上.现将此扇形沿l按顺时针方向旋转(旋转过
- 蛋白质是生命活动的主要承担者.下列不属于组成蛋白质的氨基酸是() A.
- 右图为神经元的结构模式图,请根据图回答:(1)请写出图中标号的名称:① ;② ;③



