化学研究方法与工业化学 知识点题库
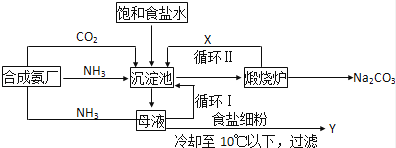
(1)沉淀池中加入(或通入)有关物质的顺序为→ →
(2)写出上述流程中X、Y的化学式:X Y
(3)写出沉淀池中发生的化学反应方程式
(4)侯氏制碱法的生产流程中可以循环使用的物质主要为 、
(5)从沉淀池中取出沉淀的操作是 ,为了进一步提纯NaHCO3晶体,可采用 法
(6)若在煅烧炉中燃烧的时间较短,NaHCO3将化解不完全.现若取10.5g NaHCO3固体,加热一定时间后,剩余固体的质量为7.1g,如果把此剩余固体全部加入到200mL 1mol/L的盐酸中,充分反应后溶液中H+的物质的量浓度为 mol/L(溶液体积变化忽略不计)
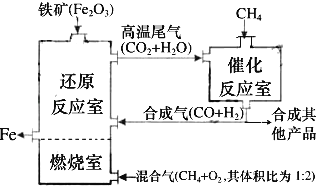
铁及其化合物在生产、生活中有广泛应用.请回答下列问题:
(一)高炉炼铁过程中发生的主要反应为: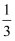 Fe2O3(s)+CO(g)⇌
Fe2O3(s)+CO(g)⇌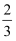 Fe(s)+CO2(g)
Fe(s)+CO2(g)
已知该反应在不同温度下的平衡常数如下:
温度/℃ | 1000 | 1115 | 1300 |
平衡常数 | 4.0 | 3.7 | 3.5 |
(1)该反应的平衡常数表达式K= ;△H 0(填“>”、“<”或“=”).
(2)欲提高上述反应中CO的平衡转化率,可采取的措施是 .
A.提高反应温度 B.移出部分CO2
C.加入合适的催化剂 D.减小容器的容积
(3)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,此时υ正 υ逆(填“>”、“<”或“=”).经过10min,在1000℃达到平衡,则该时间范围内反应的平均反应速率υ(CO2)= .
(二)高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.
(4)一定条件下Fe(OH)3与KClO在KOH溶液中反应可制得K2FeO4 , 其中反应的氧化剂是 ;生成0.5mol K2FeO4转移电子的物质的量是 mol.
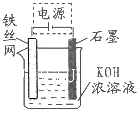
(5)从环境保护的角度看,制备K2FeO4较好的方法为电解法,其装置如图所示.电解过程中阳极的电极反应式为 .
-
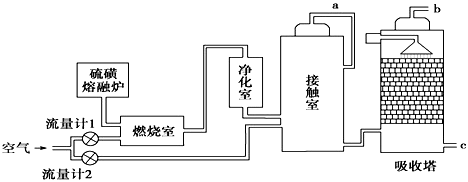
(1) 火山喷发所产生的硫磺可用于生产重要的化工原料硫酸.某企业用右图所示的工艺流程生产硫酸:
请回答下列问题:
①为充分利用反应放出的热量,接触室中应安装(填设备名称).吸收塔中填充有许多瓷管,其作用是.
②为使硫磺充分燃烧,经流量计1通入燃烧室的氧气过量50%.为提高SO2转化率,经流量计2的氧气量为接触室中二氧化硫完全氧化时理论需氧量的2.5倍,则生产过程中流经流量计1和流量计2的空气体积比应为.假设接触室中SO2的转化率为95%,b管排出的尾气中二氧化硫的体积分数为.(空气中氧气的体积分数按0.2计),该尾气的处理方法是.
③与以硫铁矿为原料的生产工艺相比,该工艺的特点是(可多选).
A.耗氧量减少 B.二氧化硫的转化率提高
C.产生的废气减少 D.不需要使用催化剂
-
(2) 硫酸的用途非常广泛,可应用于下列哪些方面 (可多选).A . 橡胶的硫化 B . 表面活性剂“烷基苯磺酸钠”的合成 C . 铅蓄电池的生产 D . 过磷酸钙的制备
-
(3) 矿物燃料的燃烧是产生大气中SO2的主要原因之一.在燃煤中加入适量的石灰石,可有效减少煤燃烧时SO2的排放,请写出此脱硫过程中反应的化学方程式.
①在含氨的饱和氯化钠溶液中通入CO2制得NaHCO3
②再将NaHCO3焙烧制得纯碱,CO2循环使用
③析出小苏打的母液中加入生石灰,NH3循环使用
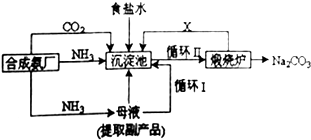
我国著名化学家侯德榜改革国外的纯碱生产工艺,生产流程可简要表示如下:
-
(1) 上述生产纯碱的方法称,副产品的一种用途为.
-
(2) 沉淀池中发生的化学反应方程式是.
-
(3) 写出上述流程中X物质的分子式.
-
(4) 向母液中通氨气,加入细小食盐颗粒,冷却析出副产品,通氨气的作用有.
-
(5) 设计实验检验产品碳酸钠中是否含有氯化钠
-
(6) 侯德榜制碱的方法与氨碱法相比,其优点是
-
(1) 在工业生产水煤气时,燃料层的温度会下降,这说明。
-
(2) 提出猜想:水煤气的成分可能是 ①和氢气,②和氢气;提出以上猜想的依据是(填元素符号)。
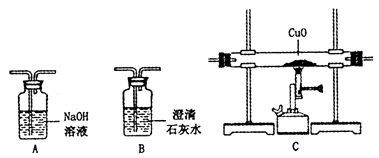
设计实验:请从下列装置中选择一种,设计简单的实验证明猜想。
-
(3) 你选择装置是(填字母代号)。
-
(4) 实验结论:如果,那么猜想(填序号)是合理。
 2NH3 , 回答下列问题:
2NH3 , 回答下列问题:
-
(1) 反应过程中拆开的化学键是;
-
(2) 反应放热,从价键角度分析,反应放热的原因是,下列图像正确的是。
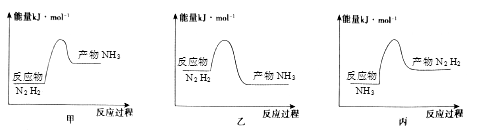
-
(3) 在体积是2L的密闭容器中开始加入1molN2 , 3molH2 , 反应过程浓度中,物质的浓度与时间的关系如图所示。
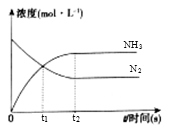
①t1时生成NH3的物质的量是;用H2表示的化学反应速率υ(H2)=。
②下列各项能表明反应达到化学平衡状态的是。
A.容器中气体的密度保持不变
B.容器中气体的压强不变
C.氨气的含量不变
D.拆开3molH-H键同时形成6molN-H键
-
(4) 下列措施中能提高合成氨反应化学反应速率的是。
A.使用高效催化剂
B.恒温恒容再充入氢气
C.降低反应温度
D.扩大容器体积
-
(1) 制硫酸的三种原料是、、,三个生产过程是①,写出反应方程式,②,写出反应方程式,③,写出反应方程式,三废指的是、、。
-
(2) 合成氨的反应原理工业合成氨的反应条件为浓度使用过量的、温度℃、高压MPa、。
①根据组成元素将氧化物分成酸性氧化物和碱性氧化物
②根据是否有丁达尔效应将分散系分为溶液、胶体和浊液
③根据反应是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应
④根据水溶液是否能导电将化合物分为电解质和非电解质
⑤根据酸分子中含有的氢原子个数,将酸分为一元酸、二元酸和多元酸
 与
与  反应生成
反应生成 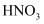 C .
C . 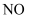 和
和  反应生成
反应生成  D .
D .  和
和  在一定条件下合成氨
在一定条件下合成氨
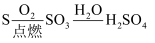 B . 淀粉
B . 淀粉  C .
C .  D . 饱和NaCl溶液
D . 饱和NaCl溶液  NaHCO3晶体
NaHCO3晶体
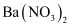 溶液,有白色沉淀生成,则原溶液中一定含有
溶液,有白色沉淀生成,则原溶液中一定含有  B . 合成氨工业中,使用铁触媒作催化剂,目的是打破原有平衡状态,从而建立新的平衡,提高氨气的产率
C . 少量的
B . 合成氨工业中,使用铁触媒作催化剂,目的是打破原有平衡状态,从而建立新的平衡,提高氨气的产率
C . 少量的 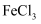 加入到过量的
加入到过量的  溶液中,充分振荡,再滴入
溶液中,充分振荡,再滴入  溶液,溶液无现象
D . 合成氨工业的成功,改变了世界粮食生产的历史,使人类免受饥荒之苦
溶液,溶液无现象
D . 合成氨工业的成功,改变了世界粮食生产的历史,使人类免受饥荒之苦
-
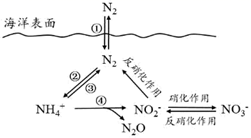
(1) 海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是(填图中数字序号)。
-
(2) 下列关于海洋氮循环的说法正确的是(填字母序号)。
a.海洋中存在游离态的氮
b.海洋中的氮循环起始于氮的氧化
c.海洋中的反硝化作用一定有氧气的参与
d.向海洋排放含NO
 的废水会影响海洋中NH
的废水会影响海洋中NH  的含量
的含量 -
(3) 有氧时,在硝化细菌作用下,NH
 可实现过程④的转化,将过程④的离子方程式补充完整:4NH
可实现过程④的转化,将过程④的离子方程式补充完整:4NH  +5O2 =2NO
+5O2 =2NO  +_H++_+
+_H++_+
-
(4) 为避免含氮废水对海洋氮循环系统的影响,需经处理后排放。右图是间接氧化工业废水中氨氮(NH
 )示意图。
)示意图。 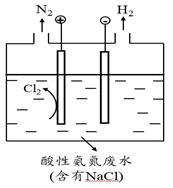
①结合电极反应式简述间接氧化法去除氨氮的原理:。
② 若生成H2和N2的物质的量之比为3:1,则处理后废水的pH将填“增大”“不变”或“减小”)。
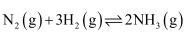 ,
, 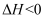 , 下列关于合成氨工业的说法不正确的是( )
, 下列关于合成氨工业的说法不正确的是( )
- 图甲所示,为某同学测绘额定电压为2.5V的小灯泡的I—U特性曲线的实验电路图。1.根据电路图甲,用笔画线代替导线,将图乙
- 从100 mL某种待测浓度的 H2SO4 溶液中取出25 mL,加入10 mL 0.5 mol·L-1 BaCl2 溶液
- —___________do you usually go fishing? —In summer. A.How
- 下列词语书写无误的一项是( ) A.并吞八方 内立法度 揭杆为旗 宰割天下 B.不测之源
- 某同学在实验室测定了几种溶液的pH,其结果如下表:溶液 盐酸 CuCl2 溶液 Na2SO4 溶液 水 Na2CO3 溶
- It took the police a long time to find some evidence. The ne
- 有关我国季风的说法,错误的是( ) A.受夏季风影响明显的地区叫季风区 B.受冬季风影响明显的地区叫非季风区 C
- 小璐同学发现洗手盆下方有如图13所示的U型管道,它是利用__________的原理。
- 可燃物在 的空间内, 地燃烧,就会在短时间内聚积大量的热,使气体的体积迅速膨胀而引起
- Do remember: you are 30times more _____ to be hit by lightn
- 在中,角所对边分别为,且,,面积,则 .
- 下列句子中加点的成语使用正确的一项是 A.最近,一名杭州乞丐流浪者——“犀利哥”的照片风靡网络,“犀利哥”迅速走红
- 下列物质中,既含有离子键,又含有非极性键的是()。 A.NaOH B.Na2O2 C.MgCl2
- 写作(40分)阅读下面文字,根据要求作文。世界虽大,但只要心灵相通,纵然上下五千年,纵横九万里,仍然可以交流和沟通,更何
- 在文中横线处填上恰当的关联词语,使上下文连贯起来。将答案写在文段下面对应的序号后。(6分) 语言的形式, ① 能
- 若3+2i是方程2x2+bx+c=0(b、c∈R)的一个根,则c的值为( )A.-13
- 20世纪90年代以来经济全球化迅速发展的根本原因是( )A.科学技术的发展和生产力的显著提高 B.新型交通和通讯方
- 伊斯兰文明和中华文明都是人类文明的瑰宝,都对人类社会的进步和发展有着不可磨灭的贡献。下列对待伊斯兰文化的态度,正确的是
- “一九七九年那是一个春天,有一位老人在中国的南海边画了一个圈。”这个“圈”中最具有代表性的城市是 A.深圳
- 阅读下面文字,根据要求作文。 有人在飞机上发现这样一个现象:同样是30岁到40岁年纪的旅客,头等舱的旅客往往是在看书,公



