化学实验方案设计与评价 知识点题库
选项 | 实验目的 | 实验操作 |
A. | 鉴别蒸馏水 | 观察颜色 |
B. | 比较Fe、Cu、Ag的金属活动性 | 铁丝浸入CuSO4溶液,铜丝浸入AgNO3溶液 |
C. | 除去CO2气体中的CO | 点燃 |
D. | 鉴别硬水和软水 |
①用小木条探究蜡烛各层火焰温度
②用鸡蛋壳和食醋来制取少许二氧化碳
③用过滤法使硬水变为软水
④用1L黄豆和1L绿豆混合所得体积小于2L的实验,说明分子之间有间隔.

实验Ⅰ:再小试管中加入8mL溶质质量分数为3%的双氧水(ρ=1g/mL),在抽滤瓶中分别加入不同质量的MnO2 , 使其反应并启动传感器,记录容器内压强变化于图2中.
实验Ⅱ:在抽滤瓶中加入0.1g MnO2 , 在小试管中分别加入不同体积溶质质量分数为3%的双氧水,使其反应并启动传感器,记录容器内压强变化于图3中.
请根据以上实验回答下列问题:
-
(1) 使容器内压强增大的反应的化学方程式:.
-
(2) 根据图2可发现,该实验条件下,30s内催化分解8mL溶质质量分数为3%的双氧水,MnO2的最小用量为 g;
-
(3) 根据图3可发现,0.1g MnO2至少能快速催化分解 g过氧化氢;
-
(4) 根据图2与图3可发现,MnO2的用量总体上与O2产量(填“正相关”、“不相关”或“负相关”),根据图3还可发现,该试验中,O2产量总体上与双氧水用量是(填“正比”或“反比”);
-
(5) 下列因素中,与本实验所测数据的精确度有关的是A . 反应容器的气密性 B . 称量MnO2质量的精准度 C . 量取双氧水体积的精准度.

-
(1) 实验I:在盛有少量蒸馏水的小烧杯中滴入2~3滴酚酞试液,再向其中滴加浓氨水,由实验I得出的结论有.
-
(2) 实验Ⅱ(如图甲所示):烧杯B中的现象是;产生这一现象的原因是.
-
(3) 为使实验结论准确可靠,该兴趣小组设计实验Ⅲ(如图乙所示)作为对比实验.你认为有无必要(填“有”或“无”),理由是.
-
(4) 【发现问题】虽然课本上这个实验的现象明显,但也存在一些不足,如:氨水的用量大、实验装置无法固定、有很多氨气逸出大烧杯等.
【查阅资料】
①氨气的密度比空气的密度小.
②T形三通管属于微型化学仪器.
【实验改进】在老师指导下,同学们改用图丙装置探究微粒的运动性.
在T形三通管的粗玻璃管里,固定一根湿润的酚酞纱布条.
用(填写仪器名称)吸取少许浓氨水,将其滴入T形三通管的细弯管处,然后用橡皮帽封闭管口.
-
(5) 一会儿,观察到(填“ba”或“bc”)段纱布条变成红色.
-
(6) 微热细弯管处的浓氨水,纱布条变红的速率会加快.
【实验反思】改进实验与课本实验相比较,有不少的优点,请你写出其中的一条.
 氧气约占空气总体积的
氧气约占空气总体积的 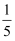 B .
B .  二氧化碳的密度比空气大且不支持燃烧
C .
二氧化碳的密度比空气大且不支持燃烧
C .  天平不平衡说明该反应不遵守质量守恒定律
D .
天平不平衡说明该反应不遵守质量守恒定律
D .  燃烧条件之一是温度需达到可燃物的着火点
燃烧条件之一是温度需达到可燃物的着火点

| |
A.CO2 能使紫色石蕊变红 | B.二氧化锰是催化剂 |
|
|
C.金属 M 生锈需要 O | D.同种溶质在不同溶剂中的溶解性不同 |
 {①变红色;变红色+石蕊试液+石蕊试液②不变红色;不变红色+石蕊试液+石蕊试液{①稀
{①变红色;变红色+石蕊试液+石蕊试液②不变红色;不变红色+石蕊试液+石蕊试液{①稀  变红色;稀
变红色;稀  变红色+石蕊试液+石蕊试液②
变红色+石蕊试液+石蕊试液②  不变红色;溶液不变红色+石蕊试液+石蕊试液()
不变红色;溶液不变红色+石蕊试液+石蕊试液()
 D . 小逸:
D . 小逸: 

①取一段镁带样品,准确称得其质量为0.030g;
②往量气管内装水至低于刻度“0”的位置,如图所示,(未装药品)装配好仪器;
③………………….;
④在试管中加入足量的稀硫酸,稍倾斜试管,将用水湿润的镁带小心贴在试管壁上,塞紧橡皮塞;
⑤调整量气管液面,使两边的液面保持同一水平,记录量气管中液面位置;
⑥把试管底部略为抬高,使镁带与稀硫酸接触完全反应;
⑦待冷却至室温后,再次记录量气管中液面位置;
⑧算出量气管中增加的气体体积为23.96 mL;
已知:同温同压下,不同气体混合后体积等于混合前各气体体积之和。
请回答下列问题:
-
(1) 写出镁与稀硫酸反应的化学方程式:。
-
(2) 能否用托盘天平称量0.030 g镁带样品(填“能”或“不能”)。
-
(3) 操作③是。
-
(4) 实验过程⑦中再次记录量气管的液面位置时,试管中留有氢气,是否会影响实验最终结果(填“是”或“否”),理由是。
-
(5) 若实际测得氢气的体积与理论值相比偏大,则可能的原因是。
 Ag:Mg
Ag:Mg  2AgCl = 2MgCl2
2AgCl = 2MgCl2  Ag
B . 用硝酸钡区别氢氧化钠和硫酸钾:K2SO4
Ag
B . 用硝酸钡区别氢氧化钠和硫酸钾:K2SO4  Ba(NO3)2 = BaSO4↓
Ba(NO3)2 = BaSO4↓  KNO3
C . 用稀硫酸除去炭粉中的少量氧化铜:CuO
KNO3
C . 用稀硫酸除去炭粉中的少量氧化铜:CuO  H2SO4 =CuSO4
H2SO4 =CuSO4  H2O
D . 用氢氧化钙治疗胃酸过多症:Ca(OH)2
H2O
D . 用氢氧化钙治疗胃酸过多症:Ca(OH)2  2HCl = CaCl2
2HCl = CaCl2  2H2O
2H2O
(查找资料)无水乙醇(无水酒精)可以燃烧,也可以引燃。
(作出猜想)①无水乙醇可以引燃盘成螺旋状的铁丝
②无水乙醇不能引燃盘成螺旋状的铁丝
-
(1) 实验探究:
实验的步骤和现象
①先把细铁丝的一端盘成螺旋状,另一端用坩埚钳夹住。
②用小烧杯盛一定量的无水乙醇,待用。
③把酒精灯和充满氧气且瓶底有少量水的集气瓶放在较近的位置,并点燃酒精灯。
④用坩埚钳夹住细铁丝的一端并将有螺旋状的另一端伸入到无水乙醇中,利用无水乙醇的表面张力,使细铁丝有螺旋状一端蘸满无水乙醇。取出后,马上在酒精灯上点燃,并迅速伸入到充满氧气且瓶底有少量水的集气瓶中,可以看到铁丝在氧气中,,放出热量,生成物质。实验中集气瓶瓶底要装少量水的原因。
-
(2) 实验的优点和结论分析:
铁丝在氧气中燃烧是检验氧气性质的一个重要的实验,按照《教科书》中的做法,难以成功,原因就是对引燃的燃烧的程度难以把握。
-
(3) 此方法极易,实验效果明显,不会再为火柴梗燃烧的程度而担忧。写出铁丝在氧气中燃烧的文字表达式。
(提出问题)橙皮的形状、温度以及酸碱性是否影响橙皮汁溶解泡沫饭盒的速率?
(查阅资料)碳酸钠溶液呈碱性,稀醋酸溶液呈酸性。
(进行实验)
每次取1/4块橙皮,1/4个泡沫饭盒进行实验,所用溶液浓度均为5%,记录10分钟时的泡沫饭盒现象如下表所示。
实验1
|
序号 |
实验操作 |
饭盒表面的实验现象 |
|
1-1 |
将一块挤压出汁的橙皮放在泡沫饭盒上 |
明显凹凸不平以及很多小洞 |
|
1-2 |
将一块橙皮切成丝,均匀地放在泡沫饭盒上 |
一点凹凸不平 |
|
1-3 |
将一块橙皮切成粒,均匀地放在泡沫饭盒上 |
一点凹凸不平 |
|
1-4 |
将一块橙皮研磨成酱,均匀放在泡沫饭盒上 |
较多凹凸不平 |
|
1-5 |
将一块橙皮研磨成酱,加热后均匀放在泡沫饭盒上 |
仍然光滑 |
实验2
|
序号 |
实验操作 |
饭盒表面的实验现象 |
|
2-1 |
将一块橙皮研磨成酱再滴入10mL醋后均匀放在泡沫饭盒上 |
较多凹凸不平 |
|
2-2 |
将一块橙皮研磨成酱再滴入10mL碳酸钠溶液后均匀放在泡沫饭盒上 |
较多凹凸不平 |
|
2-3 |
将amL醋均匀滴在泡沫饭盒上 |
仍然光滑 |
|
2-4 |
将bmL碳酸钠溶液均匀滴在泡沫饭盒上 |
仍然光滑 |
(解释与结论)
-
(1) 由实验1-2~1-4可以得出的实验结论是。
-
(2) 实验1-5的目的是。
-
(3) 实验2-3、 2-4中a和b的值分别为。
-
(4) 证明碱性环境对柠檬汁溶解泡沫饭盒速率无影响,依据的实验是。
-
(5) (反思与评价)
实验1-1的效果最明显的原因是。
-
(6) 根据实验1-5,可以猜测柠檬烯具有的性质是。
(查阅资料)
ⅰ.FeSO4溶液如果长时间显露在空气中,会与氧气发生反应转换成Fe2(SO4)3 , 色泽由最初的浅绿色或淡绿色转变成黄色。反应生成的Fe2(SO4)3遇KSCN溶液会变红。
ⅱ.保存FeSO4溶液时要加入稀硫酸和铁钉,置于阴凉处。
(提出猜想)
影响FeSO4溶液与氧气反应速率的因素可能有温度、浓度、溶液酸碱性、是否有铁钉等。
(进行实验)
|
编号 |
实验 |
0min |
30min |
2h |
|
① |
| 溶液为浅绿色 | 溶液略显黄色 | 溶液黄色略有加深 |
| ② | | 溶液为浅绿色 | 溶液明显变黄 | 溶液黄色明显加深 |
| ③ | | 溶液立即变黄 | ||
| ④ | | 溶液为浅绿色 | 溶液明显变黄,振荡后无变化 | 溶液黄色明显加深,振荡后无变化 |
| ⑤ | | 溶液为浅绿色 | 溶液为浅绿色 | 溶液为浅绿色;滴加 KSCN溶液后, 略显红色 |
| ⑥ | | 溶液为浅绿色 | 溶液为浅绿色 | 溶液为浅绿色;滴加 KSCN溶液后,略显红色,振荡后溶液变为浅绿色 |
-
(1) (解释与结论)
FeSO4溶液为浅绿色或淡绿色,Fe2(SO4)3溶液为黄色,可见这两种盐溶液的颜色差异与元素有关。
-
(2) 实验①中实验温度T=℃
-
(3) 通过对比实验②和③,得出的结论是 。
-
(4) 欲得出“稀硫酸和铁钉共同存在下才能有效防止FeSO4溶液变质”的结论,需要对比(填写实验编号)。
-
(5) 实验⑤中,FeSO4溶液变质的反应如下,补全该反应的化学方程式。

-
(6) 下列说法正确的是。
A 其他条件相同,溶液酸性增强,FeSO4溶液变质加快
B 其他条件相同,FeSO4溶液浓度越大,变质越快
C 实验⑥中,滴加KSCN 溶液后,略显红色,振荡后溶液变为浅绿色,可能是发生了反应

(查阅资料)
饱和氯化镁溶液的pH约为4
(实验过程)
-
(1) 实验前先将镁条需先打磨的原因是。
-
(2) 将打磨后的镁条放入锥形瓶中,再将注射器中某浓度的盐酸压入锥形瓶中,通过数字传感器测定实验中密闭容器(气密性良好)内压强与时间的关系如图所示。
用pH试纸测定反应后溶液的酸碱度。

(结果分析)
①注射器注入盐酸后,镁条表面的现象是。
②镁条与盐酸反应的化学方程式为。图中a、b、c、d四个点中,产生氢气最快的为点。
③图中c点镁条已完全溶解,cd段容器内压强逐渐减小的原因可能是。
④同学们根据测得反应后溶液的pH就直接得出其中含HCl,该pH的值可能是下列选项中的(填对应选项的字母)。
A.3 В.5 C.6
⑤甲同学提出向反应后的溶液中逐滴滴加NaOH溶液并振荡,若观察到的现象,也可以确定溶液中含HCl。
选 项 | A | B | C | D |
实 验 |
|
|
|
|
实 验 现 象 | 打开汽水瓶盖时,汽水 会自动喷出来 | 碘溶于水,几乎不溶于 汽油 | 白磷燃烧,产生大量白 烟,活塞先向右再向左移动,冷却至室温后, 最终停在刻度“4”附近 | 空气中,带火星的木条 复燃;呼出气体中,带 火星的木条熄灭 |
实 验 结 论 | 说明气体在水中的溶 解度随压强的增大而 减小 | 说明物质的溶解性与 溶剂的种类有关 | 氧气约占空气体积的 五分之一 | 空气中的氧气比呼出 气体中氧气多 |
- 下列说法正确的是:( )A.仅含有Na+、H+、OH—、CH3COO—四种离子的某溶液中可能存在:c(Na+)>
- 赵刚在今年5月12日发生的汶川大地震中失血过多,急需输血。经化验,他的血型为AB型。在正常情况下应该给他输入的血液为 A
- If the man is only interested in your looks, _____ just show
- 在人体内环境中发生的生理过程是( ) A.血浆蛋白的合成 B.记忆细胞增殖分化为效应B细胞,产生特异性抗体,与抗原
- Does solving a math problem give you a headache?Do you feel
- 一位留美博士放弃富足的生活,和妻子一起毅然回到国内做起了专职志愿者的工作,救助那些因贫困而上不了学的孩子。记者问他:“你
- 新中国成立后,第一次正确分析国内主要矛盾的中国的全国代表大会是( ) A.中共七大 B.中共八大
- 目前,仍然存在一些企业虚列出口货物数量,虚报出口货物价格、伪造、涂改退税凭证,这些行为属于( )行为。 A.抗税
- When a pencil is partly in a glass of water, it looks as if
- 2010年12月26日,温家宝总理在回答民众关于调控房价成果的敏感问题时,开门见山就说:“对敏感问题不回避,今年我们采取
- 化 学 反 应化学反应方程式简 答双氧水与二氧化锰混合二氧化锰的作用镁带在二氧化碳中燃烧氧化剂为氯化铁与氢氧
- 1951年世界和平理事会一致尊崇为世界文化名人的是( ) A. 李时珍 B. 徐光启 C. 詹天佑 D.
- 下列有机物命名正确的是( ) A.2-乙基戊烷
- 在-3,-1,0,2这四个数中,最小的数是( ) A. -3 B. -1 C. 0
- 复数(i是虚数单位)的共轭复数在复平面内对应的点在( ) A.第一象限 B.第二象限 C.
- “少年上人号怀素,……起来向壁不停手,一行数字大如斗。悦悦如闻神鬼惊,时时只见龙蛇走。左盘右蹙如惊电,状同楚汉相攻战。”
- I don’t know what happened ______ the old man yesterday. A.
- 两地相距,甲、乙两从两地出发相向而行,甲先出发.图中表示两人离地的距离与事件的关系.请结合图象解答下列问题: (1)表示
- 下列实验中(如图),观察不到明显变化的是 ( )
- 工业革命首先在下列哪一国家开始A.美国 B.法国 C.英国 D.意大

















