化学实验方案设计与评价 知识点题库
选项 | 实验内容 | 操作或所用试剂 |
A | 鉴别铁粉和木炭粉 | 观察颜色 |
B | 鉴别氯化铵和氯化钾 | 加熟石灰,混合研磨 |
C | 除去铜中混有的氧化铜 | 加过量稀硫酸,过滤 |
D | 除去氧化钙中混有的碳酸钙 | 高温煅烧 |

-
(1) 若按方案1制取铜,步骤Ⅱ反应的现象是什么?
-
(2) 若按方案2制取铜,请写出步骤Ⅱ发生反应的化学方程式.
-
(3) 两种方案比较,哪种方案更好?请说明理由.
A | B | C | D |
|
|
|
|
既说明甲烷具有可燃性,又说明甲烷中含有碳、氢两种元素 | 既说明二氧化碳密度比空气大,又说明二氧化碳不能燃烧也不支持燃烧 | 既说明电解水生成氢气和氧气,又说明水是由氢气和氧气组成的 | 既可探究可燃物的燃烧条件,又说明红磷不是可燃物 |
①检验一瓶气体是否为CO2 , 将燃着的木条伸入瓶中
②除去CO2中少量的CO,用点燃方法
③除去氧化铜中少量木炭粉,在空气中充分灼烧
④除去CO中少量的CO2 , 通入足量的澄清石灰水
⑤除去N2中少量的O2 , 通过足量灼热铜网
⑥碳粉中混有少量氧化铜粉末,加水过滤.


-
(1) 常温下,在密闭容器中的蔗糖溶液里,溶液下半部分的甜度与上半部分的甜度的关系是(填“相同”或“下半部分高”)。
-
(2) 用溶质质量分数为20%的氯化钠溶液来配制500g溶质质量分数为6%的氯化钠溶液,需要20%的氯化钠溶液g。
-
(3) 常温下,某同学为探究同一物质在不同溶剂中的溶解性不同,设计了如图所示的实验装置,实验时除了要控制温度相同、试管大小规格相同、加入水与汽油的体积相同外,还要控制食用油的相同。
-
(4) 事实证明,CaCl2溶于水,溶液导电能力显著增强,是因为其溶液中含有;若某CaCl2溶液中的Cl﹣为a个,则应对的Ca2+为个。

(提出问题)金属与盐酸反应快慢,除与金属的种类有关外,还受哪些因素的影响呢?
-
(1) (猜想与假设)a.可能与盐酸的浓度有关;b.可能与反应时的温度有关;c.你的猜想是。
-
(2) (设计并实验)小明利用如图甲所示装置,用不同质量分数的盐酸和相同形状的铝片进行如下实验。
实验编号
盐酸的浓度(均取20mL)
温度/℃
记录的数据
①
5%
30
②
10%
20
③
5%
20
④
10%
30
(交流讨论)请写出铝与盐酸反应的化学方程式:。
-
(3) 实验前小明先将分液漏斗的活塞关闭,再将注射器活塞往右拉,松手后,观察到注射器活塞回到原处。小明进行该操作的目的是。
-
(4) (分析数据、得出结论)
实验中记录的数据可能是:;对比实验②③可知对金属与酸反应的速率的影响
-
(5) 实验表明,四次实验时,反应的速率由快到慢依次为④、②、①、③.根据记录的数据分析,如果盐酸质量分数为10%,温度为25℃,则所记录数据应该介于两次实验所记录的数据之间。
-
(6) (拓展延伸)
小明进行铝与稀盐酸反应时,试管外壁发烫,并测得实验过程中生成氢气的体积随时间变化的曲线如图乙所示,根据曲线归纳铝与稀盐酸反应速率的变化规律:
-
(7) 研究小组同学对铝和稀盐酸的反应进行再探究。将橡皮塞连接气体压力传感器,烧瓶中放入铝片和稀盐酸,塞紧瓶塞并打开仪器,一段时间后,得到如丙图所示的气体压强与时间的关系曲线图。
AB段气体压力变化不明显的原因是:。
CD段气体压力逐渐下降的原因是:。
(查阅资料)
①固态管道疏通剂主要成分为NaOH、NaNO3和铝粉。
②铝粉能与NaOH溶液反应并能放出热量,其化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑。
③BaSO4、BaCO3都不溶于水,BaSO4也不溶于酸。
-
(1) 探究一:
(提出问题)固态管道疏通剂能够疏通管道的原理是什么?
(实验验证)
操作
现象
解释与结论
将菜叶、头发、米饭等垃圾放入烧杯中,然后加入少量固态管道疏通剂,再加入。
烧杯中产生大量气泡,烧杯壁发热,垃圾翻动,一段时间后菜叶、米饭部分溶解并分散成小颗粒,头发变成碎屑。
反应中产生的使垃圾翻动。
NaOH使垃圾分散成小颗粒,头发变成碎屑。
-
(2) (反思评价)经过大家讨论,认为固态管道疏通剂虽然能疏通管道,但使用过程中不安全,理由是;
目前超市出售更多的是液态管道疏通剂。液态管道疏通剂的成分主要是NaOH和一种钠盐。
-
(3) 探究二:
(提出问题)液态管道疏通剂中除NaOH以外,另一种钠盐是什么呢?
(猜想假设)这种钠盐是NaCl、Na2SO4、Na2CO3、NaNO3中的一种。
(实验验证)(不考虑疏通剂中其它成分对实验的影响)
操作
现象
结论
取少量液态疏通剂加入试管中,滴加溶液。
产生白色沉淀
该钠盐是Na2SO4 , 写出该反应的化学方程式:。
-
(4) (提出质疑)同学们认为该实验不能证明这种钠盐一定是Na2SO4 , 理由是,请你补充一个实验证明该钠盐是Na2SO4:;
-
(5) (拓展延伸) NaOH有强烈的腐蚀性,能腐蚀皮肤和衣物等,但管道疏通剂正是利用了它的腐蚀性,将“弊”变“利”。请你再举出一个利用物质的“弊”为生活服务的例子:。

|
装置类型 |
直立型 |
斜卧型 |
|
收集1瓶氧气所需时间/秒 |
59 |
68 |
|
收集2瓶氧气所需时间/秒 |
95 |
108 |
|
收集氧气的总体积/毫升 |
525 |
476 |

-
(1) 斜卧型装置中.试管口放置一团棉花的目的是:;写出试管中反应的化学方程式。
-
(2) 收集2瓶氧气所需时间直立型斜卧型(填“>”或“<”或“=”),除了该方法比较反应速率之外,还可以通过测量来比较两种装置制取氧气的反应速率。该实验中收集氧气的最佳方法是。
-
(3) 等质量的高锰酸钾完全反应,斜卧型装置收集到氧气的总体积比直立型少的原因是:。
-
(4) 根据相关方程式计算,得出5克高锰酸钾生成的氧气质量为理论值.实验中发现两种发生装置收集到的氧气质量明显大于理论值,他们对其原因进行了探究:
(提出假设)小峰假设:反应生成的锰酸钾在较高温度下受热分解出氧气;
你的假设:。
-
(5) (设计实验)要验证小峰的假设能否成立,请设计简明的实验方案
步骤
现象
结论
小峰猜想不正确
小峰猜想正确
-
(1) (猜想)Ⅰ、CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、CuO参与反应产生O2 , 反应前后质量和化学性质发生了改变;
Ⅲ、CuO是反应的催化剂,反应前后。
-
(2) (实验)用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:

①步骤①的目的是。
②步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、。
③过氧化氢能被CuO催化分解放出O2的符号表达式为。
 实验室制取氢气
B .
实验室制取氢气
B .  比较Fe、Cu、Ag的活动性
C .
比较Fe、Cu、Ag的活动性
C .  测定空气中氧气的含量
D .
测定空气中氧气的含量
D .  比较两种可燃物着火点的高低
比较两种可燃物着火点的高低
| | | | |
| A.探究锌、铁金属活动性强弱 | B.探究可燃物燃烧的条件 | C.探究物质在水中溶解时的能量变化 | D.探究温度对分子 运动快慢的影响 |

-
(1) A装置中仪器①的名称是,试管口略向下倾斜的原因是。
-
(2) 仪器②的名称是,该仪器的主要作用是。
-
(3) 实验室用加热氯酸钾制取氧气,应选择的发生装置为(填字母序号);若要收集较纯净的氧气,应选择的收集装置是(填字每序号)。实验室用过氧化氢溶液和二氧化锰的混合物制取氧气,应选择的发生装置为(填字母序号),发生反应的化学方程式。
-
(4) 实验室用高锰酸钾制纯净氧气时,下列做法错误的是
A在试管口放一团棉花,防止高锰酸钾粉末进入导管
B把试管口略向下倾斜固定在铁架台上
C导管口开始有气泡放出时就立即收集,防止生成的气体跑掉
D用高锰酸钾制取所需氧气停止加热时,先要把导管移出水面,然后再熄灭酒精灯
-
(5) 学习化学的捷径就是温故而知新,学会迁移。厨房中的天然气是一种比较清洁的化石能源,主要成分为甲烷(CH4),查阅资料得知:①通常状况下,甲烷是一种无色无味难溶于水的气体,密度比空气小;②实验室中常用无水醋酸钠和碱石灰两种固体药品,研磨均匀混合,通过加热制取甲烷。可用于制取甲烷的发生装置和收集装置为。(从上图中选择,填字母序号,多选或少选不得分)。甲烷点燃后,在火焰上方罩一冷而干燥的玻璃片,会看到有小液滴出现,同时还生成能使澄清的石灰水变浑浊的气体,请写出甲烷燃烧的化学反应方程式。该反应是反应(填化合、分解、氧化)。
-
(6) 工业上常采用分离液态空气的方法获取O2。能说明空气中存在氧气的事例有(写一点即可)。
-
(7) 某些空气净化剂含超氧化钾,其净化原理为:
 。该方法一般不用于实验室制取氧气的原因是(写一点即可)。
。该方法一般不用于实验室制取氧气的原因是(写一点即可)。
【查阅资料】在化学反应过程中,反应前后元素的种类没有改变。
【提出问题】过氧化钠与水反应生成的气体是什么物质?
【作出猜想】猜想Ⅰ:生成氢气;猜想Ⅱ:生成氧气;猜想Ⅲ:生成二氧化碳。
-
(1) 大家经过思考,一致认为猜想Ⅲ不正确,你能试着分析一下理由吗?。
-
(2) 【实验探究】
实验方法
实验现象
实验结论
用试管收集生成的气体,堵住试管口,移近酒精灯火焰,点燃
无现象
猜想不成立
用试管收集生成的气体,将带火星的木条伸入试管内
猜想Ⅱ成立
-
(3) 【拓展延伸】
同学们经查阅资料得知,过氧化钠与水反应时,除了产生气体,还有氢氧化钠生成,试写出该反应的文字表达式。
-
(4) 过氧化钠保存时应注意的一条是。
选项 | 实验内容 | 实验过程 |
A | 二氧化碳的溶解性 | 在充满二氧化碳气体的软塑料瓶中倒入 |
B | 浓盐酸的挥发性 | 打开盛有浓盐酸的细口瓶,瓶口有白雾产生 |
C | 除去CuCl2溶液中的CuSO4 | 加入过量的BaCl2溶液,过滤 |
D | 硫酸铵是一种铵态氮肥 | 硫酸铵样品与熟石灰混合后研磨,有刺激性气味气体生成 |
选项 | 实验目的 | 实验操作 |
A | 分离NaCl和泥沙的固体混合物 | 加足量的水溶解,蒸发 |
B | 配制50g质量分数为6%的NaCl溶液 | 向盛有3 g NaCl固体的烧杯中,加入47mL水(密度为1g/cm3),搅拌至充分溶解 |
C | 鉴别固体(NH4)2SO4和NH4Cl | 分别取样,加熟石灰研磨,闻气味 |
D | 除去二氧化碳中的水蒸气 | 通过装有浓盐酸的洗气瓶 |
物质 | NaOH溶液 | NaCl溶液 | K2CO3溶液 | Ba(NO3)2溶液 |
能否反应 | 能 | 不能 | 能 | 能 |
实验现象 | 无明显现象 | 无明显现象 | 产生气泡 | 产生白色沉淀 |
-
(1) 判断NaOH溶液与稀硫酸能发生反应的依据是生成物中有生成。
-
(2) 【提出问题】对于没有明显现象的反应,如何设计实验进行证明?
【设计实验】在老师的指导下,同学们向少量稀硫酸中逐滴加入过量NaOH溶液,并进行了如下分组实验:
组号
操作
实验现象
结论
1
用pH试纸测定实验前后溶液的pH
pH由1变至9
能反应
2
向反应后的溶液中加入适量Ba(NO3)2溶液
溶液产生白色沉淀
不能反应
3
向反应后的溶液中加入适量K2CO3溶液
能反应
若开始时将pH试纸用蒸馏水润湿。则测得的稀硫酸的pH将(填“偏大”、“偏小”或“不变”)。
-
(3) 请你判断第2小组同学得出的结论是否正确,并说明理由。
-
(4) 第3小组的实验现象为。
-
(5) 【实验结论】对于无明显现象的反应,我们可以分析比较反应物和生成物的性质,从多个角度设计实验进行证明。
【实验反思】向NaOH溶液中通入少量CO2 . 再向其中加入,有气泡产生,即可证明NaOH与CO2发生了反应。
-
(6) 【拓展提升】稀硫酸与NaCl溶液不能发生反应,请你设计实验进行证明(写出实验操作与现象)。
| 实验目的 | 实验操作 | |
| A | 除去硫酸亚铁溶液中少量硫酸铜 | 加过量铁粉充分反应,过滤 |
| B | 检验某固体为碳酸盐 | 取样,滴加稀盐酸,观察是否有气泡产生 |
| C | 除去氯化钠溶液中少量氯化镁 | 加入过量氢氧化钠溶液,过滤,向滤液中加稀盐酸至中性 |
| D | 鉴别氢氧化钠固体和硝酸铵固体 | 取样,加水溶解,观察温度变化 |
- 下列句子排列顺序最恰当的一项是 ( ) ①发思古之幽情 ②不约而同地都把长江奔流视
- 数间民居、一弯流水、挺拔的青松和结伴的人们……以丰子恺漫画为底稿的“中国梦”公益广告,亮相于全国大街小巷,向人们诠释者我
- 下列关于蛋白质的叙述不正确的是() A.蛋白质溶液里加入饱和(NH4)2SO4溶液,蛋白质析出,向析出的蛋白质中加水,蛋
- 正在建设的武汉至宜昌的高速铁路全长约291km,计划2012年建成通车。它的建成将会给沿途经过的仙桃、天门、潜江等市带来
- 已知,,,则三者的大小关系是( ) A. B. C. D.
- 民国时期,初小四年级课本《平等》一文写道:“共和国无阶级之分,人人平等,受治于同一之法律…… 虽以大总统之地位,犹必谨
- 半导体制冷技术是用于电脑元件散热的前沿科技。如图所示是半导体制冷的原理图,图中标有“N”和“P”字样的材料分别叫做N型半
- 二次根式有意义,则x的取值范围是__________________.
- 为测量木块所受摩擦力,可以采用图12中甲、乙所示装置实验: (1)图甲所示装置,木块放在水平面上,右端用手拉弹簧测力计使
- 唐代长安城格局井然、尊卑地位呈现鲜明。宋代开封、临安却没有分隔整齐的坊、市,而是一种街市状态,官府、民户、商家相互混杂。
- 下列有关空气各成分的说法正确的是A.氧气的化学性质很活泼,属于可燃物B.氮气的化学性质不活泼,可用于食品防腐C.空气质量
- 在北宋,人们要在都城购物,必须在规定的东市和西市才能买到东西。以上表述是否正确?请指出并说明理由。___________
- 两千多年前,古罗马哲学家西塞罗说:“谁控制了海洋,谁就控制了世界。”纵观历史,中国近代遭受的第一次来自海上的侵略战争是由
- 下列有关细胞分化、衰老、凋亡与癌变的叙述,正确的是() A.花药离体培养形成植株的过程中
- 曲线在区间上截直线与所得的弦长相等且不为0,则下列描述中正确的是 A
- 已知a,b为不垂直的异面直线,α是一个平面,则a,b在α上的射影有可能是①两条平行直线;②两条互相垂直的直线;③同一条直
- 下列装置中能构成原电池产生电流的是 ()
- 区分唯物史观和唯心史观的分水岭是 A. 是否承认生产力是社会发展的最终决定力量 B. 是否承认阶级斗争是社会发展的动力
- __________the mooncakes are! A. How delicious B.What delic
- 在没有其他光照的情况下,舞台追舞灯发出的红光照在穿白色上衣、蓝色裙子的演员身上,观众看到她( )A.全身呈蓝色B.全身红








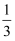 的水,拧紧瓶盖,振荡,塑料瓶迅速变瘪
的水,拧紧瓶盖,振荡,塑料瓶迅速变瘪


