化学方程式的配平 知识点题库
例如:□Al+□MnO2═□Al2O3+□Mn,具体配平步骤如下:
①“标变价”:找出化合价发生改变的元素,并标出改变前后的化合价.
4 +3
+3 ═2
═2 +3
+3
②“列变化”:列出改变的价态数.

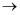
 升高3价
升高3价 
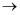
 降低4价
降低4价
③“找倍数”:找出化合价升、降的最小公倍数为3×4=12,从而确定Al、MnO2的系数.
4Al+3MnO2═2Al2O3+3Mn
④“配系数”:再用观察法,配平其它系数.
4Al+3MnO2═2Al2O3+3Mn
根据以上信息,结合已学知识,回答下列问题:
-
(1) HNO3中N的化合价为 价,NO2中N的化合价为 价.
-
(2) 请配平下列化学方程式(系数写在横线上,所有系数都必须填写)
C+ HNO3(浓)═ CO2↑+ NO2↑+ H2O.
北京2008年奥运会火炬“祥云”使用的燃料是丙烷(C3H8),其燃烧的化学方程式为:C3H8+xO2 yCO2+4H2O,其中x、y分别是 ( )
yCO2+4H2O,其中x、y分别是 ( )
在工业上,精炼铜、镀铜以及制取各种铜的化合物时,常用到硫酸铜。某工厂用硫化铜(CuS)生产硫酸铜,提出了以下两个生产方案: 
方案I:硫化铜在硫杆菌的作用下跟空气中的氧气发生反应,生成硫酸铜,反应方程式为:CuS+2O2![]() CuSO4;
CuSO4;
方案Ⅱ:高温煅烧硫化铜,生成氧化铜;氧化铜跟硫酸反碰生成硫酸铜。根据上述信息,请你回答:
-
(1) 在方案I所发生的化学反应中,硫杆菌起作用。
-
(2)
高温煅烧硫化铜的化学反应方程式为2CuS+3O2
 2CuO+2x则x的化学式是。
2CuO+2x则x的化学式是。 -
(3) 上述两个方案中,哪个更合理?并说明理由(最少写出两点)。
 zCO2+nH2O,请你根据方程式的配平方法,试确定化学计量数x、y、z、n是( )
zCO2+nH2O,请你根据方程式的配平方法,试确定化学计量数x、y、z、n是( )
-
(1) C3H8+O2
 CO2+H2O
CO2+H2O
-
(2) NaOH+H2SO4═ Na2SO4+H2O
-
(3) FeS2+O2
 Fe2O3+SO2 .
Fe2O3+SO2 .
-
(1) P+FeO
 P2O5+Fe
P2O5+Fe
-
(2) Fe(红热)+H2O(气)
 Fe3O4+H2
Fe3O4+H2
-
(3)
N2+ H2 =
 NH3
NH3 -
(4) Al+Fe3O4
 Fe+Al2O3
Fe+Al2O3
-
(5) NH3+Cl2N2+HCl
-
(6) C2H2+O2
 CO2+H2O.
CO2+H2O.
-
(1) H2+N2
 NH3
NH3
-
(2) C2H2+O2
 CO2+H2O.
CO2+H2O.
① Fe+Cl2  FeCl3
FeCl3
② CH4+O2  CO2+H2O
CO2+H2O
③ CuSO4+NaOH=Cu(OH)2↓+Na2SO4
④ P+O2  P2O5 .
P2O5 .
-
(1) C3H8+O2
 CO2+ H2O
CO2+ H2O
-
(2) Al(OH)3+H2SO4═ Al2(SO4)3+H2O.
-
(1) Al+O2
 Al2O3
Al2O3
-
(2) C2H6+O2
 H2O+CO2 .
H2O+CO2 .
Fe2O3+CO  Fe+CO2
Fe+CO2
C2H4+O2  CO2+H2O.
CO2+H2O.
C+Fe2O3  Fe+CO2↑
Fe+CO2↑

Ⅰ.将一根长度等于玻璃钟罩最宽部分直径的铁棒横放在钟罩里,把装有稀硝酸的陶罐通过铁钩挂在铁棒上,用绳索将小铁方(铁块的升降通过在钟罩外拉动或放松绳索来实现)。
Ⅱ.调整水槽中初始水位如图乙,再使铁块浸入稀硝酸中,观察到铁块表面迅速产生大量气泡,钟罩内水面下降。[稀硝酸有强氧化性,能与铁发生如下反应:4HNO3+Fe=Fe(NO3)3+NO↑+2H2O]
Ⅲ.当水位降至接近钟罩口时(如图丙),立即取出铁块,以防气体外逸。
IV.等待一段时间后,水面稳定在如图丁的位置。(一氧化氮会与氧气等物质发生如下反应:4NO+3O2+2 ? =4HNO3)
分析与评价:
-
(1) 步骤IV中的“?”处应填 。
-
(2) 从图丙到图丁过程中,钟罩内水位上升的原因是。(忽略温度变化的影响)
-
(3) 小科重复了上述实验,虽实验时装置气密性良好,且钟罩内液面上方气体体积均能精确测量(即测定气体体积的误差忽略不计),但经多次实验测定,发现每次测得空气的含氧量都小于1/5,原因是 。

 2Fe2O3 化合反应
B . Cu+2AgCl=2Ag+CuCl2 置换反应
C . SiO2+3C
2Fe2O3 化合反应
B . Cu+2AgCl=2Ag+CuCl2 置换反应
C . SiO2+3C  SiC+2CO↑置换反应
D . BaCO3+2HCl==BaCl2+H2O+CO2↑复分解反应
SiC+2CO↑置换反应
D . BaCO3+2HCl==BaCl2+H2O+CO2↑复分解反应
 8SO2+2X中的X的化学式是,组成该化学式的两种元素还可以组成另一种黑色固体物质(写化学式).
8SO2+2X中的X的化学式是,组成该化学式的两种元素还可以组成另一种黑色固体物质(写化学式).

-
(1) 地展发生后,搜救过程中,搜救犬能根据人体发出的气味发现幸存者。从微观角度分析,幸存者的某些物质能扩散到搜救犬附近是因为。
-
(2) 如图为地球表面部分板块示意图,据图分析,四川(标★处)是地震高发区的原因是其位于。
-
(3) 84消毒液可用于灾区防疫.制备其主要成分次氯酸钠(NaClO) 的化学方程式为:NaOH+X=NaClO+NaCl+H2O。则X的化学式为。
- 2010年1月,为加强能源战略决策和统筹协调,国务院决定成立 ,国务院总理温家宝出任主任。 A.
- 在下列特称命题中假命题的个数是()①有的实数是无限不循环小数 ②有些三角形不是等腰三角形 ③有的菱形是正方形A.0
- (康熙)十九年,(于成龙)擢直隶巡抚,莅任,戒州县私加火耗①馈遗上官。令既行,道府劾州县,州县即讦道府不得馈遗挟嫌,疏
- 请按“正确”或“不正确”填空: (1)某同学认为多吃蔬菜、水果能补充维生素 ; (2)
- 读我国不同地区景观图,完成23—24题。① ② ③ ④ 23.四幅景观图与所
- “河北醉归,怒斩曹瞒六将;江南赴宴,笑倾鲁肃三杯。”请说出这副对联所称赞的人物,并简述对联中所写的事情。(《三国演义》)
- 今年拟安排财政赤字10500亿元,其中中央财政赤字8500亿元,继续代发地方债2000亿元并纳入地方财政预算。这样的安排
- 西方第一次思想解放运动中的智者运动有重要作用。智者学派研究的核心问题是 A.雅典工商业的发展方向
- 在高额利润的引诱下,假币犯罪很可能死灰复燃。我国现金发行量较大,特别是近几年,现金发行量年均增长23%,这也为制贩假币犯
- 当凸透镜成的像的像距>2f时,以下几种说法错误的是( ) A、2f >u>f B、u>2
- 若x,y满足不等式组,且z=2x+y的最大值是最小值的3倍,则a=() A. B.0 C. D.1
- 阅读下面的文字,完成(13)--(16)题。(17分) 两株玉兰树 陈忠实 清明前一日回到老家,到村子背靠的白鹿原北坡上
- 已知以Rt△ABC的直角边AB为直径作⊙O,与斜边AC交于点D,E为BC边上的中点,连结DE.(1)如图,求证:DE是⊙
- 设集合,集合,若,则实数的取值范围是( ) A、 B、 C、 D、
- 与直线x+2y-1=0关于点(1,-1)对称的直线方程为( )A.2x-y-5=0 B.x+2y
- 如图,已知△ABC是面积为的等边三角形,△ABC∽△ADE,AB=2AD,∠BAD=45°,AC与DE相交于点F,则△A
- 曲线y=x3-x2+5在x=1处的切线的倾斜角是A. B. C.
- 小亮同学想通过实验探究某企业采用的氨碱法制的的纯碱样品的成分及含量。 【提出问题1】该纯碱样品中含有哪些物质? 【猜想与
- Lose one hour in the morning ______ you will be looking for
- 读下图,做题。该图的比例尺属于 A.文字式 B.直线式 C.线段式



