微项目 科学使用含氯消毒剂——运用氧化还原反应原理解决实际问题 知识点题库
-
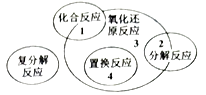
(1) 水是人体的重要组成部分,是人体中含量最多的一种物质.而“四种基本反应类型与氧化还原反应的关系”也可用图1表达.试写出有水参加的符合反应类型Ⅳ的一个化学方程式:,其中水为剂.
-
(2) 过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口.关于双氧水,回答下列问题:
①下列反应中,H2O2既体现氧化性又体现还原性的反应是
A.Na2O2+2HCl═2NaCl+H2O2 B.Ag2O+H2O2═2Ag+O2↑+H2O
C.2H2O2═2H2O+O2↑ D.3H2O2+Cr2(SO4)3+10KOH═2K2CrO4+3K2SO4+8H2O
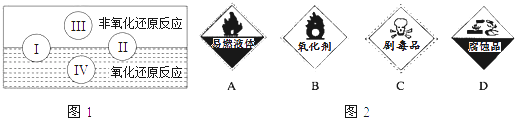
②保存过氧化氢的试剂瓶上最适合贴上的一个标签是图2中(填序号)
-
(3) 焊接铜器时,可先用NH4Cl 除去其表面的氧化铜再进行焊接,该反应可表示为:4CuO+2NH4Cl
 3Cu+CuCl2+N2↑+4H2O
3Cu+CuCl2+N2↑+4H2O ①用双线桥标明电子转移的方向和数目.
②该反应中,被氧化的元素是,氧化剂是.
③还原剂与氧化产物的物质的量之比为.
④反应中若产生0.2mol的氮气,则有 mol的电子转移.
-
(1) 在试管中加入少量三硫代碳酸钠样品,加水溶解,所得溶液pH=10,由此可知H2CS3是酸(填“强”或“弱”)。向该溶液中滴加酸性KMnO4溶液,紫色褪去,由此说明Na2CS3具有性。
-
(2) 为了测定某Na2CS3溶液的浓度,按图装置进行实验。将35.0 mLNa2CS3溶液置于下列装置A的三颈瓶中,打开仪器d的活塞,滴入足量2.0 mol/L稀H2SO4 , 关闭活塞。
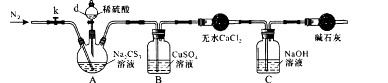
已知:
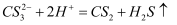 CS2和H2S均有毒:CS2不溶于水,沸点46℃,与CO2某些性质相似,与NaOH作用生成Na2COS2和H2O。
CS2和H2S均有毒:CS2不溶于水,沸点46℃,与CO2某些性质相似,与NaOH作用生成Na2COS2和H2O。①仪器d的名称是。反应开始时需要先通入一段时间N2 , 其作用为。
②B中发生反应的离子方程式是。
③反应结束后打开活塞k,再缓慢通入热N2 一段时间,其目的是。
④为了计算三硫代碳酸铀溶液的浓度,可测定B中生成沉淀的质量。称量B中沉淀质量之前需要进行的实验操作名称是,若B中生成沉淀的质量为8.4g则35.0 mL三硫代碳酸钠溶液的物质的量浓度是。
⑤若反应结束后将通热N2改为通热空气,通过测定C中溶液质量的增加值来计算三硫代碳酸钠溶液的浓度时,计算值<填“偏高”“偏低”或“无影响”)。
 Na2CO3+H2O+CO2↑
C . 4Fe(OH)2+O2+2H2O=4Fe(OH)3
D . CH4+2O2
Na2CO3+H2O+CO2↑
C . 4Fe(OH)2+O2+2H2O=4Fe(OH)3
D . CH4+2O2  CO2+2H2O
CO2+2H2O
-
(1) Ⅰ.工业上常利用电解含有铁、钯、铜等金属的粗银棒精炼银,示意图如下:
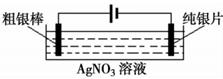
阴极反应式为。
-
(2) 精炼过程中,AgNO3溶液的浓度将(填“增大”、“减小”或“不变”);原因是。
-
(3) Ⅱ.“钯(Pd)金”不仅是优异的催化剂,也是首饰界的新宠。精炼银的过程中钯元素可在电解液中大量富集,因此工业上常利用精炼银的电解液[主要成分为:AgNO3、Pd(NO3)2、Cu(NO3)2、Fe(NO3)3、Ni(NO3)2、HNO3等]为原料生产“钯金”,流程如下:
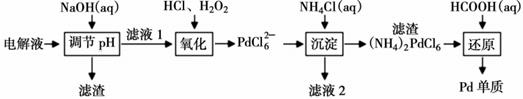
定量实验检测表明,当滤液1中c(Ni2+)=2×10-3mol·L-1时,Pd2+仍没有开始沉淀,计算此时溶液中c(Fe3+)=,(Ksp[Ni(OH)2]=2.0×10-15、Ksp[Fe(OH)3]=4.0×10-38)。
-
(4) “氧化”过程中氧化剂与还原剂的物质的量之比为。
-
(5) 为保证产品的纯净,“沉淀”过程中所得滤渣需要洗涤,简述检验滤渣是否洗净的实验方法。
-
(6) 写出“还原”步骤中发生反应的离子方程式:。
-
(1) I.实验室中有一未知浓度的稀盐酸,某学生在实验室中进行测定盐酸浓度的实验。
配制480mL 0.1000mol·L-1 NaOH 标准溶液。
①配制所需的玻璃仪器有:烧杯、量筒、玻璃棒、、等。
② 称取g氢氧化钠固体所需仪器有天平(带砝码、镊子)、药匙、小烧杯;
-
(2) 取20.00 mL待测稀盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用(填仪器名称)盛装配制的标准NaOH溶液进行滴定。重复上述滴定操作2〜3次,记录数据如下:
滴定次数
待测盐酸
的体积/mL
标准NaOH溶液体积
滴定前的刻度/mL
滴定后的刻度/rnL
第一次
20.00
0.40
20.50
第二次
20.00
4.10
24.00
第三次
20.00
1.00
24.00
-
(3) ①如何判断滴定终点:。
②根据上述数据,可计算出该盐酸的浓度约为mol·L-1。
-
(4) 在上述实验中,下列操作(其他操作正确)会造成测定果偏低的有(填序号)。
A 酸式滴定管使用前,水洗后未用待测盐酸润洗
B 锥形瓶水洗后未干燥
C 称量NaOH固体中混有Na2CO3固体
D 滴定终点读数时俯视读数
E 碱式滴定管尖嘴部分有气泡,滴定后消失
-
(5) II. 氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。测血钙的含量时,进行如下实验:
①可将4mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成CaC2O4沉淀,将沉淀用稀硫酸处理得H2C2O4溶液。
②将①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化产物为CO2 , 还原产物为Mn2+。
③终点时用去20mL l.0×10-4mol/L的KMnO4溶液。
写出H2C2O4溶液与酸性KMnO4溶液反应的离子方程式。
计算:血液中含钙离子的浓度为mol/L。
-
(1) 已知反应:①Cu+2Fe3+=Cu2++2Fe2+ , ②Cu2++Fe=Cu+Fe2+ , 两个反应中各种离子的氧化性从强到弱的顺序是。
-
(2) 用双线桥法标出下列反应中电子转移的方向和数目Cl2+SO2+2H2O=H2SO4+2HCl。并指出氧化剂和还原剂:氧化剂,还原剂:。
-
(3) 已知反应:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。铜与稀硝酸反应的离子方程式是。
-
(4) 下列物质在氧化还原反应中,常作还原剂的有;常作氧化剂的有。(均填序号)
①KMnO4②铝③氯水④FeCl3⑤一氧化碳
-
(1) 常温下,可用氯酸钾固体与浓盐酸反应制备Cl2 , 写出反应的化学方程式,若氧化产物比还原产物多1mol,则被氧化HCl的物质的量为mol。
-
(2) Cl2O为淡棕黄色气体,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为。
-
(3) “有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力,Cl2O的有效氯含量为。(计算结果保留两位小数)

-
(1) K2FeO4中铁元素的化合价为。
-
(2) 制备 K2FeO4需要在(填“酸性”、“碱性”或“中性”)环境中进行。
-
(3) 下列关于K2FeO4的说法中,错误的是。
a.是强氧化性的盐
b.固体保存需要防潮
c.其消毒和净化水的原理相同
d.其净水优点有:作用快、安全性好、无异味
-
(4) 将K2FeO4与水反应的化学方程式补充完整:4K2FeO4+_H2O=_Fe(OH)3(胶体)+ _+ _KOH,。
-
(5) 消毒净化500 m3水,至少需要K2FeO4的质量为kg。
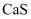 遇酸迅速反应放出
遇酸迅速反应放出 气体,
气体, 和
和 反应生成S和
反应生成S和 。一种烟气脱硫的过程如下:①脱硫:将含
。一种烟气脱硫的过程如下:①脱硫:将含 烟气的空气通过装有
烟气的空气通过装有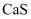 的脱硫塔,加热发生反应
的脱硫塔,加热发生反应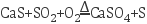 ;②再生:将
;②再生:将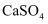 转移到再生塔,加入脱硫煤,高温重新生成
转移到再生塔,加入脱硫煤,高温重新生成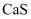 , 并放出
, 并放出 。下列关于
。下列关于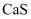 烟气脱硫的说法正确的是( )
烟气脱硫的说法正确的是( )
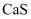 晶胞(如图)中钙离子周围最近的钙离子数为6
B . 脱硫塔中参与反应的还原剂和氧化剂的物质的量之比为
晶胞(如图)中钙离子周围最近的钙离子数为6
B . 脱硫塔中参与反应的还原剂和氧化剂的物质的量之比为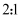 C . 理论上每处理64.0吨
C . 理论上每处理64.0吨 , 将会排放出44.0吨
, 将会排放出44.0吨 D .
D . 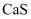 烟气脱硫能减少“温室效应”的形成
烟气脱硫能减少“温室效应”的形成
- 某电场的部分电场线如图所示,A、B是一带电粒子仅在电场力作用下运动轨迹(图中虚线)上的两点,下列说法中正确的是A.粒子一
- 选出成语使用正确的一项: A他们(指白人)的自由和我们(指黑人)的自由是休戚相关的。我们不能单独行动。 B瞿秋白举止
- 在数轴上,点A所表示的实数为3,点B所表示的实数为a,⊙A的半径为2.下列说法中不正确的是( )A.当时,点B在⊙A
- 有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同。下列各项的事实能说明上述观点的是 A.甲苯能
- The bird’ssinging came into our room the window and woke me
- 下图为南半球的一段纬线,图中M、N两点为北半球夏至日晨昏线与该纬线的交点。 读图回答1~3题。1.此时,北京时间为
- 如图所示为水平放置的两个弹簧振子a和b的振动图象,已知两个振子质量之比ma∶mb=2∶3,弹簧的劲度系数之比ka∶kb=
- 小西和小敏放暑假时结伴旅游,他们乘火车从乌鲁木齐出发到呼和浩特旅游,在途中他们能看见的自然景观依次是( ) A.
- 科学家利用催化技术将汽车尾气中的NO和CO转变成C02和N2,以减少对环境的污染,其化学方程式为:2NO +2CO.
- 下图表示某河流随生活污水的流入,其溶解氧量(DO)、生物耗氧量(BOD)、无机物(富含N、P)的浓度变化情况。下列有关叙
- 假定你是李华。你收到了美国笔友彼得寄来的最新英文小说。请给他回信,内容包括: 1.小说收到; 2.回赠礼物; 3.礼物意
- 下列各组物质中,互为同系物的是()。
- The question is_______ he won't listen to anyone. A.that B
- 下列词语中没有错别字的一组是() A.修葺 自负赢亏 河清海晕 言必信,行必
- 下列有关有机化合物的说法中错误的是( ) A.乙醇能使某些蛋白质变性 B.乙烯能发生加成反应、氧化反应及加聚反应等 C
- 下列依据热化学方程式得出的结论正确的是 A.已知2SO2(g)+O2 2SO3(g)
- 下列说法中,正确的是( ) A.由公式可知,在离点电荷非常近的地方(r→0),电场强度E可达无穷大 B.由公式可知负
- 下列叙述中,不能用平衡移动原理解释的是 ( ) A.红棕色的NO2,加压后颜色先变深后变浅 B.高压比常压有利
- 利用一定浓度的秋水仙素处理二倍体水稻,培育出了四倍体水稻新品种。那么利用该四倍体水稻的花粉,通过花药离体培养形成的植株是
- 下列各项中,标点符号使用不合规范的一项是 () A.据搜狐证券统计的创业板财富



