微项目 科学使用含氯消毒剂——运用氧化还原反应原理解决实际问题 知识点题库
下列反应中属于氧化还原反应,且水作为氧化剂的是( )
A . Cl2 + H2O = HCl + HClO
B . 2F2 + 2H2O = 4HF + O2
C . 2Na + 2H2O = 2NaOH + H2↑
D . 2Na2O2 + 2H2O = 4NaOH + O2↑
元素R有如下反应:RO3﹣+5R﹣+6H+═3R2+3H2O,下列说法正确的是( )
A . 元素R位于周期表中第ⅤA族
B . RO3﹣中的R只能被还原
C . R2在常温常压下一定是气体
D . 每反应消耗1molRO3﹣ , 转移电子的物质的量为5mol
三氟化氮(NF3)是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生反应:3NF3+5H2O⇌2NO+HNO3+9HF,下列有关该反应的说法正确的是( )
A . NF3是氧化剂,H2O是还原剂
B . HF是还原产物
C . 还原剂和氧化剂的物质的量之比是2:1
D . NF3在潮湿的空气中泄漏会产生红棕色气体
铜与过量的浓硝酸反应,当有0.2mol硝酸被还原时,参加反应的铜为( )
A . 0.05mol
B . 0.1mol
C . 0.2mol
D . 0.04mol
实验室里通常用MnO2与浓盐酸反应制取氯气,为进行有关氯气的性质实验,需要4瓶容积为100mL的氯气.(常温下,氯气的密度为2.91g/L)
-
(1) 写出制取氯气的离子方程式.
-
(2) 制取4瓶氯气,理论上需要MnO2固体的质量是多少?
-
(3) 制取4瓶氯气,被氧化的HCl的物质的量是多少?
高锰酸钾常用作消毒杀菌、水质净化剂等。某小组用软锰矿(主要含MnO2 , 还含有少量SiO2、Al2O3、Fe2O3等杂质)模拟工业制高锰酸钾流程如下。试回答下列问题。
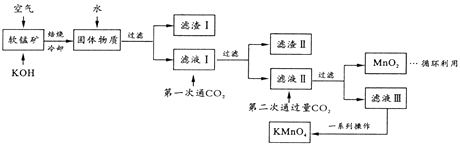
-
(1) 配平焙烧时化学反应: MnO2+ +O2
 K2MnO4+H2O;工业生产中采用对空气加压的方法提高MnO2利用率,试用碰撞理论解释其原因。
K2MnO4+H2O;工业生产中采用对空气加压的方法提高MnO2利用率,试用碰撞理论解释其原因。
-
(2) 滤渣II 的成分有(化学式);第一次通CO2不能用稀盐酸代替的原因是。
-
(3) 第二次通入过量CO2生成MnO2的离子方程式为。
-
(4) 将滤液Ⅲ进行一系列操作得KMnO4。
由下图可知,从滤液Ⅲ得到KMnO4需经过、、洗涤等操作。
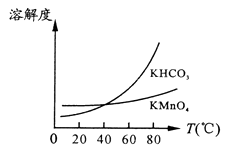
-
(5) 工业上按上述流程连续生产。含MnO2a%的软锰矿1吨,理论上最多可制KMnO4吨。
-
(6) 利用电解法可得到更纯的KMnO4。用惰性电极电解滤液II。
①电解槽阳极反应式为;
②阳极还可能有气体产生,该气体是。
化学与生活密切相关。下列应用中利用了物质氧化性的是()
A . 明矾净化水
B . 铁粉作食品袋内的脱氧剂
C . 食醋除水垢
D . 漂白粉漂白织物
厌氧氨化法(Anammox)是一种新型的氨氮去除技术,下列说法中正确的是
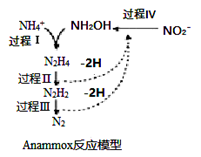
A . 1molNH4+所含的质子总数为10NA
B . 1molNH4+经过过程I、II、III,(假设每步转化均完全)得到氮气的体积约为11.2L
C . 该过程的总反应是:NH4++NO2-=N2↑+2H2O
D . 该方法每处理1molNH4+ , 需要的NO2—为0.5mol
在酸性条件下,黄铁矿(FeS2)催化氧化的反应方程式为2FeS2+7O2+2H2O=2Fe2++4SO42-+4H+ , 实现该反应的物质间转化如图所示。下列分析错误的是( )
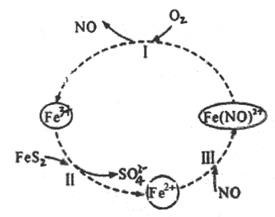
A . 反应Ⅰ的离子方程式为4Fe(NO)2++O2+4H+=4Fe3++4NO+2H2O
B . 反应Ⅱ的氧化剂是Fe3+
C . 反应Ⅲ是氧化还原反应
D . 黄铁矿催化氧化中NO作催化剂
下列反应中铁元素被还原的是( )
A . 2Fe(OH)3  Fe2O3+3H2O
B . Fe+CuSO4=Cu+FeSO4
C . Fe(OH)3+3HCl=FeCl3+3H2O
D . 2Fe2O3+3C
Fe2O3+3H2O
B . Fe+CuSO4=Cu+FeSO4
C . Fe(OH)3+3HCl=FeCl3+3H2O
D . 2Fe2O3+3C  4Fe+3CO2↑
4Fe+3CO2↑
 Fe2O3+3H2O
B . Fe+CuSO4=Cu+FeSO4
C . Fe(OH)3+3HCl=FeCl3+3H2O
D . 2Fe2O3+3C
Fe2O3+3H2O
B . Fe+CuSO4=Cu+FeSO4
C . Fe(OH)3+3HCl=FeCl3+3H2O
D . 2Fe2O3+3C  4Fe+3CO2↑
4Fe+3CO2↑
-
(1) 根据下列化学方程式填空。
①3S+6KOH
 K2SO3+2K2S+3H2O,氧化剂,还原剂;
K2SO3+2K2S+3H2O,氧化剂,还原剂;②2KMnO4+16HCl(浓)=2KCl+2MnCl2+8H2O+5Cl2↑,氧化剂,被氧化的物质。
-
(2) 请把符合要求的化学反应方程式的编号填入括号内:是分解反应又是氧化还原反应的是,是分解反应不是氧化还原反应的是,是化合反应又是氧化还原反应的是,是化合反应不是氧化还原反应的是,不属于四种基本反应类型的氧化还原反应的是。
A.2KClO3
 2KCl+3O2↑
2KCl+3O2↑B.2FeCl2+Cl2
 2FeCl3
2FeCl3C.NH4HCO3
 NH3↑+H2O+CO2↑
NH3↑+H2O+CO2↑D.CaO+CO2=CaCO3
E.Cl2+2NaOH=NaCl+NaClO+H2O
-
(3) 按要求分别用双线桥或单线桥标出下列反应中电子转移的情况。
①3NO2+H2O=2H++2
 +NO(双线桥) 。
+NO(双线桥) 。②8NH3+6NO2
 7N2+12H2O(单线桥) 。
7N2+12H2O(单线桥) 。
下列实验操作对应的现象和根据现象得出的结论均正确的是 ( )
| 实验操作 | 现象 | 结论 | |
| A | 向FeCl3溶液中加入浓NaOH溶液 | 溶液由黄色变为红棕色 | 生成了氢氧化铁胶体 |
| B | 向Co2O3中滴入浓盐酸加热 | 产生黄绿色气体 | 氧化性:Cl2>Co2O3 |
| C | 向某溶液中滴加K3[Fe(CN)6]溶液 | 产生蓝色沉淀 | 溶液中存在亚铁离子 |
| D | 向NaHCO3溶液中滴加NaAlO2溶液 | 有白色沉淀和气体产生 | AlO2-与HCO3-发生了水解的相互促进 |
A . A
B . B
C . C
D . D
现有20mL浓度为0.04mol/L的Na2SO3溶液恰好与10mL浓度为0.02mol/L的K2A2O7溶液完全反应。已知Na2SO3可被K2A2O7氧化为Na2SO4 , 则元素A在还原产物中的化合价为( )
A . +2
B . +3
C . +4
D . +5
下列叙述正确的是( )
A . 在化学反应中,得电子越多的氧化剂,其氧化性就越强
B . 元素的单质一定是通过氧化或还原该元素的化合物制得的
C . 阳离子只能得电子被还原,阴离子只能失电子被氧化
D . 含有最低价元素的化合物不一定具有很强的还原性
NaCl是一种化工原料,可以制备一系列物质(见图)。下列说法正确的是( )
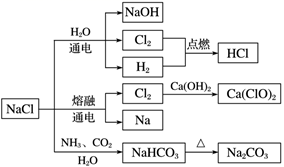
A . 25 ℃时,NaHCO3在水中的溶解度比Na2CO3的大
B . 石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂
C . 常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应
D . 如图所示转化反应不都是氧化还原反应
某同学通过如下流程制备氧化亚铜:
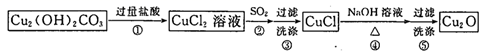
已知:CuCl难溶于水和稀硫酸;Cu2O+2H+=Cu2++Cu+H2O。下列说法错误的是( )
A . 步骤②中,SO2为还原剂,将CuCl2还原为CuCl
B . 步骤③中为防止CuCl被氧化,可用H2SO3水溶液洗涤
C . 步骤④发生反应的离子方程式为2CuCl+2OH-=Cu2O+2Cl-+H2O
D . 得到的Cu2O试样中可能会混有CuCl杂质,可通过加足量稀硫酸充分溶解过滤后分离除去
氧化还原反应广泛存在于生产和生活中,下列不属于氧化还原反应的是( )
A . 燃料的燃烧
B . 食物的腐败
C . 水滴石穿
D . 钢铁的锈蚀
下图是一种处理废锌锰干电池的流程,电池内除铜帽、锌皮(含少量铁)、石墨棒外,还含有MnOOH、ZnCl2、NH4Cl、C及有机物等糊状填充物。
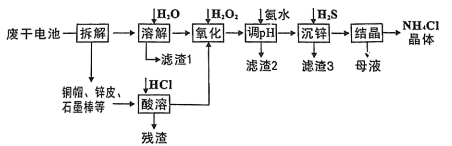
回答下列问题:
-
(1) “溶解”过程中为了提高浸出效率,可以采取的措施有;(写一条即可)
-
(2) 将“滤渣1”灼烧有
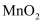 生成,产生
生成,产生 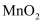 的化学方程式为;
的化学方程式为;
-
(3) “氧化”过程中,还原产物是;
-
(4) “滤渣2”的主要成分是;
-
(5) “调pH”时,应控制溶液pH的范围是;(已知:“溶解”后的溶液中c(Zn2+)=0.10mol/L,忽略滴加
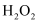 、氨水后溶液的体积变化;Ksp[Zn(OH)2]=10-17 , Ksp[Fe(OH)2]=10-17 , Ksp[Fe(OH)3]=10-38.3)
、氨水后溶液的体积变化;Ksp[Zn(OH)2]=10-17 , Ksp[Fe(OH)2]=10-17 , Ksp[Fe(OH)3]=10-38.3)
-
(6) 写出“沉锌”的离子方程式;
-
(7) 测定NH4Cl晶体中的氮元素含量:准确称取样品0.100g放至锥形瓶中,加适量的水完全溶解,再加5mL中性甲醛溶液(足量),摇匀,静置,用0.100mol/L的NaOH标准溶液平行滴定三次,消耗标准溶液的平均体积为18.50mL,则样品中氮元素的质量分数为。
[已知:4
 +6HCHO=(CH2)6N4H++3H++6H2O;(CH2)6N4H++3H++4OH-=(CH2)6N4+4H2O]
+6HCHO=(CH2)6N4H++3H++6H2O;(CH2)6N4H++3H++4OH-=(CH2)6N4+4H2O]
陈述Ⅰ和Ⅱ均正确但不具有因果关系的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 用焦炭和石英砂制取粗硅 | |
| B | 利用海水制取溴和镁单质 | |
| C | 石油裂解气能使溴的 | 石油裂解可得到乙烯等不饱和烃 |
| D | | |
A . A
B . B
C . C
D . D
下列物质中的硫元素不能表现出氧化性的是( )
A . S
B . Na2S
C . SO2
D . H2SO4
最近更新
- 某种植物病毒V是通过稻飞虱吸食水稻汁液在水稻间传播的。稻田中青蛙数量的增加可减少该病毒在水稻间的传播。下列叙述正确的是(
- 如图所示,一轻绳上端固定,下端系一个质量为m的小球.现对小球施加一个F=mg的水平拉力,使小球偏离竖直位置并保持静止,则
- (6分)(1)欲将80 g质量分数为20%的NaOH溶液稀释到质量分数为10%NaOH溶液 ,需要加水的质量为
- 如图所示,电路与一绝热密闭气缸相连,Ra为电阻丝,电源有内阻,气缸内有一定质量的理想气体,电键S闭合,现将变阻器的滑动片
- You’re sitting in the car, stuck(无法离开的) in traffic. You’re g
- 下列各组物质中,能用溴水或高锰酸钾溶液鉴别的是 A.乙烷、乙烯 B.乙炔、丙烯
- 如图所示,在绝缘的斜面上方存在着沿水平向右的匀强电场,斜面上的带电金属块沿斜面滑下,已知在金属块滑下的过程中动能增加了1
- 在下面横线处填写相关语句。(8分,每空2分) (1)三顾频烦天下计, __________。(杜甫《蜀相》) (2)__
- 除去下列各组物质中的杂质,所用试剂和方法均正确的是( )物质 杂质 除杂所用的试剂和方法 A CaO固体 CaC
- 目前,正在制定“十二五”规划的深圳,同时布局生物、新能源、互联网、新材料、文化创意等五大战略性新兴产业。为促进这些产业发
- 依次填入下面句子横线处的词语最恰当的一项是( ) (2分) 生活中,面对别人的困难,有的人总是一副____的姿态
- 下列说法正确的是A.没有光纤就没有互联网,光纤的主要成分是硅B.碳酸钠具有碱性,医疗上可用来治疗胃酸过多C.煤气化技术
- 若、均为锐角,且,,则 .
- 设集合,则A. B. C. D.
- 炼铁的还原剂CO是由焦炭和CO2反应而得。现将焦炭和CO2放入体积为2L的密闭容器中,高温下进行下列反应:C(s)+CO
- 22. 下列关于生物学实验的描述正确的是 A.观察细胞质流动时,换用高倍镜后视野会变暗,这时应该使用较大光圈或换平面镜采
- 如果60m表示“向北走60m”,那么“向南走40m”可以表示为【 】A.-20m B.-40m
- 阅读文言文,完成第10~14题。(10分)魏绛谏悼公伐诸戎①五年②,无终子嘉父③僮孟乐④因魏庄子⑤纳虎豹之皮以和诸戎。公
- (6分)773 K、固定体积的容器中,反应CO(g)+2H2(g)CH3OH(g)过程中能量变化如下图。曲线Ⅱ表示使用催
 可制作光导纤维
可制作光导纤维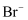 可被氧化,
可被氧化,  可被还原
可被还原 溶液褪色
溶液褪色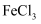 水解可生成
水解可生成 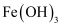 胶体
胶体


