微项目 科学使用含氯消毒剂——运用氧化还原反应原理解决实际问题 知识点题库
下列变化中,需加氧化剂才能实现的是( )
A . NaClO →NaCl
B . FeCl3 →FeCl2
C . C → CO2
D . CaO→Ca(OH)2
氧化还原反应与四种基本反应类型的关系如图所示,下列化学反应中不属于区域3的化学反应是( )
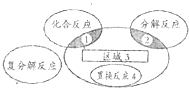
A . Br2+SO2+2H2O═H2SO4+2HBr
B . CuO+CO  Cu+CO2
C . 4NH3+5O2═4NO+6H2O
D . 3Fe+4H2O(g)
Cu+CO2
C . 4NH3+5O2═4NO+6H2O
D . 3Fe+4H2O(g)  Fe3O4+4H2
Fe3O4+4H2
 Cu+CO2
C . 4NH3+5O2═4NO+6H2O
D . 3Fe+4H2O(g)
Cu+CO2
C . 4NH3+5O2═4NO+6H2O
D . 3Fe+4H2O(g)  Fe3O4+4H2
Fe3O4+4H2
已知M2O7x﹣+3S 2﹣+14H+=2M3++3S↓+7H2O,则M2O7x﹣中的M的化合价为( )
A . +2价
B . +3价
C . +4价
D . +6价
反应3Cl2+8NH3=6NH4Cl+N2常用于判断氯气管道是否漏气,关于该反应的说法正确的是( )
A . Cl2发生氧化反应
B . NH3是还原剂
C . 每生成1 mol N2 , 转移3 mol电子
D . 被氧化与未被氧化的NH3物质的量之比为1:3
Cu与一定浓度的硝酸反应时,其方程式可表示为:Cu+HNO3→Cu(NO3)2+NO↑+NO2↑+H2O
-
(1) 硝酸在反应中体现了性和性;
-
(2) 0.3mol Cu被完全溶解后,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是多少?该NO和NO2混合气体的平均相对分子质量是多少?
下列说法正确的是( )
A . 元素从化合态变为游离态,一定是被还原
B . 在标准状况下,水、氧气和氮气分子间的平均距离都相等
C . 0.5 mol·L−1的 MgCl2溶液中Cl−的数目为6.02×1023
D . 6.4g S2和S8的混合物,所含的硫原子数一定为1. 204×1023
已知:5PbO2+2Mn2++4H+=5Pb2++2MnO4- +2H2O,下列说法正确的是( )
A . PbO2 为还原剂,具有还原性
B . 氧化产物与还原产物的物质的量之比为 5∶2
C . 生成 1 mol 的 Pb2+ , 转移的电子数为 5 mol
D . 酸性环境下 PbO2 的氧化性强于 MnO4-
氧化还原反应的本质是。在反应
MnO2+4HCl(浓)→MnCl2+2H2O+Cl2↑中,元素化 合价升高,被(填“氧化”或“还原”),发生(填“氧化”或“还原”)反应,还原剂是。元素化合价降低,被(填“氧化”或“还原),发生(填”氧化“或”还原“)反应,氧化剂是。
如图中的每一方框内表示一种反应物或生成物,其中A,C,D,E,F 在通常情况下均为气体,且A 与 C 物质的量之比为 1:1,B 为常见液体,F 为红棕色气体。
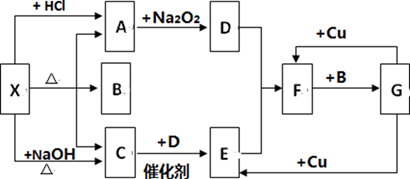
试回答下列问题:
-
(1) X 是;F 是。(写化学式)
-
(2) 写出 G→E 反应的化学方程式并用双线桥标出电子转移的方向和数目。
-
(3) G 与 Cu 的反应中,G 表现性质。
-
(4) 写出X→A 的离子方程式:。
-
(5) 以 C、B、D 为原料可生产 G,若使 amolC 的中心原子完全转化到 G 中,理论上至少需要 Dmol。
氨的催化氧化是工业制硝酸的重要反应:4NH3+5O2 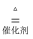 4NO+6H2O,对于该反应判断正确的是( )
4NO+6H2O,对于该反应判断正确的是( )
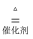 4NO+6H2O,对于该反应判断正确的是( )
4NO+6H2O,对于该反应判断正确的是( )
A . 氧气被还原
B . 该反应是置换反应
C . 氨气是氧化剂
D . 若有17 g氨参加反应,反应中转移10 mol电子
酸性溶液中离子还原性强弱顺序为 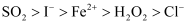 ,则下列反应不可能发生的是( )
,则下列反应不可能发生的是( )
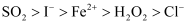 ,则下列反应不可能发生的是( )
,则下列反应不可能发生的是( )
A . 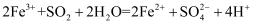 B .
B . 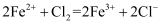 C .
C .  D .
D . 
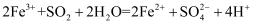 B .
B . 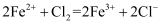 C .
C .  D .
D . 
按要求填空:
-
(1) 已知NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。
①上述反应中氧化剂是(填化学式,下同),还原产物是,若反应中生成的气体在标准状况下的体积是2.24L,则反应中转移的电子数。
②根据上述反应,鉴别NaNO2和NaCl。可选用的物质有:①水、②碘化钾淀粉试纸、③淀粉、④白酒、⑤食醋,你认为必须选用的物质有(填序号)。
-
(2) 实验室用二氧化锰和浓盐酸反应制取氯气,
①写出该反应的化学方程式
②用(填名称)除去氯气中的杂质氯化氢气体,用(填化学式)溶液吸收尾气,
③足量的二氧化锰与40mL10 mol·L-1的浓盐酸充分反应,收集到的氯气在标准状况下的体积2.24L(填“大于”“等于”或“小于”)。
下列反应不属于四种基本反应类型,但属于氧化还原反应的是( )
A . Fe+CuSO4=FeSO4+Cu
B . AgNO3+NaCl=AgCl↓+NaNO3
C . Fe2O3+3CO 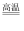 2Fe+3CO2
D . 2KMnO4
2Fe+3CO2
D . 2KMnO4  K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
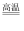 2Fe+3CO2
D . 2KMnO4
2Fe+3CO2
D . 2KMnO4  K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
以下反应①②可用于从不同原料中提取碘:
① 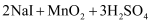
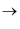
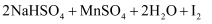
② 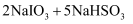
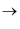
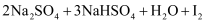
-
(1) 反应①中的氧化剂是,在该反应中发生氧化反应;反应
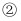 中的还原产物是。每生成
中的还原产物是。每生成 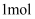 还原产物,将有mol电子发生转移。
还原产物,将有mol电子发生转移。
-
(2) 根据反应①②可推知。
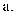 氧化性
氧化性 
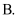 氧化性:
氧化性: 
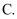 还原性:
还原性: 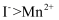
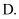 还原性:
还原性: 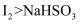
某温度下将Cl2通入KOH溶液里,反应后得到KCl、KClO、KClO3的混合溶液,其中ClO-与ClO  的个数比为11∶1,则Cl2与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为( )
的个数比为11∶1,则Cl2与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为( )
 的个数比为11∶1,则Cl2与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为( )
的个数比为11∶1,则Cl2与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为( )
A . 1∶3
B . 4∶3
C . 2∶1
D . 3∶1
吸进人体内的氧有2%转化为氧化性极强的活性氧,活性氧能加速人体衰老,被称为“生命杀手”,中国科学家尝试用Na2SeO3清除人体内的活性氧,则Na2SeO3的作用是( )
A . 还原剂
B . 氧化剂
C . 既是氧化剂又是还原剂
D . 以上均不是
-
(1) 写出H2O2在二氧化锰作催化剂的条件下分解的方程式,并在方程式上用双线桥法标出电子转移的方向和数目取少量H2O2于试管中,滴加FeCl2溶液,立即生成红褐色沉淀,配平下列反应的离子方程式:_H2O2 +_Fe2++_OH-=_Fe(OH)3 , ,该反应中H2O2表现了性(填“氧化”或“还原”)。
-
(2) 工业制CuSO4时,不是直接用铜跟浓硫酸在加热条件下反应,而是将铜丝浸入稀硫酸中,再不断由容器下部吹入细小的空气泡。
写出所发生反应的化学方程式
-
(3) 这样做的好处是①②
-
(4) 实验室常用浓硝酸与铜反应制备二氧化氮,离子方程式是。若有1.5molCu参加反应,则mol硝酸作氧化剂,转移 mol电子
钴是一种中等活泼金属,化合价为+2价和+3价,其中CoCl2易溶于水。某校同学设计实验制取(CH3COO)2Co(乙酸钴)并验证其分解产物。回答下列问题:
-
(1) I.甲同学用Co2O3与盐酸反应制备CoCl2·4H2O,其实验装置如图:
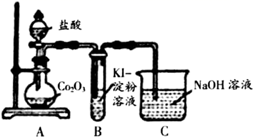
①烧瓶中发生反应的氧化剂和还原剂的物质的量之比为。
②装置B中的现象可以说明氧化性>,从原子结构的角度解释。
-
(2) II.乙同学利用甲同学制得的CoCl2·4H2O在醋酸氛围中制得无水(CH3COO)2Co,并利用下列装置检验(CH2COO)2Co在氮气气氛中的分解产物。已知PdCl2溶液能被CO还原为Pd。
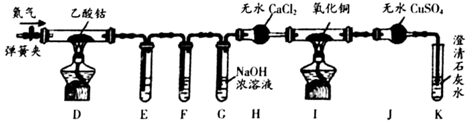
①装置E、F分别盛放和。
②E、F、G中的试剂均足量,观察到I中氧化铜变红,J中固体由白色变蓝色,K中石灰水变浑浊,则可得出的结论是。
③通入氮气的作用是。
某兴趣小组利用下列装置制得了纯度高的NaClO溶液。
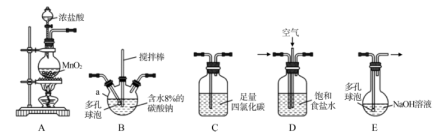
已知:Cl2O是棕黄色气体,是HClO的酸酐,沸点约3.8 ℃,42 ℃以上分解生成Cl2和O2。通入的空气不参与化学反应。回答下列问题:
-
(1) 装置的连接顺序是A→ →→C→,Cl2O 和Cl2在CCl4中的溶解度较大的是。
-
(2) 装置A中发生反应的离子方程式为 ,D 的作用是,E中发生的化学反应方程式为。
-
(3) 实验时装置B应置于水浴中加热,其水浴温度应 , 实验开始后观察到B中有大量的棕黄色气体产生,B中反应的离子方程式为。
-
(4) 测定所制得的次氯酸钠的物质的量浓度:量取10.0mL实验制得的次氯酸钠溶液,并稀释至100 mL,再从其中取出10. 00 mL于锥形瓶中,加入10. 00 mL 0. 5000 mol/L的Na2SO3溶液,充分反应后,用0.1000 mol/L碘水滴定过量Na2SO3溶液至终点,平行滴定三次,消耗碘水溶液平均体积20.00mL,滴定时所选指示剂是,终点时的现象为,所制得次氯酸钠溶液的浓度为(氧化性:ClO- >
 , 还原性:
, 还原性: >I- )。
>I- )。
宋代著名法医学家宋慈的《洗冤集录》中有银针验毒的记载,“银针验毒”的原理 , 下列说法正确的是( )
, 下列说法正确的是( )
 , 下列说法正确的是( )
, 下列说法正确的是( )
A . X的化学式为AgS
B . 反应中 是还原产物
C . 银针验毒时,空气中氧气失去电子
D . 反应中Ag和
是还原产物
C . 银针验毒时,空气中氧气失去电子
D . 反应中Ag和 均是还原剂
均是还原剂
 是还原产物
C . 银针验毒时,空气中氧气失去电子
D . 反应中Ag和
是还原产物
C . 银针验毒时,空气中氧气失去电子
D . 反应中Ag和 均是还原剂
均是还原剂
最近更新
- 的相反数是__▲__.
- 一位时装店经理不小心将一条高档呢裙烧了一个小洞,该裙无人问津。按说,请一名技艺高超的师傅把洞补上就行了,但该经理却反其道
- 对于一只生活在田野里的蝗虫来说,它的环境是指 (A)田野中的植物和蛇、蛙等动物 (B)除蝗虫外的其他生物和非生物 (C)
- One day I walked down to get tomy car, thinking about what I
- 进入血液的氧,通过血液循环输送到全身各处的组织细胞内的什么部位被利用?( ) A.细胞核 B.细胞质 C.叶绿体
- . 图①示限制酶切割某生物DNA分子的过程;图②表示该生物体细胞部分基因和染色体的关系;该生物的黑色素产生需要如图③所示
- 1米长的小棒,第1次截去一半,第二次截去剩下的一半,如此截下去,第4次后剩下的小棒长________米.
- 与唐前期实行的租庸调制相比,唐中期实行的两税法的主要特点是 ( ) A.保证了农民生产时间
- “橄榄型”收入分配格局的特征是,中等收入者占多数,扶贫对象大幅减少,绝对贫困现象基本消除,低收入者和高收入者均占少数,呈
- 下列词语中加点字读音完全相同的一组是 A.沏茶 栖息 休戚相关 期期艾艾 B.余暇 裴葭
- 向10mL一定物质的量浓度的盐酸中滴加一定物质的量浓度的NaOH溶液,其pH变化如右图所示,则两溶液的物质的量浓度分别是
- 下图是1949〜2008年中国与外国建交情况曲线图。在下列各项中,建交最高峰出现的主要原因是 A.“大跃进”的政治
- It is not until May, 2013 the online consultation comes
- 某九级(2)班的四名同学在学习了《俄国十月革命》后对其进行了评价,其中下列中评价错误的是 A.甲说:这是人类第一次获胜的
- (16分)航空母舰上的飞机弹射系统可以减短战机起跑的位移,假设弹射系统对战机作用了0.1s时间后,可以使战机达到一定的初
- ①自20世纪60年代初,现代工业机器人“尤尼曼特”和“沃莎特兰”在美国诞生以来,至20世纪70年代,工业机器人在世
- 从唯物辩证法度看,“顾“钱”不顾后”的看法 A.没有做到实事求是 B.割裂了事物的联系 C.混淆了主观与客观
- I ____ toward the door to go outsidewhen suddenly Jim opened
- I’m a 20-year-old boy, and the following is my story. A mont
- At last, we found ourselves in a pleasant park with trees pr



