微项目 科学使用含氯消毒剂——运用氧化还原反应原理解决实际问题 知识点题库
你认为甲实验的操作和现象是。振荡后出现的蓝色主要与有关(填写化学式,下同);蓝色消失又与有关。
高锰酸钾是锰的重要化合物和常用的氧化剂.以下是工业上用软锰矿(主要成分MnO2)制备高锰酸钾的一种工艺流程.
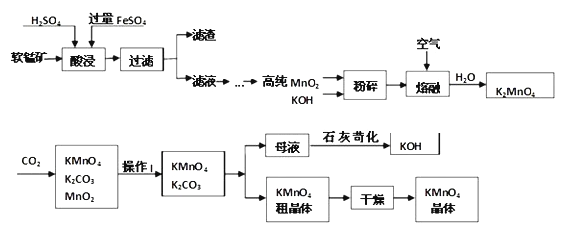
请回答:
(1)KMnO4稀溶液是一种常用的消毒剂.其消毒机理与 (填字母)相同.
a.NaClO溶液 b.乙醛 c.双氧水 d.75%的酒精
(2)操作Ⅰ的名称是 ;硫酸亚铁在酸性条件下将MnO2还原为MnSO4 , 酸浸时发生主要反应的化学方程式为
(3)上述流程中可以循环使用的物质有 KOH 和 MnO2 (填化学式).若不考虑物质循环与制备过程中的损失,则1mol MnO2可制得 mol KMnO4 .
(4)MnO2在酸性条件下具有强氧化性,可被还原为Mn2+ . 写出MnO2与浓盐酸制取氯气的化学方程式
为验证MnO2具有强氧化性,下列方案可行的是 (填字母)
A.MnO2固体加入到FeCl3溶液中,再加KSCN溶液,观察溶液是否变红
B.MnO2固体加入到Na2SO3溶液中,再加BaCl2溶液,观察是否有白色沉淀生成
C.MnO2固体加入到FeSO4与KSCN的酸性混合液中,观察溶液是否变红
(5)酸性KMnO4与H2C2O4溶液反应,反应开始时溶液褪色较慢,反应一段时间后褪色会迅速加快,其原因是
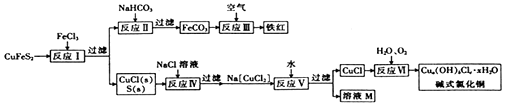
已知:a、b、c、x均为整数。
-
(1) 该流程需进行多次过滤,过滤时用到的玻璃仪器为、和。
-
(2) 反应Ⅰ的离子方程式为,该反应的还原剂是(填化学式,下同),氧化产物是。
-
(3) 反应Ⅱ 的离子方程式为。
-
(4) 反应Ⅵ是在45~50℃的条件下进行的,该反应中氧化剂与还原剂的物质的量之比为。
-
(5) 为测定制得的碱式氯化铜的组成,某实验小组进行下列实验:
①称取样品9.30g,用少量稀HNO3 溶解后配成100.00 mL溶液A;
②取25.00mL溶液A,加入足量AgNO3溶液,得到AgCl 固体1.435 g;
③另取25.00mL溶液A,调节pH为4~5,用浓度为0.40mol·L-1的EDTA(Na2H2Y·2H2O)标准溶液滴定Cu2+ (离子方程式为Cu2++H2Y2-=CuY2-+2H+),滴定至终点,消耗标准溶液50.00 mL。通过计算确定该样品的化学式为(填化学式)。
-
(1) 写出丙烷的结构简式:。
-
(2) 写出亚硫酸钠在空气中被氧化的化学方程式:
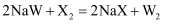 ;
; 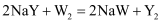 ;
;  。由此得出结论正确的是( )
。由此得出结论正确的是( )
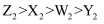 B . 还原性:
B . 还原性:  C .
C . 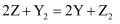 D . X-、Y-、Z-、W-中Z-还原性最强
D . X-、Y-、Z-、W-中Z-还原性最强
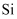 D . 嫦娥五号带回的月壤中含铬、钠、镁、铜等元素,这些金属均可以用热还原法冶炼
D . 嫦娥五号带回的月壤中含铬、钠、镁、铜等元素,这些金属均可以用热还原法冶炼
- 下列事实不能用分子观点解释的是 A.柳絮纷飞 B.给轮胎打气时气体被压缩 C.花香四溢 D.1滴
- 在我国,股份有限公司和有限责任公司的主要区别在于( ) A.股东是否以货币出资 B.股东是否
- 下列关于1889年《日本帝国宪法》的表述,不正确的是 A.由伊藤博文起草 B.天皇权力受议会限制 C.国家主权掌握在天皇
- 如图,是两根柱子在同一灯光下的影子.(1)请在图中画出光源的位置(用点P表示光源);(2)在图中画出人物DE在此光源下的
- 请以“放慢脚步”为题,写一篇文章。(60分) 要求:(1)认真思考题目含义,选择恰当的角度:(2)除诗歌外,文体不限
- 18.阅读下面的文字,根据要求作文。 (60分) 北大教授、著名作家曹文轩曾说过,生活中不只是些有意义的事,还有很
- 阅读分析下列材料并回答问题。 目前,土地退化是我国面临的生态环境问题之一。其中土地荒漠化面积已达267.4万平方
- —It is reported in the local newspaper that the murderer was
- 金属-空气电池是以金属为燃料,与空气中的氧气发生氧化还原反应产生电能的一种特殊燃 料电池。如图为钠-空气电池的装置示意图
- 如下图各装置中均盛有海水,铁在其中被腐蚀由快到慢的顺序正确的是( )A.②>①>③ B.①>②>③
- 题23图关于细胞核中染色体、DNA、基因三者间包含关系的表述,其中正确的是:
- 1929──1933年资本主义经济危机的根源是 ( ) A.资本主义社会的基
- 加点的成语使用正确的一项是( ) A.我们该有鹏举鸿飞的豪情,鱼游濠水的自在,同时拥有温暖安稳的家园,还有足以自豪
- 2222222222222222222222222222222
- 使用普通光学显微镜观察水中微生物,若发现视野中微生物如图1所示方向游走,请问应该把载玻片向图2所示的哪个方向移动 (
- 若直线l1:ax+2y+6=0与直线l2:x+(a﹣1)y+(a2﹣1)=0平行则实数a=.
- ______, they would certainly come and help us. A. Had they t
- 写出下列程序的运行结果.(1)a=5;b=3;c=(a+b)/2;print(% io(2),c);输出结果为_____
- 日常生活中的下列变化,属于物理变化的是( ) A.木柴燃烧 B.冰雪融化 C.钢铁生锈 D.食物变质
- 史书记载,秦孝公死后,太子即位。守旧的贵族诬告商鞅“谋反”,结果商鞅被处死。这突出地说明,商鞅变法( ) A.没有改



