第3节 氧化还原反应 知识点题库
-
(1) 氢化钠(NaH)中氢元素的化合价为.
-
(2) NaH能与水反应制氢气:NaH+H2O=NaOH+H2↑,该反应的氧化剂是.若12g NaH与水反应,转移电子的数目为.请写出实验室制氢气的化学方程式并标出电子转移的方向和数目.
-
(1) 请配平方程式,并用双线桥表示得失电子情况:
KClO3+HCl(浓)=KCl+ClO2↑+Cl2↑+H2O
-
(2) 氧化剂是,还原产物是(写化学式).
-
(3) 产生0.1molCl2时,转移电子的物质的量为 mol.
①SeO2+4KI+4HNO3=Se+2I2+4KNO3+2H2O;②Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O
下列有关叙述正确的是( )
【资料】 | 溴水是溴单质的水溶液,因溶有溴单质而呈黄色; 溶有溴的 |
根据已有化学知识及资料,请你参与上述现象形成原因的分析与探究:
【提出问题猜想】:
猜想①:溶液呈黄色是因为 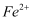 被氧化成
被氧化成  所致:
所致:
猜想②:溶液呈黄色是因为 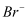 被氧化成
被氧化成  所致。
所致。
-
(1) 【设计实验并验证】
为验证①与②中是哪个原因导致了溶液变黄色,设计并进行了以下实验。请根据以下所给试剂,进行合理选用,完成实验方案1和方案2:
试剂
酚酞试液、
 、无水酒精、
、无水酒精、 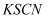 溶液
溶液方案
操作步骤
实验现象
结论
①
取所述黄色溶液于试管中,滴加并振荡
溶液变红色
猜想①正确
②
取所述黄色溶液于试管中,滴加并振荡
-
(2) 实验结论:以上实验不仅验证了溶液变黄的真实原因,同时证明了
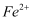 的还原性比
的还原性比 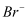 (填“强”或“弱”)。
(填“强”或“弱”)。
-
(3) 【实验反思】
根据上述实验推测,若在溴化亚铁溶液中滴入足量氯水,再加入
 并充分振荡后静置,观察到的现象是。
并充分振荡后静置,观察到的现象是。
①混合物:氯水、氨水、水玻璃、水银、福尔马林、淀粉
②含有氧元素的化合物叫氧化物
③CO2、NO、P2O5均为酸性氧化物,Na2O、Na2O2均为碱性氧化物
④同位素:1H+、2H2、3H
⑤同素异形体:C60、C80、金刚石、石墨
⑥浓盐酸、浓硫酸、浓硝酸均具有氧化性,都属于氧化性酸
⑦化合物:烧碱、冰醋酸、HD、聚氯乙烯
⑧强电解质溶液的导电能力一定强
⑨在熔化状态下能导电的化合物为离子化合物
⑩有单质参加的反应或有单质产生的反应是氧化还原反应
 2BN(s)+3H2O(g)反应制得,实际中还添加Ca3(PO4)2作为填料,以降低B2O3熔体的黏度。下列有关说法正确的是( )
2BN(s)+3H2O(g)反应制得,实际中还添加Ca3(PO4)2作为填料,以降低B2O3熔体的黏度。下列有关说法正确的是( )
 Na2CO3+H2O+CO2↑
C . Cl2+2NaOH=NaCl+NaClO+H2O
D . NaBr+AgNO3=AgBr↓+NaNO3
Na2CO3+H2O+CO2↑
C . Cl2+2NaOH=NaCl+NaClO+H2O
D . NaBr+AgNO3=AgBr↓+NaNO3
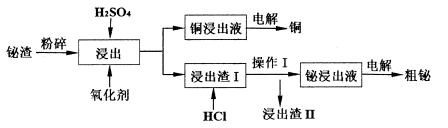
已知:Sb2O3难溶于H2SO4;Bi2Oз+2H2SO4=2Bi(OH)SO4↓+H2O。
回答下列问题:
-
(1) “粉碎”的目的是。
-
(2) ①若氧化剂为H2O2 , 溶解Cu2O反应的离子方程式为;
②温度对铜浸出率的影响如图所示。
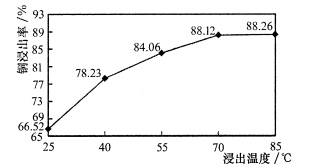
工业浸出时一般选择70℃~80℃,温度过低时铜浸出率低的原因是;
-
(3) “操作I”为减压过滤。与常压过滤比较,其优点是;
-
(4) ①“浸出渣II”的主要成分是SbOCl、;
②写出SbCl3水解生成SbOCl的化学方程式:;
-
(5) “铜浸出液”用如图旋流式电解装置电解。
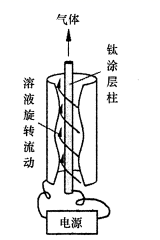
①钛涂层柱的电极反应式是;
②若“铜浸出液”中含铜92.16g·L-1 , 选择合适条件进行旋流电解。取电解后溶液25.00mL,加入足量KI溶液充分反应,以淀粉为指示剂,用0.1000mol·L-1的标准液Na2S2O3滴定,反应为:2Cu2++4I-=2CuI↓+I2、I2+2
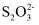 =2I-+
=2I-+ 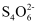 ,消耗18.00mL标准液。旋流电解铜回收率是。(用质量分数表示,保留一位小数)。
,消耗18.00mL标准液。旋流电解铜回收率是。(用质量分数表示,保留一位小数)。
 稀溶液冲洗
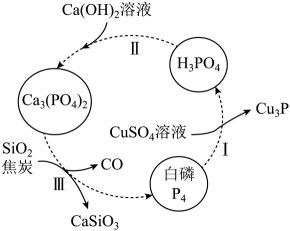
B . 过程I中氧化产物和还原产物的物质的量之比为5∶6
C . 过程II中,除生成
稀溶液冲洗
B . 过程I中氧化产物和还原产物的物质的量之比为5∶6
C . 过程II中,除生成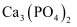 外,还可能生成
外,还可能生成 、
、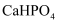 D . 过程III的化学方程式为
D . 过程III的化学方程式为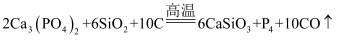
- 在制果酒、果醋、泡菜、腐乳时,所用微生物的代谢类型分别是 A.兼性厌氧型、需氧型、厌氧型、需氧型 B.厌氧型、厌氧型、厌
- 下列各组物质,同时放入适量的水中,可得到无色透明溶液的是 …………( ) A、CuSO4、H2SO4、FeCl3
- 下列过程中,没有发生膜融合的是( ) A.植物体细胞杂交 B.受精过程 C.氧进入细胞中的线粒体
- 下图表示人体内各类血细胞生成的途径。A.~f表示不同种类的细胞,①~⑥表示有关过程。(1)造血干细胞形成各种血细胞,需要
- 如图,AC=DF, AE=BD,BC=EF.求证:∠C=∠F. 【解析】利用三角形全等求解
- 地球自转产生了
- Growing up in the USA, I was ashamed of my mother’s Chinese
- 当今社会,能源问题是个重要的问题,而目本福岛核电站危机,使能源的安全问题更受关注。下列哪种能源的利用对环境的污染最小
- 已知Q与R的摩尔质量之比为9∶22,在反应X+2Y2Q+R中,当1.6 g X与Y完全反应后,生成4.4 g R,则参与
- 一个具有细胞核的活的植物细胞离体后培养就能表现全能性,而在植物体内却不表现出全能性,你认为下列解释比较合理的是( )
- 下列各图表示的变化中,只属于物理变化的是 ( )
- 某校化学兴趣小组参观制碱厂后,获得以下信息并对相关问题进行研究。 【产品与原理】 该厂采用“侯氏制碱法”生产化工产品——
- 我国少数民族中分布最广泛的是 ( ) A
- 商品 原料
- 阅读下列材料: 一位英国的宪法权威人士曾说:“上下两院如果作出决定,就是把女王本人的死刑判决书送到她面前,她也不得
- 随着科学技术的进步,我们的生活水平大大提高,同时也产生了一些新的问题。试用所学化学知识判断,下列说法或做法中错误的是A.
- 阅读下面一则材料,按要求回答问题。 李某,出生在一个富裕的家庭,自小父母就对其娇生惯养,以至于李某自私狭隘,蛮横粗暴。从
- 砹(At)是卤素中核电荷数最多的元素,推测砹或砹的化合物下列性质错误的是 A.砹为有色固体 B.H
- 下列关于统计图的描述错误的是 (
- 20世纪70年代初,跃居资本主义世界第二经济大国的是( ) A.德国 B.法国



