第3节 氧化还原反应 知识点题库
厨房中的化学知识很多,下面是有关厨房中的常见操作或者常见现象,其中不属于氧化还原反应的是()
A . 烧菜用过的铁锅,经放置常出现红棕色斑迹
B . 用煤气灶燃烧沼气(主要成分为甲烷:CH4)为炒菜提供热量
C . 牛奶久置变质腐败
D . 用醋酸除去水垢[主要成分是CaCO3、Mg (OH)2]
在KClO3+HCl→KCl+Cl2↑+H2O的反应中(未配平):
① 元素被氧化, 元素被还原(以上两空均填元素符号).
②配平该反应并用双线桥标出电子转移的方向和数目 .
在酸性介质中,往MnSO4溶液里滴加(NH4)2S2O8溶液会发生如下离子反应(未配平):Mn2++S2O82一+H2O→MnO4一+SO42一+H+ , 下列说法不正确的是( )
A . 氧化性比较:S2O82﹣>MnO4﹣
B . 氧化剂S2O82﹣的摩尔质量为 192 g/mol
C . 该反应中酸性介质可以为盐酸
D . 若有0.1 mol氧化产物生成,则转移电子 0.5 mol
下列比较中中正确的是( )
A . 氧化性:Mg2+>Al3+>Fe2+ >Cu2+
B . 熔沸点:Li>Na>K>Rb
C . 稳定性:H2O<NH3<CH4<HF
D . 原子半径:Cl>Si>F>H
反应8NH3+3Cl2=N2+6NH4Cl,被氧化的NH3与被还原的Cl2的物质的量之比为( )
A . 2∶3
B . 8∶3
C . 6∶3
D . 3∶2
氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一种反应物”在40℃~50℃时反应可生成它。CuH不稳定,易分解;CuH在氯气中能燃烧;跟盐酸反应能产生气体,以下有关的推断中错误的是( )
A . “另一种反应物”一定具有还原性
B . CuH既可做氧化剂也可做还原剂
C . CuH+Cl2=CuCl+HCl(燃烧)
D . CuH+HCl=CuCl+H2↑(常温)
下列说法中正确的是( )
A . 强电解质溶液导电能力一定强
B . 氧化还原反应的本质是元素化合价的升降
C . 阳离子只有氧化性,阴离子只有还原性
D . 氧化还原反应中,某元素由化合物变为单质,此元素可能被还原也可能被氧化
根据下列反应判断有关物质的氧化性由强到弱的顺序是 ( )
①2FeCl2+Cl2=2FeCl3; ②2FeCl3+2HI=2FeCl2+2HCl+I2;
③H2SO3+I2+H2O=2HI+H2SO4;
A . Cl2> FeCl3> I2> H2SO4
B . I2> FeCl3>H2SO4> Cl2
C . FeCl3>I2>H2SO4> Cl2
D . Cl2> FeCl3>H2SO4>I2
CO、NO及H2S都是有毒气体。下列有关这三种气体的说法正确的是( )
A . 都能与氧气反应
B . 都易溶于水
C . 都能与碱溶液反应
D . 都是电解质
40mL物质的量浓度为0.05mol▪L-1Na2SO3溶液恰好与25mL浓度为0.02mol▪L-1的K2X2O6溶液完全反应,已知Na2SO3可被K2X2O6氧化为Na2SO4 , 则元素X在还原产物中的化合价为下列的( )
A . +1价
B . +2价
C . +3价
D . +4价
下列反应中既属于化合反应,又属于氧化还原反应的是( )
A . SO2+H2O2=H2SO4
B . Zn+2AgNO3=Zn(NO3) 2+2Ag
C . 2HClO=2HCl+O2↑
D . CO2+2NaOH=Na2CO3+H2 O
下列反应中属于氧化还原反应又是吸热反应的是( )
A . 镁与盐酸反应放出氢气
B . 氢氧化钠与盐酸的反应
C . 硫在空气或氧气中燃烧
D . 灼热的炭与二氧化碳反应
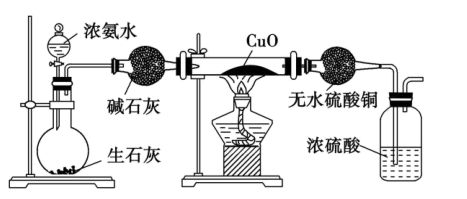
某课外活动小组在实验室用如图所示的装置进行实验,验证氨的某些性质并收集少量纯净干燥的 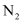 。
。
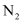 。
。 
-
(1) 碱石灰的作用是;
-
(2) 实验进行一段时间后,观察到加热的硬质玻璃管内的黑色氧化铜粉末变为红色,盛无水
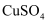 的干燥管内出现蓝色,并且在最后的出气导管处收集到纯净、干燥的
的干燥管内出现蓝色,并且在最后的出气导管处收集到纯净、干燥的 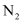 。
。 根据这些现象,写出硬质玻璃管内发生反应的化学方程式;该反应说明氨气具有。
A.碱性 B.还原性 C.氧化性 D.不稳定性
-
(3) 盛有浓氨水的玻璃仪器名称为;洗气瓶中浓
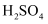 的主要作用是。
的主要作用是。
某油脂厂废弃的油脂加氢所用催化剂主要含金属Ni、Al、Fe及他们的氧化物,还有少量其他不溶性杂质。采用如图工艺流程回收其中的镍来制备硫酸镍晶体(NiSO4•7H2O):
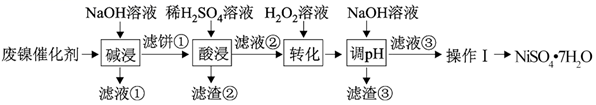 溶液中金属离子开始沉淀和完全沉淀的pH如表所示,回答下列问题:
溶液中金属离子开始沉淀和完全沉淀的pH如表所示,回答下列问题:
| 金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀时的pH(c=1.0mol•L-1) | 6.2 | 3.7 | 2.2 | 7.5 |
| 沉淀完全时的pH(c=1.0×10-5mol•L-1) | 8.7 | 4.7 | 3.2 | 9.0 |
-
(1) 废镍催化剂上的油脂在过程中被处理,滤液①中含有的无机阴离子有OH-、。
-
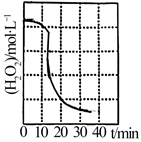
(2) “转化”过程中反应的化学方程式为,c(H2O2)随时间t的变化关系如图所示,反应开始10~20min内c(H2O2)迅速减小,原因是。
-
(3) 利用表格数据,计算Ni(OH)2的Ksp=,“转化”后的溶液中Ni2+的浓度为1.0mol•L-1 , “调pH”应控制的pH范围是。
-
(4) 进行操作I前通常要在滤液③中加入少量稀硫酸,作用为。
-
(5) 硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH,反应的离子方程式为。
二氧化氯(ClO2)是一种优良的消毒剂,可用氯酸钠和双氧水在酸性条件下制备,反应方程式为NaClO3+H2O2+H2SO4®ClO2+Na2SO4+H2O+O2(未配平)。下列说法错误的是( )
A . NaClO3做氧化剂,发生还原反应
B . 将该方程式配平后H2O的化学计量数应为2
C . NaClO3与H2O2的化学计量系数之比为2:1
D . 反应过程中每生成2.24LO2转移0.2mol电子
 是一种无色有臭鸡蛋气味的剧毒气体。将
是一种无色有臭鸡蛋气味的剧毒气体。将  通入
通入  与
与 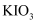 的混合溶液,发生如下反应:
的混合溶液,发生如下反应: 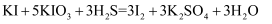 。下列说法正确的是( )
。下列说法正确的是( )
A .  是氧化剂,
是氧化剂, 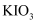 是还原剂
B . 每消耗
是还原剂
B . 每消耗 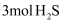 ,则转移电子的物质的量为
,则转移电子的物质的量为 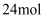 C . 若有
C . 若有 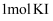 被氧化,则被
被氧化,则被  还原的
还原的 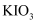 为
为 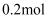 D . 被氧化的原子与被还原的原子的物质的量之比为
D . 被氧化的原子与被还原的原子的物质的量之比为 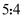
 是氧化剂,
是氧化剂, 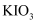 是还原剂
B . 每消耗
是还原剂
B . 每消耗 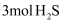 ,则转移电子的物质的量为
,则转移电子的物质的量为 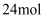 C . 若有
C . 若有 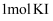 被氧化,则被
被氧化,则被  还原的
还原的 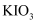 为
为 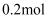 D . 被氧化的原子与被还原的原子的物质的量之比为
D . 被氧化的原子与被还原的原子的物质的量之比为 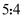
下列物质的应用与氧化还原反应无关的是( )
A . 利用铝热反应焊接铁轨
B . NaClO溶液用于公共环境杀菌消毒
C . 用硅胶作食品干燥剂
D . 用还原Fe粉作食品脱氧剂
氮化铝 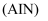 具有耐高温、抗冲击、导热性好等优良性能,广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:
具有耐高温、抗冲击、导热性好等优良性能,广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成: 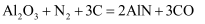
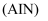 具有耐高温、抗冲击、导热性好等优良性能,广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:
具有耐高温、抗冲击、导热性好等优良性能,广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成: 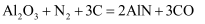
-
(1) 氮化铝中氮的化合价;生成
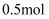 氮化铝转移电子的物质的量为。
氮化铝转移电子的物质的量为。
-
(2) 该反应中,氧化剂是,氧化产物。
回答下列问题:
-
(1) ①重晶石的化学式;②乙酸的结构简式。
-
(2) 实验室制氨气的化学反应方程式。
-
(3) 乙烯和氢气的化学反应方程式。
镍是一种硬而有延展性并具有铁磁性的金属,它能够高度磨光和抗腐蚀,工业上用红土镍矿[主要成分为 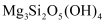 、
、  、NiO、
、NiO、 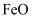 、
、  ]为原料,采用硫酸铵焙烧法选择性提取镍并回收副产物黄铵铁矾[化学式可表示为
]为原料,采用硫酸铵焙烧法选择性提取镍并回收副产物黄铵铁矾[化学式可表示为  ,摩尔质量为
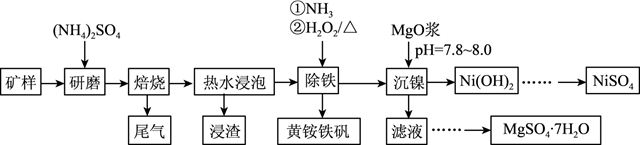
,摩尔质量为 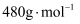 ]的工艺流程如图所示:
]的工艺流程如图所示:
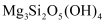 、
、  、NiO、
、NiO、 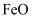 、
、  ]为原料,采用硫酸铵焙烧法选择性提取镍并回收副产物黄铵铁矾[化学式可表示为
]为原料,采用硫酸铵焙烧法选择性提取镍并回收副产物黄铵铁矾[化学式可表示为  ,摩尔质量为
,摩尔质量为 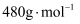 ]的工艺流程如图所示:
]的工艺流程如图所示:
已知:
①  ②
② 
-
(1) 除铁时加入的
 的用量高于理论用量的原因是。(写出2点)
的用量高于理论用量的原因是。(写出2点)
-
(2) 经分析矿样中大部分铁仍以氧化物形式存在于“浸渣”中,只有部分FeO在空气中焙烧时与
 反应生成
反应生成 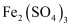 该反应的化学方程式为;“浸渣”的主要成分除含有铁元素的化合物外还有(填化学式)。
该反应的化学方程式为;“浸渣”的主要成分除含有铁元素的化合物外还有(填化学式)。
-
(3) 该工艺条件下,
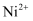 生成
生成 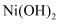 沉淀,
沉淀,  生成
生成 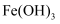 或黄铵铁矾沉淀,开始沉淀和沉淀完全时的pH如下表:
或黄铵铁矾沉淀,开始沉淀和沉淀完全时的pH如下表: 沉淀物
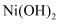
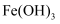
黄铵铁矾
开始沉淀时的pH
7.1
2.7
1.3
沉淀完全
 时的pH
时的pH9.2
3.7
2.3
若残留在浸出液中的铁完全转化为黄铵铁矾除去,“除铁”时通入
 调节溶液pH的范围是。
调节溶液pH的范围是。 -
(4) “沉镍”时pH调为8.0,滤液中
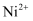 浓度约为mo/L
浓度约为mo/L 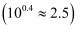 。
。
-
(5) 由所得滤液获得
 晶体时,常用无水乙醇代替蒸馏水作洗涤剂,原因是(写出2点)
晶体时,常用无水乙醇代替蒸馏水作洗涤剂,原因是(写出2点)
-
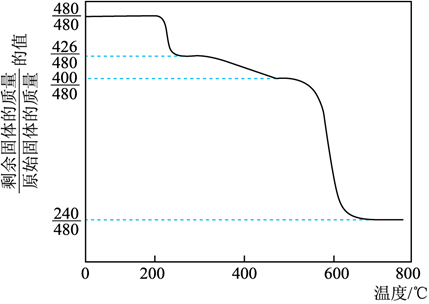
(6) 对黄铵铁巩进行热分解实验,其结果如下图所示,则黄铵铁矾的化学式为。(已知:黄铵铁矾在300℃前分解释放的物质为
 ,300-575℃之间只有
,300-575℃之间只有  和
和  放出,此时残留固体只存在Fe、O、S三种元素,670℃以上得到的是纯净的红棕色粉末)。
放出,此时残留固体只存在Fe、O、S三种元素,670℃以上得到的是纯净的红棕色粉末)。
最近更新
- 设集合A是由1,-2,a2-1三个元素构成的集合,集合B是由1,a2-3a,0三个元素构成的集合,若A=B,则实数a=_
- 在酸性条件下,可以水解生成相对分子质量相同的两种物质的有机物有( ) ①葡萄糖 ②蔗糖 ③麦芽糖 ④甲酸甲酯
- 某种零件模型可以看成如图所示的几何体(空心圆柱),该几何体的俯视图是()A. B. C. D.
- 下列关于夏、商、西周经济发展的说法不正确的是()。 A.今天家畜家禽的主要品种,西周时才齐全。 B.后代称为“五谷”的农
- 计算:
- —It's already eleven o'clock, and she______ have been here
- 为了使大众吃得明白、吃得健康,我国规定包装食品必须标注营养成分表,标注的内容包括能量以及4种核心营养素的含量值(碳水化合
- 现有硅酸钠、石灰石、二氧化硅三种白色粉末,只用一种试剂就可以将它们鉴别开,该试剂是( ) A.纯水
- 在△ABC中,三边长a,b,c满足a3+b3=c3,那么△ABC的形状为() A.锐角三角形
- 阅读下面的文字,完成下列小题。 曾国藩﹣﹣从“中人”到“完人”的追求(节选) 湘乡流传一个故事,说一个小偷在房梁上等着曾
- 下列各组括号内除杂的方法或试剂错误的是 A.Cu粉中混有Fe粉(
- 我国已禁止在公共场所吸烟,因为香烟燃烧会产生有毒物质,影响吸烟和被动吸烟者的健康,被动吸“二手烟”是因为() A.分子间
- There were smiling children all the way. Clearly they knew a
- 6.下列句子中,没有语病的一项是( ) A.这几年,随着社会对城市管理和城市文化的关注以及城管执法中一些事情的发生,
- 用30 N的力拉放在水平地面上的木箱,拉力F和地面成30°角斜向上.画出拉力F的图示和示意图.
- 昆虫分布广,活动范围大,主要原因是昆虫有 A.足 B.外骨骼
- “再现历史场景,弘扬民族精神”是历史影视剧的主题,若要再现邓世昌率领中国海军抗击日本侵略者的悲壮场景,应该选择的素材是
- 幸福是什么?幸福有时是一种拥有,有时是一种等待,有时是一种感动。收获是一种幸福,付出也是一种幸福;功成名就是幸福,淡泊宁
- 如图所示是小明测量物体质量的情景,明显的操作错误是: (1)__________________________
- 若曲线:在点处的切线与直线垂直,则= .



