第2节 研究物质性质的方法和程序 知识点题库
将一小块钠放入下列溶液时,既能产生气体,又会出现白色沉淀的是 ( )
A . 稀盐酸
B . 氢氧化钠稀溶液
C . 硫酸铜溶液
D . 氯化镁溶液
A、B、C、D、F五种物质的焰色反应均为黄色,A、B、C、D与盐酸反应均生成E,此外B还生成一种可燃气体.而C、D还生成一种无色无味气体H,该气体能使澄清石灰水变浑浊.D和A可反应生成C,F和H也可反应生成C和另一种无色无味气体.请回答下列问题:
(1)写出A、B、C、D、E、F的化学式
(2)写出F和H反应的化学方程式 .
(3)写出下列反应的离子方程式:
①D+盐酸 .
②B+水 .
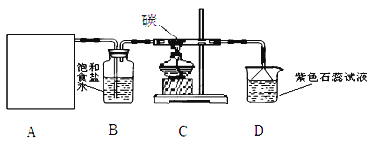
实验室用浓盐酸和MnO2制取并探究Cl2化学性质,装置图如图所示:
-
(1) A是氯气发生装置,请完成反应的离子方程式为 除了酒精灯和导管外,还用到的玻璃仪器有
-
(2) 从C装置出来的气体中含有CO2和HCl,写出C中反应的化学方程式
-
(3) 同学们在实验中发现:若用稀盐酸代替浓盐酸与MnO2混合加热没有氯气生成.“影响氯气生成的原因是什么呢?”,同学们作了如下探究:
①提出合理假设
假设1:Cl﹣的浓度对反应的影响;假设2:
下列说法中不正确的是( )
A . P2O5可用于干燥Cl2和NH3
B . NO2溶于水时发生氧化还原反应
C . 可用蘸浓盐酸的棉棒检验输送氨气的管道是否漏气
D . 液氨汽化时要吸收大量的热,可用作制冷剂
将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO﹣和ClO3﹣两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法不正确的是( )

A . Cl2和苛性钾溶液在不同温度下可能发生不同反应
B . 反应中转移电子数为是0.21 NA
C . 原苛性钾溶液中KOH的物质的量无法确定
D . 生成物中Cl﹣的物质的量为 0.21 mol
下列说法正确的是( )
①将足量的Na2O、Na2O2分别加入到酚酞溶液中,最终溶液均为红色
②金刚石用于制造切割刀具,石墨用于制造电极、铅笔芯.
③强电解质溶液的导电能力不一定比弱电解质溶液的导电能力强
④氯气的性质活泼,它与氢气混合后立即发生爆炸
⑤胶体和溶液的本质区别是胶体能发生丁达尔现象.
⑥工业上常用Cl2和石灰乳反应来制取漂白粉.
A . ①②④
B . ②③⑥
C . ②⑤⑥
D . ④⑤⑥
下列说法错误的是( )
A . 乙醇、苯应密封保存,置于阴凉处,且远离火源
B . 金属钠着火时,可用细沙覆盖灭火
C . 容量瓶和滴定管使用之前必须检查是否漏水
D . 配制浓硫酸、浓硝酸的混酸时,应将浓硝酸沿玻璃棒缓慢注入浓硫酸中
下列推理正确的是( )
A . 铝粉在氧气中燃烧生成Al2O3 , 故铁丝在氧气中燃烧生成Fe2O3
B . 钠与氧气、水等反应时钠作还原剂,故金属单质参与反应可作还原剂
C . 活泼金属钠保存在煤油中,故活泼金属铝也保存在煤油中
D . 铁能从硫酸铜溶液中置换出铜,故钠也能从硫酸铜溶液中置换出铜
向某含有SO  、SiO
、SiO  、CO
、CO  、Br-、Na+的溶液中缓慢通入Cl2直至过量,下列对该反应过程的判断错误的是( )
、Br-、Na+的溶液中缓慢通入Cl2直至过量,下列对该反应过程的判断错误的是( )
 、SiO
、SiO  、CO
、CO  、Br-、Na+的溶液中缓慢通入Cl2直至过量,下列对该反应过程的判断错误的是( )
、Br-、Na+的溶液中缓慢通入Cl2直至过量,下列对该反应过程的判断错误的是( )
A . 整个过程共发生2个氧化还原反应
B . 所有阴离子的浓度都发生了变化
C . 溶液的颜色发生了变化
D . 反应过程中既有气体产生,也有沉淀产生
几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 | X | Y | Z | M | R | Q | |
| 原子半径(×10-10 m) | 1.86 | 0.99 | 1.43 | 1.60 | 0.75 | 0.74 | |
| 主要化 合价 | 最高正价 | +1 | +7 | +3 | +2 | +5 | — |
| 最低负价 | — | -1 | — | — | -3 | -2 | |
下列说法正确的是 ( )
A . 元素X和Q形成的化合物呈淡黄色
B . X、Z、R的最高价氧化物的水化物之间可两两相互反应
C . Q2-比R3-更容易失去电子
D . M(OH)2的碱性比XOH的碱性强
检验HCl气体中是否混有Cl2,可采取的方法是( )
A . 用干燥的蓝色石蕊试纸
B . 用干燥的有色布条
C . 将气体通入AgNO3溶液
D . 用湿润的红色布条
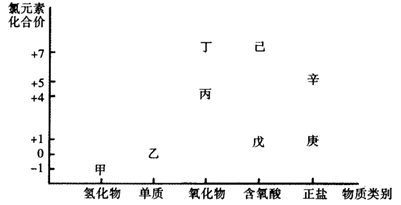
利用图像,可以从不同角度研究含氯物质的性质及其转化关系,图中甲~辛均含氯元素。回答下列问题:
-
(1) 丙的化学式为,用途之一是;丁属于(“酸性”或”碱性”)氧化物。
-
(2) 根据氯元素的化合价判断,乙物质。
a.只有氧化性 b.既有氧化性又有还原性 c.只有还原性
-
(3) 电解甲溶液制备己的化学反应为甲+H2O
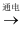 己+H2↑(未配平),配平后参与反应的甲与H2O的计量数之比是。
己+H2↑(未配平),配平后参与反应的甲与H2O的计量数之比是。
-
(4) 若庚是漂粉精的有效成分,存放不当,在空气中易失效。原因是(用化学方程式表示)。
某兴趣小组为探究  和
和  的性质,将两种气体同时通入水中,实验装置如图:
的性质,将两种气体同时通入水中,实验装置如图:
 和
和  的性质,将两种气体同时通入水中,实验装置如图:
的性质,将两种气体同时通入水中,实验装置如图: 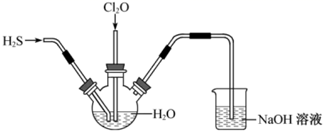
请回答:
-
(1) 三颈瓶中出现淡黄色沉淀,溶液呈强酸性,用一个化学方程式表示。
-
(2) 若通入水中的
 已过量,设计实验方案检验。
已过量,设计实验方案检验。
如图所示,A处通入干燥的氯气,打开B阀后,C处的红布条不褪色,关闭B阀时,C处的红布条逐渐褪色,则D瓶中装的是( )
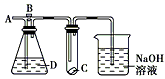
A . 浓KOH溶液
B . 浓硫酸
C . 饱和NaCl溶液
D . 浓NaOH溶液
下列说法错误的是( )
A . 研究物质组成时,常用原子吸收光谱确定物质中含有哪些金属元素
B . NaHCO3固体可以做干粉灭火剂,金属钠着火可以用其来灭火
C . 二氧化硫可以抑制酒中细菌生长,可在葡萄酒中微量添加
D . 液氨汽化时吸收大量的热,工业上可使用液氨作制冷剂
根据要求,回答下列问题:
-
(1) Ⅰ.如图为实验室在加热条件下利用二氧化锰和浓盐酸反应制取氯气并验证氯气的某些性质的实验装置。E瓶内放有干燥的红色布条;F的玻璃管中放有红色的铜网。
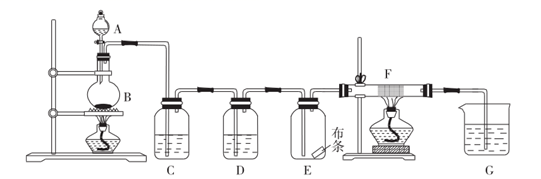
装置C中盛装的溶液是,D中试剂的作用是。
-
(2) 实验中,E瓶内干燥的红色布条(填“褪色”或“不褪色”),说明干燥的氯气(填“具有”或“不具有”)漂白作用。
-
(3) F中反应的化学方程式为。
-
(4) 装置G的作用是,发生反应的离子方程式为。
-
(5) Ⅱ.某实验小组利用以下装置制取并探究氨气的性质:
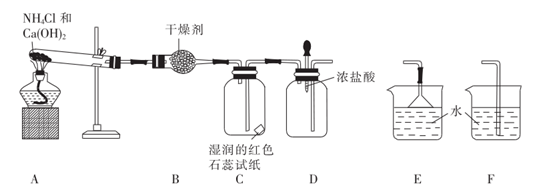
装置A中发生反应的化学方程式为。
-
(6) 装置B中的干燥剂是(填名称)。
-
(7) 装置C中的现象是。
-
(8) 实验进行一段时间后,挤压装置D中的胶头滴管,滴入
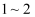 滴浓盐酸,可观察到的现象是。
滴浓盐酸,可观察到的现象是。
-
(9) 为防止过量氨气外逸,需要在上述装置的末端增加一个尾气吸收装置,应选用的装置是(填“E”或“F”),尾气吸收过程中发生反应的化学方程式为。
下列说法错误的是( )
A . 还原铁粉常用作食品干燥剂
B . 硬铝(一种铝合金)密度较小、强度高,可用于制造飞机和宇宙飞船部件
C . 氯气、臭氧、二氧化氯都可用于饮用水的消毒
D . 过氧化钠可在呼吸面具或潜水艇中作为供氧剂
利用如图可从不同角度研究含氯物质的性质及其转化关系。回答下列问题:
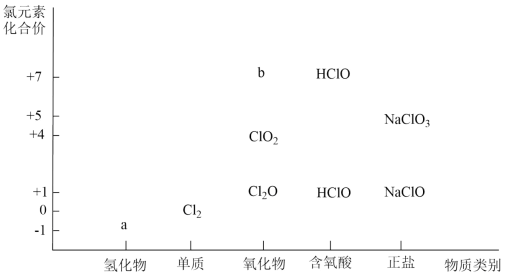
-
(1) a物质的化学式为,b属于 (填“酸性”或“碱性”)氧化物。
-
(2) 用ClO2消毒水时,ClO2还可将水中的Fe2+转化为Fe3+ , Fe3+再水解生成Fe(OH)3胶体,说明ClO2具有性,检验有胶体生成的简便方法是。
-
(3) 工业上可以用反应2NaClO3+H2SO4+SO2=2ClO2+2NaHSO4 , 制备ClO2 , 若生成1molClO2 , 则反应中转移电子的物质的量为。
-
(4) 实验室可用二氧化锰与浓盐酸在加热条件下制取氯气,写出该反应的化学方程式:。
①浓盐酸在该反应中体现的性质有 (填字母)。
A.还原性 B.氧化性 C.酸性
②若上述反应中产生0.2molCl2 , 需消耗MnO2的质量为 g。
化学反应中常涉及到多彩的颜色变化,下列对颜色变化的描述错误的是( )
A . 用 试纸检验过氧化钠与水反应之后溶液的酸碱性,
试纸检验过氧化钠与水反应之后溶液的酸碱性, 试纸变蓝色
B . 氯气通入放置干燥红色布条的集气瓶中,布条红色褪去
C . 金属钠在空气中燃烧生成淡黄色粉末,露置在空气中一段时间逐渐变成白色
D . 氯水久置,溶液颜色由浅黄绿色变为无色
试纸变蓝色
B . 氯气通入放置干燥红色布条的集气瓶中,布条红色褪去
C . 金属钠在空气中燃烧生成淡黄色粉末,露置在空气中一段时间逐渐变成白色
D . 氯水久置,溶液颜色由浅黄绿色变为无色
 试纸检验过氧化钠与水反应之后溶液的酸碱性,
试纸检验过氧化钠与水反应之后溶液的酸碱性, 试纸变蓝色
B . 氯气通入放置干燥红色布条的集气瓶中,布条红色褪去
C . 金属钠在空气中燃烧生成淡黄色粉末,露置在空气中一段时间逐渐变成白色
D . 氯水久置,溶液颜色由浅黄绿色变为无色
试纸变蓝色
B . 氯气通入放置干燥红色布条的集气瓶中,布条红色褪去
C . 金属钠在空气中燃烧生成淡黄色粉末,露置在空气中一段时间逐渐变成白色
D . 氯水久置,溶液颜色由浅黄绿色变为无色
下列说法错误的是( )
A . 金属钠可用于钛、锆、铌、钽等金属的冶炼
B .  消毒液的主要成分为次氯酸钠
C . 可用pH试纸测定次氯酸盐溶液的酸碱性
D . 小苏打与食醋混合使用,发面效果更好
消毒液的主要成分为次氯酸钠
C . 可用pH试纸测定次氯酸盐溶液的酸碱性
D . 小苏打与食醋混合使用,发面效果更好
 消毒液的主要成分为次氯酸钠
C . 可用pH试纸测定次氯酸盐溶液的酸碱性
D . 小苏打与食醋混合使用,发面效果更好
消毒液的主要成分为次氯酸钠
C . 可用pH试纸测定次氯酸盐溶液的酸碱性
D . 小苏打与食醋混合使用,发面效果更好
最近更新
- 利用物体自由落体运动,做《验证机械能守恒定律》的实验: (1)已备好的器材有:打点计时器,固定计时器用的夹子、铁架台、纸
- 古人云:“少而好学,如日出之阳;壮而好学,如日中之光;老而好学,如炳烛之明”。今日西方教育家断言:“不提高就死亡。”这给
- 如下图所示,甲地所在的地形区是A.内蒙古高原 B.柴达木盆地 C.四川盆地
- 利用下列仪器制取相关气体,不能实现的是 A.用锌和稀硫酸制取氢气 B.用双氧水和二氧化锰制取氧气 C.用高锰酸
- 不属于碳元素的同素异形体的是 A、金刚石 B、石墨 C、碳60 D、一氧化碳
- (本题满分10分) 选修4-5:不等式选讲 (1)解关于x的不等式; (2)若关于的不等式有解,求实数的取值范围.
- 如图是某分子的比例模型,黑色的是碳原子,白色的是氢原子,灰色的是氧原子。该分子是A.C2H5OH
- Wall Street is the banking center of New York City. But how
- 逝去的岁月值得追忆,与亲人相聚的时光值得追忆,同学、朋友共度的时光值得追忆……多少往事值得追忆啊!请以“追忆”为题写一篇
- (06年江西卷理)(12分)如图,在三棱锥A-BCD中,侧面ABD、ACD是全等的直角三角形,AD是公共的斜边,且AD=
- 在蚕豆叶的叶肉细胞中,既含有DNA,又有双层膜的结构是( ) ①细胞核 ②线粒体 ③核糖体 ④中心体 ⑤内质网 ⑥
- 阅读文章,回答问题。(12分)成全一棵树⑴一个平常的春天,一位饱经风霜的母亲,向别人讨了几棵树苗。她要把树苗栽在门前。⑵
- There’s ______ an English evening in our school. A. have
- 王杰同学在课外实践活动中自制了一个可调节亮度的台灯,他设计的电路如图16所示.灯泡上标有“220V 40W”,滑动变阻器
- 近年来,福建和台湾两岸的中华儿女定期地进行祭拜“妈祖”的大型民间活动。“妈祖”文化现象与宗法制有密切关系,在宗法制中,大
- 对下列句子中加点词语的解释不正确的一项是() A.第三个身量未足,形容(身体面貌)尚小。 B.身体面庞虽
- 小宁设计了一种照明电路图,其设计要求是:用两个开关控制一盏灯,两个开关同时闭合灯才能发光,只闭合其中任意一个开关都不能发
- 下列说法正确的是: A.将pH均为a的氢氧化钠溶液和氨水分别加水稀释100倍,pH变为b和c, 则a、b、c的大小关系是
- (12分)A、B、C、D、E代表5种元素。请填空: (1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其轨
- 红细胞吸收无机盐和葡萄糖的共同点是 A.都可以从低浓度一边向高浓度一边 B.都需要供给ATP C.都需要载体协助



